
ЁОЬтФПЁПЮхжжЖЬжмЦкдЊЫиXЁЂYЁЂZЁЂWЁЂQЕФдзгађЪ§вРДЮдіЁЃXЁЂYЪЧЗЧН№ЪєдЊЫиXЁЂYЁЂQдЊЫиЕФдзгзюИпФмМЖЩЯЕчзгЪ§ЯрЕШЃЛZдЊЫидзгЕФзюЭтВуЕчзгЪ§ЪЧДЮЭтВуЕФСНБЖЃЛWдЊЫидзгКЫЭтгаШ§жжВЛЭЌЕФФмМЖЧвдзгжаpбЧВугыsбЧВуЕчзгзмЪ§ЯрЕШЃЛQдЊЫиЕчРыФмЗжБ№ЪЧI1=496ЃЌI2=4562ЃЌI3=6912ЁЃЛиД№ЯТСаЮЪЬтЃК
(1)ЛљЬЌQдзгЕФКЫЭтЕчзгХХВМЪНЪЧ____________________ЁЃ
(2)QЁЂWаЮГЩЕФЛЏКЯЮяQ2W2жаЕФЛЏбЇМќРраЭЪЧ______________ЁЃ
(3)YФмгыЗњдЊЫиаЮГЩYF3ЃЌИУЗжзгЕФПеМфЙЙаЭЪЧ_______ЃЌИУЗжзгЪєгк______Зжзг(ЬюЁАМЋадЁБЛђЁАЗЧМЋадЁБ)ЁЃYгыXПЩаЮГЩОпгаСЂЬхНсЙЙЕФЛЏКЯЮяY2X6ЃЌИУНсЙЙжаYВЩгУ______дгЛЏЁЃ
(4)Y(OH)3ЪЧвЛдЊШѕЫсЃЌЦфжаYдзгвђШБЕчзгЖјвзаЮГЩХфЮЛМќЃЌаДГіY(OH)3дкЫЎШмвКжаЕФЕчРыЗНГЬЪН_______________ЁЃ
(5) ZЕФвЛжжЕЅжЪОЇАћНсЙЙШчЯТЭМЫљЪОЁЃ
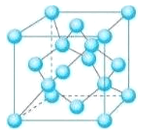
ЂйИУЕЅжЪЕФОЇЬхРраЭЮЊ___________ЁЃ
ЂкКЌ1 mol ZдзгЕФИУОЇЬхжаЙВга_____molЛЏбЇМќЁЃ
ЂлМКжЊZЕФЯрЖддзгжЪСПЮЊMЃЌдзгАыОЖЮЊr pmЃЌАЂЗќйЄЕТТоГЃЪ§ЕФжЕЮЊNAЃЌдђИУОЇЬхЕФУмЖШЮЊ____gЁЄcm-3ЁЃ
ЁОД№АИЁП [Ne]3s1(Лђ1s22s22p63s1) РызгМќЁЂЗЧМЋадОЎМлМќ ЦНУцШ§НЧаЮ ЗЧМЋад ЃЉsp3 B(OH)3+H2O![]() [B(OH)4]-+H+ дзгОЇЬх 2
[B(OH)4]-+H+ дзгОЇЬх 2 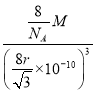 Лђ
Лђ![]() ЁС1030
ЁС1030
ЁОНтЮіЁПZдЊЫидзгЕФзюЭтВуЕчзгЪ§ЪЧДЮЭтВуЕФСНБЖЃЌдђZЮЊЬМдЊЫиЃЛWдЊЫидзгКЫЭтгаШ§жжВЛЭЌЕФФмМЖЧвдзгжаpбЧВугыsбЧВуЕчзгзмЪ§ЯрЕШЃЌдђЦфЕчзгХХВМЪНЮЊ1s22s22p4ЃЌЮЊOдЊЫиЃЛQдЊЫиЕчРыФмЗжБ№ЪЧI1=496ЃЌI2=4562ЃЌI3=6912ЃЌЫЕУїзюЭтВуЪЧ1ИіЕчзгЃЌдђQЮЊNaдЊЫиЃЛдйНсКЯXЁЂYЁЂZЁЂWЁЂQЕФдзгађЪ§вРДЮдіЁЂXЁЂYЪЧЗЧН№ЪєдЊЫиXЁЂYЁЂQдЊЫиЕФдзгзюИпФмМЖЩЯЕчзгЪ§ЯрЕШПЩжЊXЮЊHЃЌYЮЊBЃЛ
(1)NaЕФКЫЕчКЩЪ§ЮЊ11ЃЌЛљЬЌNaдзгЕФКЫЭтЕчзгХХВМЪНЪЧ[Ne]3s1(Лђ1s22s22p63s1) ЃЛ
(2) NaЁЂOаЮГЩЕФЛЏКЯЮяNa2O2жаКЌгаNa+КЭO22-ЃЌдђЫљКЌЛЏбЇМќРраЭЪЧРызгМќКЭЗЧМЋадЙВМлМќЃЛ
(3)BF3ЗжзгжааФBдзгЙТЕчзгЖдЪ§=![]() =0ЃЌМлВуЕчзгЖдЪ§=3+0=3ЃЌЙЪBдзгВЩШЁsp2дгЛЏЃЌVSEPRЙЙаЭЮЊЦНУцШ§НЧаЮЃЌЗжзгЕФСЂЬхЙЙаЭЮЊЦНУцШ§НЧаЮЃЛBF3жаBдЊЫиЛЏКЯМлЮЊ+3ЃЌBдзгзюЭтВу3ИіЕчзгШЋВПГЩМќЃЌЮЊЗЧМЋадЗжзгЃЛдкB2H6ЗжзгжааФBдзгЙТЕчзгЖдЪ§=
=0ЃЌМлВуЕчзгЖдЪ§=3+0=3ЃЌЙЪBдзгВЩШЁsp2дгЛЏЃЌVSEPRЙЙаЭЮЊЦНУцШ§НЧаЮЃЌЗжзгЕФСЂЬхЙЙаЭЮЊЦНУцШ§НЧаЮЃЛBF3жаBдЊЫиЛЏКЯМлЮЊ+3ЃЌBдзгзюЭтВу3ИіЕчзгШЋВПГЩМќЃЌЮЊЗЧМЋадЗжзгЃЛдкB2H6ЗжзгжааФBдзгЙТЕчзгЖдЪ§=![]() =0ЃЌМлВуЕчзгЖдЪ§=4+0=4ЃЌЙЪBдзгВЩШЁsp3дгЛЏЃЛ
=0ЃЌМлВуЕчзгЖдЪ§=4+0=4ЃЌЙЪBдзгВЩШЁsp3дгЛЏЃЛ
(4)B(OH)3жаBдзгвђШБЕчзгЖјвзгыЫЎЕчРыГіЕФOH-жабѕдзгМфаЮГЩХфЮЛМќЃЌДйНјЫЎЕФЕчРыЃЌЪЙЕУШмвКЯдЫсадЃЌдђB(OH)3дкЫЎШмвКжаЕФЕчРыЗНГЬЪНЮЊB(OH)3+H2O![]() [B(OH)4]-+H+ ЃЛ
[B(OH)4]-+H+ ЃЛ
(5) ЂйЬМдзгМфЭЈЙ§CЁЊCМќаЮГЩСЂЬхЭјзДНсЙЙЃЌДЫОЇЬхРраЭЮЊдзгОЇЬхЃЛ
ЂкгЩОЇАћНсЙЙПЩжЊЃЌУПИіЬМдзгЦНОљаЮГЩ2ИіCЁЊCМќЃЌКЌ1mol CдзгЕФИУОЇЬхжаЙВга2molЛЏбЇМќЃЛ
ЂлОЇАћжаЬМдзгЪ§ФПЮЊ4+8ЁС![]() +6ЁС
+6ЁС![]() =8ЃЌдђОЇАћЕФжЪСПЮЊ8ЁС
=8ЃЌдђОЇАћЕФжЪСПЮЊ8ЁС![]() gЃЌДІгкЬхЖдНЧЯпЩЯЕФCдзгЯрСкЃЌШєCдзгАыОЖЮЊ(rЁС10-10)cmЃЌдђОЇАћЬхЖдНЧЯпГЄЖШЮЊ8(rЁС10-10)cmЃЌдђОЇАћРтГЄЮЊ
gЃЌДІгкЬхЖдНЧЯпЩЯЕФCдзгЯрСкЃЌШєCдзгАыОЖЮЊ(rЁС10-10)cmЃЌдђОЇАћЬхЖдНЧЯпГЄЖШЮЊ8(rЁС10-10)cmЃЌдђОЇАћРтГЄЮЊ cmЃЌдђИУОЇЬхЕФУмЖШЮЊ[8ЁС
cmЃЌдђИУОЇЬхЕФУмЖШЮЊ[8ЁС![]() g]ЁТ[
g]ЁТ[ ]3cm3=
]3cm3=![]() ЁС1030gЁЄcm-3ЁЃ
ЁС1030gЁЄcm-3ЁЃ



| ФъМЖ | ИпжаПЮГЬ | ФъМЖ | ГѕжаПЮГЬ |
| ИпвЛ | ИпвЛУтЗбПЮГЬЭЦМіЃЁ | ГѕвЛ | ГѕвЛУтЗбПЮГЬЭЦМіЃЁ |
| ИпЖў | ИпЖўУтЗбПЮГЬЭЦМіЃЁ | ГѕЖў | ГѕЖўУтЗбПЮГЬЭЦМіЃЁ |
| ИпШ§ | ИпШ§УтЗбПЮГЬЭЦМіЃЁ | ГѕШ§ | ГѕШ§УтЗбПЮГЬЭЦМіЃЁ |
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЁОШЋЙњАйЧПаЃ.2017НьНЫеЪЁбЮГЧжабЇИпШ§ЯТбЇЦкПЊбЇПМЪдЁП
ГЃЮТЯТЃЌЯђ10mL0.1molЁЄLЃ1H2AШмвКжаж№ЕЮМгШы0.1molЁЄLЃ1NaOHШмвКЁЃгаЙиЮЂСЃЕФЮяжЪЕФСПБфЛЏШчЭМЃЈЦфжаЂёДњБэH2AЃЌЂђДњБэHA-ЃЌЂѓДњБэA2-ЃЉЁЃИљОнЭМЪОЗжЮіХаЖЯЃЌЯТСаЮЂСЃХЈЖШДѓаЁЙиЯЕе§ШЗЕФЪЧ

A. ЕБv=0ЪБЃЌc(H+)=c(OH-)+c(HA-)+c(A2-)
B. ЕБv=10ЪБЃЌc(Na+)=c(H2A)+c(HA-)+c(A2-)
C. ЕБv=20ЪБЃЌc(Na+)ЃОc(A2-)ЃОc(HA-)ЃОc(OH-)ЃОc(H+)
D. ЕБpH=7ЪБЃЌc(Na+)ЃОc(HA-)+ c(A2-)
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЕБЙтЪјЭЈЙ§ЯТСаЗжЩЂЯЕЪБЃЌФмЙлВьЕНЖЁДяЖћаЇгІЕФЪЧЃЈ ЃЉ
A.ЕэЗлШмвК
B.ФрЫЎ
C.NaCl ШмвК
D.ХЈбЮЫс
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТСаЮяжЪЖМПЩвдЬэМгЕНЪГЦЗжаЃЌЦфжаЪЙгУЪББиаыбЯИёПижЦгУСПЕФЪЧ
AЃЎЪГДз BЃЎесЬЧ CЃЎСЯОЦ DЃЎбЧЯѕЫсФЦ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЯТЭМжаaЁЂbЗжБ№ЪЧдЕчГиЕФСНМЋЃЌНгЭЈЕчТЗКѓЗЂЯжaМЋАхжЪСПдіМгЃЌbМЋАхШмНтЃЌЗћКЯетвЛЧщПіЕФЪЧ( )
aМЋАх | bМЋАх | aЕчМЋ | ZШмвК | |
A | аП | ЪЏФЋ | ИКМЋ | CuSO4 |
B | ЪЏФЋ | ЪЏФЋ | ИКМЋ | NaOH |
C | вј | Ьњ | е§МЋ | AgNO3 |
D | Э | ЪЏФЋ | е§МЋ | CuCl2 |

A. A B. B C. C D. D
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПвбжЊвдЯТаХЯЂЃКЂй1 mol N2ЕФЙВМлМќЖЯСбЮќЪе946 kJЕФФмСПЃЛ1 mol H2ЕФЙВМлМќЖЯСбЮќЪе436 kJЕФФмСПЃЛаЮГЩ1 mol NH3жаЕФЛЏбЇМќЪЭЗХ1 173 kJЕФФмСПЁЃЂкНЋвЛЖЈСПЕФN2КЭH2ЭЖШывЛУмБеШнЦїжаЃЌдквЛЖЈЬѕМўЯТНјааЗДгІЃЌВтЕУгаЙиЪ§ОнШчЯТЃК
N2(molЁЄLЃ1) | H2(molЁЄLЃ1) | NH3(molЁЄLЃ1) | |
Ц№ЪМЪБ | 3 | 3 | 0 |
2sФЉ | 2.6 | 1.8 | 0.8 |
ИљОнвдЩЯЯрЙиЪ§ОнЛиД№ЮЪЬтЃК
(1)гУH2БэЪОИУЗДгІ2 sФкЕФЦНОљЗДгІЫйТЪЮЊ________
(2)______(ЬюЁАФмЁБЛђЁАВЛФмЁБ)ШЗШЯИУЗДгІ2 sФЉвбДяЛЏбЇЦНКтзДЬЌЁЃ
(3)аДГіИУЗДгІЕФЛЏбЇЗНГЬЪНЃК
________________________________________________________________________ЁЃ
(4)ЕЊЦјКЭЧтЦјЩњГЩАБЦјЕФЙ§ГЬ______(ЬюЁАЪЭЗХЁБЛђЁАЮќЪеЁБ)ФмСПЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПЂё.ИпДПЖШЧтбѕЛЏУОЙуЗКгІгУгквНвЉЁЂЕчСІЕШСьгђЁЃУОЙшЫсбЮПѓЪЏПЩгУгкЩњВњЧтбѕЛЏУОЃЌМђвЊЙЄвеСїГЬШчЭМЫљЪОЃК
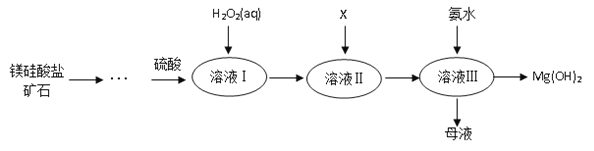
вбжЊЃК
ЂйШмвКЂёжаГ§КЌMg2+ЁЂSO42ЭтЃЌЛЙКЌгаЩйСПFe3+ЁЂAl3+ЁЂFe2+ЕШРызгЃЛ
ЂкГЃЮТЯТЃЌМИжжН№ЪєРызгПЊЪМГСЕэКЭГСЕэЭъШЋЪБЕФpHШчЯТБэЫљЪОЃК
Н№ЪєРызг | Fe3+ | Al3+ | Fe2+ | Mg2+ |
ПЊЪМГСЕэЪБЕФpH | 1.5 | 3.3 | 6.5 | 9.4 |
ГСЕэЭъШЋЪБЕФpH | 3.7 | 5.2 | 9.7 | 12.4 |
ЧыЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉУОдкдЊЫижмЦкБэжаЕФЮЛжУ_______________ЃЛ
ЃЈ2ЃЉЯђШмвКЂђжаМгШыЪдМСXЪЧ_____________ЃЌзїгУЪЧ_________________________ЃЛ
ЃЈ3ЃЉСїГЬжаВЛМгH2O2в§Ц№ЕФКѓЙћЪЧ___________________________________ЃЛ
ЃЈ4ЃЉЫЕГіФИвКЕФвЛжжгУЭО___________________ЃЛ
ЃЈ5ЃЉМгШыH2O2ШмвКЗЂЩњЗДгІЕФРызгЗНГЬЪНЪЧ___________________ЃЛ
Ђђ.КЃЫЎжаКЌгаЗсИЛЕФУОзЪдДЁЃФГЭЌбЇЩшМЦСЫДгФЃФтКЃЫЎжажЦБИMgOЕФЪЕбщЗНАИЃК
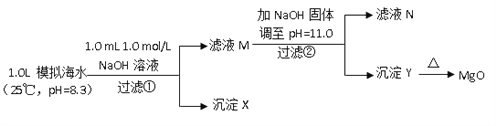
ФЃФтКЃЫЎжаЕФРызгХЈЖШ/ ЃЈmol/LЃЉ | Na+ | Mg2+ | Ca2+ | ClЃ | HCO3Ѓ |
0.439 | 0.050 | 0.011 | 0.560 | 0.001 |
зЂЃКШмвКжаФГжжРызгЕФХЈЖШаЁгк1.0ЁС10Ѓ5mol/LЃЌПЩШЯЮЊИУРызгВЛДцдкЃЛЪЕбщЙ§ГЬжаЃЌМйЩшШмвКЬхЛ§ВЛБфЁЃ
вбжЊЃКKsp(CaCO3)ЃН4.96ЁС10Ѓ9ЃЛKsp(MgCO3)ЃН6.82ЁС10Ѓ6ЃЛKsp [Ca(OH)2]ЃН4.68ЁС10Ѓ6ЃЛKsp [Mg(OH)2]ЃН5.61ЁС10Ѓ12ЁЃЧыЛиД№ЯТСаЮЪЬтЃК
ЃЈ6ЃЉГСЕэЮяXЮЊ_____________ЃЛ
ЃЈ7ЃЉТЫвКNжаCa2ЃЋХЈЖШЮЊ_______________ЃЛ
ЃЈ8ЃЉМгNaOHЙЬЬхЕїећpH=12.5ЪЧЗёПЩаа______ЃЈЬюЁАЪЧЁБЁАЗёЁБЃЉЃЛдвђЪЧ________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПМффхБНМзШЉЃЈ![]() ЃЉЃЌЪЧЯуСЯЁЂШОСЯЁЂгаЛњКЯГЩжаМфЬхЃЌГЃЮТБШНЯЮШЖЈЃЌИпЮТвзБЛбѕЛЏЁЃЯрЙиЮяжЪЕФЗаЕуШчЯТЃЈ101kPaЃЉЁЃ
ЃЉЃЌЪЧЯуСЯЁЂШОСЯЁЂгаЛњКЯГЩжаМфЬхЃЌГЃЮТБШНЯЮШЖЈЃЌИпЮТвзБЛбѕЛЏЁЃЯрЙиЮяжЪЕФЗаЕуШчЯТЃЈ101kPaЃЉЁЃ
ЮяжЪ | ЗаЕу/Ёц | ЮяжЪ | ЗаЕу/Ёц |
фх | 58.8 | 1ЃЌ2ЃЖўТШввЭщ | 83.5 |
БНМзШЉ | 179 | МффхБНМзШЉ | 229 |
ЦфЪЕбщЪвжЦБИВНжшШчЯТЃК
ВНжш1ЃКНЋШ§ОБЦПжаЕФвЛЖЈХфБШЕФЮоЫЎAlCl3ЁЂ1ЃЌ2ЃЖўТШввЭщКЭБНМзШЉГфЗжЛьКЯКѓЃЌЩ§ЮТжС60ЁцЃЌЛКТ§ЕЮМгОХЈСђЫсИЩдяЙ§ЕФвКфхЃЌБЃЮТЗДгІвЛЖЮЪБМфЃЌРфШДЁЃ
ВНжш2ЃКНЋЗДгІЛьКЯЮяЛКТ§МгШывЛЖЈСПЕФЯЁбЮЫсжаЃЌНСАшЁЂОВжУЁЂЗжвКЁЃгаЛњЯргУ10%NaHCO3ШмвКЯДЕгЁЃ
ВНжш3ЃКОЯДЕгЕФгаЛњЯрМгШыЪЪСПЮоЫЎMgSO4ЙЬЬхЃЌЗХжУвЛЖЮЪБМфКѓЙ§ТЫЁЃ
ВНжш4ЃКМѕбЙеєСѓгаЛњЯрЃЌЪеМЏЯргІСѓЗжЁЃЃЈЪЕбщзАжУМћЯТЭМЃЉ

ЃЈ1ЃЉвЧЦїAЕФУћГЦЮЊ___________________ЃЌ1ЃЌ2ЃЖўТШввЭщЕФЕчзгЪНЮЊ__________ЃЛ
ЃЈ2ЃЉЪЕбщзАжУжаРфФ§ЙмЕФжївЊзїгУЪЧ________ЃЌНјЫЎПкЮЊ____ЃЈЬюЁАaЁБЛђЁАbЁБЃЉЃЛ
ЃЈ3ЃЉВНжш1ЗДгІЗНГЬЪНЮЊ____________________ЃЛЮЊЮќЪеЮВЦјзЖаЮЦПжаЕФШмвКгІЮЊ________ЃЌЗДгІЕФРызгЗНГЬЪНЮЊ________________ЃЛ
ЃЈ4ЃЉЫЎдЁМгШШЕФгХЕуЪЧ__________________________ЃЛ
ЃЈ5ЃЉВНжш2жагУ10%NaHCO3ШмвКЯДЕггаЛњЯрЃЌЪЧЮЊСЫГ§ШЅШмгкгаЛњЯрЕФ______(ЬюЛЏбЇЪН)ЃЛ
ЃЈ6ЃЉВНжш4жаВЩгУМѕбЙеєСѓММЪѕЃЌЪЧЮЊСЫЗРжЙ_______________ЁЃ
ВщПДД№АИКЭНтЮі>>
ПЦФПЃКИпжаЛЏбЇ РДдДЃК ЬтаЭЃК
ЁОЬтФПЁПГЃЮТЯТ10mLХЈЖШОљЮЊ0.1molЁЄL-1ЕФHXКЭHYСНжжвЛдЊЫсШмвКМгЫЎЯЁЪЭЙ§ГЬжаЕФpHЫцШмвКЬхЛ§БфЛЏЧњЯпШчЭМЫљЪОЁЃдђЯТСаЫЕЗЈВЛе§ШЗЕФЪЧ

A. ЕчРыГЃНЬЃКK(HX)<K(HY)
B. ХЈЖШОљЮЊ0.1molЁЄL-1ЕФHXКЭHYЕФЛьКЯШмвКжаЃКc(X-)+c(HX)=c(Y-)+ c(HY)
C. ХЈЖШОљЮЊ0.1molЁЄL-1ЕФNaXКЭNaYЕФЛьКЯШмвКжа:c(Na+)>c(Y-)>c(X-)>c(OH-)>c(H+)
D. aЕуЫЎЕФЕчРыЖШДѓгкbЕуЫЎЕФЕчРыЖШ
ВщПДД№АИКЭНтЮі>>
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com