
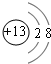
 ��MΪFԪ�أ���Ԫ�����ڱ��е�λ��Ϊ���ڶ����ڵڢ�A�壬
��MΪFԪ�أ���Ԫ�����ڱ��е�λ��Ϊ���ڶ����ڵڢ�A�壬 ���ڶ����ڵڢ�A�壻
���ڶ����ڵڢ�A�壻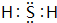 �����й��ۼ���Na��O��ԭ�Ӹ�����2��1�γɵĻ�����ΪNa2O2������ʽΪ
�����й��ۼ���Na��O��ԭ�Ӹ�����2��1�γɵĻ�����ΪNa2O2������ʽΪ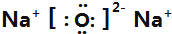 ���������Ӽ������ۼ���
���������Ӽ������ۼ���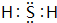 �����ۼ�����
�����ۼ�����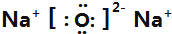 �����Ӽ������ۼ�����
�����Ӽ������ۼ�����


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����Ԫ�ص�����ͬλ�� |
| B����Ԫ�ص� ���ֺ��� |
| C����Ԫ�ص�����ͬ�������� |
| D����Ԫ�ص����ֲ�ͬ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
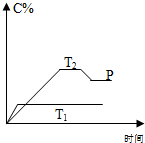 ��һ�������£����淴ӦA+B?mC�仯��ͼ��ʾ����֪�������ʾ�ڲ�ͬ�¶Ⱥ�ѹǿ��������C�ڻ�����е�����������PΪ��Ӧ��T2�¶�ʱ�ﵽƽ�����������ѹ�ı仯������ʣ�
��һ�������£����淴ӦA+B?mC�仯��ͼ��ʾ����֪�������ʾ�ڲ�ͬ�¶Ⱥ�ѹǿ��������C�ڻ�����е�����������PΪ��Ӧ��T2�¶�ʱ�ﵽƽ�����������ѹ�ı仯������ʣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� | ������ҩƷ | ���ӷ���ʽ |
| CaCl2�� CaCO3�� | ||
| FeSO4 ��CuSO4�� | ||
| Cu��Al�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
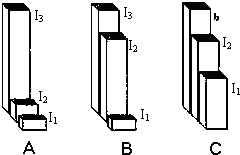
| Ԫ�� | �����Ϣ |
| Q | Q����̬�⻯����һ��10�����������ּ��� |
| R | R�ǵؿ��к�����ḻ��Ԫ�� |
| X | X��Y��ͬһ���ڣ�X����һ������ԭ�Ӱ뾶����Ԫ�� |
| Y | Y�Ĵ��������������������������� |
| Z | Z��һ�ָ���Ľ���Ԫ�أ�ԭ������Ϊ26 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com