
 反应类型取代反应
反应类型取代反应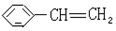 使溴水褪色的反应方程式
使溴水褪色的反应方程式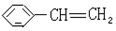 +Br2→
+Br2→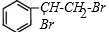 反应类型加成反应
反应类型加成反应 .
. 分析 (1)碳化钙(CaC2)与水反应生成氢氧化钙[Ca(OH)2]和乙炔;
(2)甲苯可以和浓硝酸发生取代反应生成2,4,6-三硝基甲苯;
(3)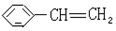 与溴发生加成反应;
与溴发生加成反应;
(4)1,3-丁二烯分子中含有两个碳碳双键,能够发生加聚反应.
解答 解:(1)碳化钙(CaC2)与水反应生成氢氧化钙[Ca(OH)2]和乙炔,配平即可,反应的化学方程式为:CaC2+2H2O=Ca(OH)2+C2H2↑,
故答案为:CaC2+2H2O=Ca(OH)2+C2H2↑;
(2)甲苯可以和浓硝酸之间发生取代反应生成2,4,6-三硝基甲苯,即TNT,化学反应方程式为: ,该反应为取代反应,
,该反应为取代反应,
故答案为: ;取代反应;
;取代反应;
(3)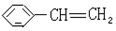 中含有碳碳双键,能够与溴单质发生加成反应,反应的化学方程式为:
中含有碳碳双键,能够与溴单质发生加成反应,反应的化学方程式为: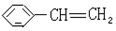 +Br2→
+Br2→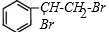 ,
,
故答案为: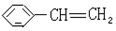 +Br2→
+Br2→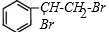 ;加成反应;
;加成反应;
(4)1,3-丁二烯含有2个碳碳双键,可发生加聚反应,反应的化学方程式为: ,
,
故答案为: .
.
点评 本题考查了化学方程式的书写,题目难度中等,明确发生反应实质为解答关键,注意掌握常见有机物组成、结构与性质,试题培养了学生的灵活应用能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 沉淀溶解后,将会生成深蓝色的配合离子[Cu(NH3)4]2+ | |
| B. | 反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 | |
| C. | 向反应后的溶液加入乙醇,溶液不会有变化,因为[Cu(NH3)4]2+不会与乙醇发生反应 | |
| D. | 在[Cu(NH3)4]2+离子中,Cu2+给出孤对电子,NH3提供空轨道 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验操作及现象 | 实验结论 | |
| A | 分别向2mL 0.1mol•L-1 CH3COOH溶液和2mL 0.1mol•L-1 H3BO3溶液中滴加等浓度的NaHCO3溶液,前者有气泡产生,后者无明显现象 | 酸性:CH3COOH>H2CO3>H3BO3 |
| B | 向2mL 0.1mol•L-1 NaOH溶液中滴加3滴0.1mol•L-1 MgCl2溶液,出现白色沉淀后,再滴加3滴0.1mol•L-1 FeCl3溶液,出现红褐色沉淀 | 溶解度:Mg(OH)2>Fe(OH)3 |
| C | 过氧化钠用于呼吸面具中作为氧气的来源 | 过氧化钠是强氧化剂,能氧化二氧化碳 |
| D | 向含有淀粉的FeI2溶液中滴加足量的氯水后变蓝 | 还原性:I->Fe2+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 回收废弃塑料制成燃油来替代汽油、柴油,可减轻环境污染和节约化石能源 | |
| B. | 火药是我国古代四大发明之一,配方为“一硫二硝三木炭”,其中的“硝”是指硝酸 | |
| C. | 高压钠灯发出的黄光射程远、透雾能力强,常用作路灯 | |
| D. | 黑色金属材料通常包括铁、铬、锰以及它们的合金,是应用非常广泛的金属材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在pH=1的溶液中:NH4+、K+、CO32-、Cl- | |
| B. | 有SO42-存在的溶液中:Na+、Mg2+、Ca2+、I- | |
| C. | 无色透明水溶液中:K+、Ba2+、I-、NO3- | |
| D. | 与铝粉反应有氢气生成的溶液中:Na+、Cl-、SO42-、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 化学键 | H-H | C-O | C=O | H-O | C-H |
| E/(kJ•mol-1) | 436 | 343 | 745 | 465 | 413 |
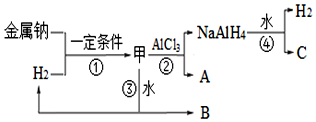
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
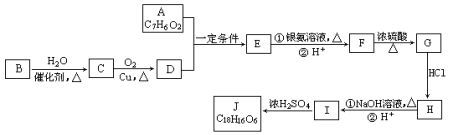
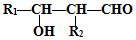
 ,G中含氧官能团的名称羟基、羧基.
,G中含氧官能团的名称羟基、羧基. $?_{△}^{浓H_{2}SO_{4}}$
$?_{△}^{浓H_{2}SO_{4}}$  +2H2O.
+2H2O.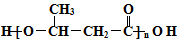 的路线图
的路线图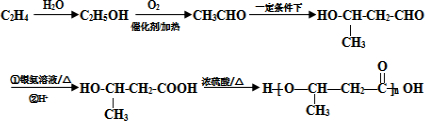 (提示:路线图的书写方法RCH=CH2
(提示:路线图的书写方法RCH=CH2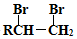 $→_{水/加热}^{NaOH}$
$→_{水/加热}^{NaOH}$ 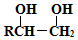 )
)查看答案和解析>>
科目:高中化学 来源: 题型:实验题
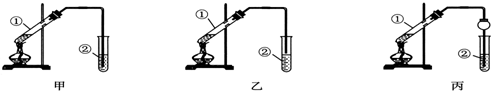
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com