
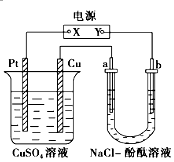
 如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色.下列说法正确的是( )
如图所示装置中,a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色.下列说法正确的是( )| A. | ①③ | B. | ②③ | C. | ①④ | D. | ②④ |
分析 a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色,则b电极上氢离子放电生成氢气,同时电极附近有氢氧根离子生成,则b是阴极、a是阳极,所以Y是负极、X是正极,Cu是阴极,电解时,硫酸铜溶液中阳极上氢氧根离子失电子、阴极上铜离子得电子,根据电解方程式确定溶液pH的变化据此分析解答.
解答 解:a、b都是惰性电极,通电一段时间后,b极附近溶液呈红色,则b电极上氢离子放电生成氢气,同时电极附近有氢氧根离子生成,则b是阴极、a是阳极,所以Y是负极、X是正极,Cu是阴极,Pt为阳极,
A.通过以上分析知,Y是负极、X是正极,故①正确;
B.通过以上分析知,b是阴极,a是阳极,故②错误;
C.电解过程中CuSO4溶液里,阳极上氢氧根离子失电子,阳极附近同时生成氢离子,所以CuSO4溶液的pH逐渐减小,故③正确;
D.通电电解NaCl溶液时,总反应为:2NaCl+2H2$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑,电解生成氢氧化钠,所以溶液的pH增大,故④错误;
故选A.
点评 本题考查电解池的工作原理知识,题目难度不大,注意根据电极现象判断电源的正负极为解答该题的关键.


科目:高中化学 来源: 题型:选择题
| A. | 浓硝酸光照逐渐变黄,说明光照分解生成的有色产物能溶于其中 | |
| B. | 中和滴定时,眼睛应注视滴定管中的液面下降 | |
| C. | 向饱和FeCl3溶液中滴加过量氨水,可制得Fe(OH)3胶体 | |
| D. | 配制一定物质的量浓度的溶液时,应将刚溶解后的溶液立即转移到容量瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al+O2$\frac{\underline{\;点燃\;}}{\;}$AlO2 | B. | C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 | ||
| C. | 2H2O═2H2+O2 | D. | Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 白色沉淀是BaSO4和BaSO3 | B. | FeCl3全部被还原为FeCl2 | ||
| C. | 白色沉淀是BaSO3 | D. | 溶液的酸性减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题

| A. | 装置②的待镀铁制品应与电源正极相连 | |
| B. | 装置①中阴极上析出红色固体 | |
| C. | 装置③闭合开关后,外电路电子由a极流向b极 | |
| D. | 装置④的X电极是外接电源的正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
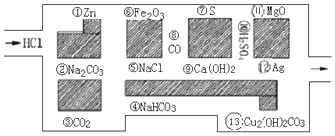

 (物质序号)
(物质序号)查看答案和解析>>
科目:高中化学 来源: 题型:填空题
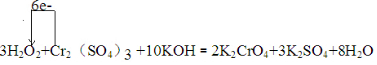 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com