
����Ŀ��������Ԫ�أ����ǵĽṹ�����ʵ���Ϣ���������
Ԫ�� | �ṹ�����ʵ���Ϣ |
A | �Ƕ������У���ϡ�������⣩ԭ�Ӱ뾶����Ԫ�� |
B | B��Aͬ���ڣ�������������ˮ��������� |
C | Ԫ�ص���̬�⻯�K������ˮ������������� |
D | �Ǻ�ˮ�г��⡢��Ԫ���⺬������Ԫ�أ��䵥�ʻ���Ҳ������ˮ���������г��õ�����ɱ���� |
E | ��̬ԭ�ӵ�M��ȫ������N��û�гɶԵ��ӣ�ֻ��һ��δ�ɶԵ��� |
����ݱ�����Ϣ��д��
��1��AԪ����Ԫ�����ڱ��е�λ�� ��
��2�����Ӱ뾶��BA������ڡ���С�ڡ�����
��3��Cԭ�ӵĵ����Ų�ͼ�� �� ��ԭ�Ӻ�������δ�ɶԵ��ӣ�������ߵĵ���Ϊ����ϵĵ��ӣ��������Σ�
��4��B������������Ӧ��ˮ������A������������Ӧ��ˮ���ﷴӦ�����ӷ���ʽΪ �� ��D����������ˮ����ˮ��Һ��Ӧ�Ļ�ѧ����ʽΪ ��
��5��EԪ�ػ�̬ԭ�ӵĵ����Ų�ʽΪ ��
���𰸡�
��1���������ڵڢ�A��
��2����
��3��![]() ��3��2p������
��3��2p������
��4��OH��+Al��OH��3�TAlO2��+2H2O��Al��OH��3+3HClO4�TAl��ClO4��3+3H2O��
��5��1s22s22p63s23p63d104s1��[Ar]3d104s1
���������⣺A�Ƕ������У���ϡ�������⣩ԭ�Ӱ뾶����Ԫ�أ���AΪNaԪ�أ�B��Aͬ���ڣ�������������ˮ��������ԣ���BΪAlԪ�أ�CԪ�ص���̬�⻯�K������ˮ�����������������CΪNԪ�أ�D�Ǻ�ˮ�г��⡢��Ԫ���⺬������Ԫ�أ��䵥�ʻ���Ҳ������ˮ���������г��õ�����ɱ��������DΪClԪ�أ�E�Ļ�̬ԭ�ӵ�M��ȫ������N��û�гɶԵ��ӣ�ֻ��һ��δ�ɶԵ��ӣ���E�ĵ����Ų�ʽӦΪ1s22s22p63s23p63d104s1 �� EΪCuԪ�أ���1��AΪNaԪ�أ�ԭ������Ϊ11��λ�����ڱ��е������ڵڢ�A�壬 ���Դ��ǣ��������ڵڢ�A�壻��2��BΪ��Ԫ�أ������Ӻ������ӵ��Ӳ�����ͬ���˵����Խ�����Ӱ뾶�뾶ԽС�����������Ӱ뾶С�������ӣ�
���Դ��ǣ�С�ڣ���3��CΪNԪ�أ���ԭ������Ϊ7��Nԭ�ӵĻ�̬ԭ�ӵĵ����Ų�ͼ�ǣ� ![]() ����ԭ�Ӻ�����3��δ�ɶԵ��ӣ�������ߵĵ���Ϊ2p����ϵĵ��ӣ����������壬
����ԭ�Ӻ�����3��δ�ɶԵ��ӣ�������ߵĵ���Ϊ2p����ϵĵ��ӣ����������壬
���Դ��ǣ� ![]() ��3��2p�����壻��4��BΪ��Ԫ�أ�DΪ��Ԫ�أ�B�����������Ϊ����������D������������ˮ����Ϊ�����ᣬ���߷�Ӧ�����ӷ���ʽΪ��OH��+Al��OH��3�TAlO2��+2H2O��D����������ˮ����ΪHClO4 �� HClO4������������Ӧ�Ļ�ѧ����ʽΪ��Al��OH��3+3HClO4�TAl��ClO4��3+3H2O��
��3��2p�����壻��4��BΪ��Ԫ�أ�DΪ��Ԫ�أ�B�����������Ϊ����������D������������ˮ����Ϊ�����ᣬ���߷�Ӧ�����ӷ���ʽΪ��OH��+Al��OH��3�TAlO2��+2H2O��D����������ˮ����ΪHClO4 �� HClO4������������Ӧ�Ļ�ѧ����ʽΪ��Al��OH��3+3HClO4�TAl��ClO4��3+3H2O��
���Դ��ǣ�OH��+Al��OH��3�TAlO2��+2H2O��Al��OH��3+3HClO4�TAl��ClO4��3+3H2O����5��EΪCuԪ�أ�ԭ������Ϊ29�����̬ԭ�ӵĵ����Ų�ʽΪ��1s22s22p63s23p63d104s1��[Ar]3d104s1 ��
���Դ��ǣ�1s22s22p63s23p63d104s1��[Ar]3d104s1 ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NaOH��MgCl2��AlCl3���ֹ�����ɵĻ������������ˮ����1.16g��ɫ�����������õ���Һ����μ���1molL��1 HCl��Һ������HCl��Һ����������ɳ�����������ϵ��ͼ��ʾ���Իش� 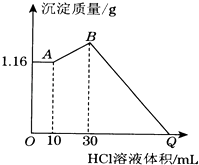
��1��д�����������ˮʱ������Ӧ�����ӷ���ʽ�� ��
��2��д��AB�η�Ӧ�����ӷ���ʽ �� B��ij�����Ļ�ѧʽΪ ��
��3��ԭ�������AlCl3�����ʵ�����mol��NaOH��������g��
��4��Q������HCl��Һ�����mL��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У���һ���������ܷ���ȡ����Ӧ�ͼӳɷ�Ӧ��������ʹ���Ը��������Һ��ɫ���ǣ� ��
A.����
B.����
C.��
D.��ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ֻ��һ���Լ��Ϳ��Լ���������Һ����������Һ��������Һ�������Լ��ǣ� ��
A.NaOH��Һ
B.����Cu��OH��2����Һ
C.ʯ����Һ
D.Na2CO3��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʽ�У�û����Է�������Ҳ����ȷ������ʽ���� ��������
A. CH3B. CHC. CH2D. CH2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���ѧ��Ҫ�о��л��������������ķ�Ӧ�����л������в����л�����ǣ� ��
A.CO2
B.C2H6
C.HCHO
D.CH3OH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͼ��A��B��C�ֱ��������л���Ľṹģ�ͣ�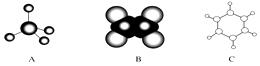
��ش��������⣺
��1��A��B����ģ�ͷֱ����л����ģ�ͺ�ģ�ͣ�
��2��C����ͬϵ��ķ���ʽ����ͨʽ����n��ʾ�����л���C���еĽṹ��������������ĸ����
a����̼̼˫����̼̼��������Ľṹb���ж���������ˮ���ܶȱ�ˮС
c������ʹ����KMnO4��Һ����ˮ��ɫd��һ������������������������Ӧ
��3�������������ɷ��ӵĽṹ�����ģ�ͨ������ͼ���ӽṹ�Ĺ۲����Ʋ��������ʣ�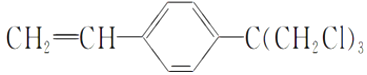
���л����к��еĹ������������ƣ����������ֿɷ�����Ӧ����Ӧ���Ӧ���ͣ���д�����л����γɵĸ߷��ӻ�����Ľṹ��ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڼ��Է����У����������ͬ��������ļ�ľ����Ϊż������ͨ����d��ʾ�����Է��ӵļ���ǿ��ͬż������������������ĵĵ�����q���йأ�һ����ż���أ��̣������������ӵ�ż���ض���Ϊż������ż���϶˵�ɵ����ij˻�������=dq���Իش��������⣺ �ΰ�ҩPt��NH3��2Cl2���������칹�壬�ػ�ɫ�ߦ̣�0������ɫ�ߦ�=0��
�����ڷ����ڻ��������칹��Ŀռ乹��ͼ��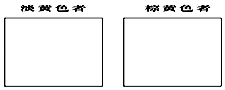
�ڸû�����������칹����ˮ���ܽ�Ƚϴ��������ػ�ɫ�ߡ�����ɫ�ߡ����������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Դ�Ŀ����������������ɳ�����չ����Ҫ���⣮������������Դ���ǣ� ��
A.����
B.ú̿
C.��Ȼ��
D.ʯ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com