
下列叙述不正确的是
A.工业上可用碳在高温下还原二氧化硅制取硅。
B.工业上可用氯气和石灰乳为原料制造漂白粉。
C.镁条不能在二氧化碳气体中燃烧。
D.将盛有氢氧化铁胶体的烧杯置于暗处,用一束光照射,从垂直于光线的方向可以观察到一条光亮的通路。
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源:2014-2015浙江省杭州市高一12月月考化学试卷(解析版) 题型:选择题
对相同状况下的12C18O和14N2两种气体,下列说法正确的是
A.若质量相等,则质子数相等 B.若质子数相等,则中子数相等
C.若分子数相等,则体积相等 D.若体积相等,则密度相等
查看答案和解析>>
科目:高中化学 来源:2014-2015浙江省杭州市高二12月月考化学试卷(解析版) 题型:选择题
下图为一原电池的结构示意图,下列说法中,错误的是

A.Cu电极为正电极
B.原电池工作时,电子从Zn电极流出
C.原电池工作时的总反应为:Zn+Cu2+=Zn2++Cu
D.盐桥(琼脂-饱和KCl溶液)中的K+移向ZnSO4溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省西安市高一上学期期末考试化学试卷(解析版) 题型:选择题
在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如图所示,由此确定,原溶液中含有的阳离子可能是
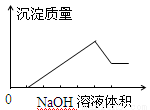
A.Mg2+、Al3+、Fe3+ B.H+、Mg2+、Al3+
C.H+、Ba2+、Al3+ D.Na+、Mg2+、Al3+
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省西安市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列有关试剂的保存方法,不正确的是
A.浓硝酸保存在无色玻璃试剂瓶中
B.少量的钠保存在煤油中
C.氢氧化钠溶液保存在带橡皮塞的玻璃试剂瓶中
D.新制的氯水通常保存在棕色玻璃试剂瓶中
查看答案和解析>>
科目:高中化学 来源:2014-2015安徽省淮南市高一上学期期末考试化学试卷(解析版) 题型:实验题
某化学兴趣小组的同学选定稀硫酸和氢氧化钡溶液做中和反应的实验。在烧杯中加入一定量的氢氧化钡溶液后滴入几滴酚酞试液,再向烧杯中加入一定量的稀硫酸。用玻璃棒充分搅拌后过滤,得白色沉淀和无色液体。
【提出问题】无色液体是什么物质?(不考虑指示剂)
【猜想】①小明:无色液体是水;
②小岩:无色液体是Ba(OH)2溶液;
③小丽认为无色液体可能是 溶液。
【实验探究】
(1)如果你是小组成员之一,你认为小明猜想的理由是 ;写出反应的离子方程式 。
(2)你认为小岩的猜想 (“正确”或“不正确”)。理由是 。
(3)填写小丽的猜想,并针对她的猜想,请你设计实验验证是否正确。
实验步骤 | 实验现象及结论 |
【拓展应用】
(4)中和反应在生产、生活中应用十分广泛,其中医疗上可以借助中和反应,来减轻胃酸过多病人的痛苦。根据你所学的知识判断下列物质适合用来中和胃酸的是 。
A.氢氧化钡 B.碳酸氢钠 C.氢氧化钠 D.氢氧化铝
查看答案和解析>>
科目:高中化学 来源:2014-2015安徽省淮南市高一上学期期末考试化学试卷(解析版) 题型:选择题
在某强酸性溶液中因发生氧化还原反应而不能大量共存的离子组是
A.K+、Fe2+、Cl-、NO3- B.Al3+、NH4+、OH- 、NO3--
C.Na+、H+、Cl-、CO32- D.Mg2+、Ba2+、SO42-、Cl-
查看答案和解析>>
科目:高中化学 来源:2014-2015安徽省淮南市高二上学期期末考试化学(文)试卷(解析版) 题型:填空题
下表是某食品包装上的说明,表中列出了部分配料。配料中,富含维生素的是 (填序号,下同),属于着色剂的是 ,属于防腐剂是 ,属于调味剂的是 。
品 名 | 浓苹果汁 |
配 料 | ① 浓缩苹果汁 ② 蔗糖 ③ 柠檬黄 ④ 山梨酸钾 |
果汁含量 | ≥80% |
生产日期 | 标于包装封口处 |
查看答案和解析>>
科目:高中化学 来源:2014-2015安徽省淮南市高二上学期期末考试化学(理)试卷(解析版) 题型:实验题
某研究小组进行Mg(OH)2沉淀溶解和生成的实验探究。
向2支盛有1 mL 1 mol/L的MgCl2溶液中各加入10滴2 mol/L NaOH,制得等量Mg(OH)2沉淀;然后分别向其中加入不同试剂,记录实验现象如下表:
实验序号 | 加入试剂 | 实验现象 |
Ⅰ | 4 mL 2 mol/L NH4Cl 溶液 | 沉淀溶解 |
Ⅱ | 4 mL蒸馏水 | 沉淀不溶解 |
(1)测得实验Ⅰ中所用NH4Cl溶液显酸性(pH约为4.5),用离子方程式解释其显酸性的原因 。
(2)同学们猜测实验Ⅰ中沉淀溶解的原因有两种:
猜想1:氢氧化镁电离出OH-离子,与氯化铵电离出来的铵根离子反应生成氨水.
猜想2: 。
(3)为验证猜想,又设计了以下实验
序号 | 实验内容 | 结 果 |
1 | 测定醋酸铵溶液的pH | pH约为7,溶液呈中性 |
2 | 取少量的相同质量的氢氧化镁分别盛放在试管中,分别向其中滴加醋酸铵溶液和氯化铵溶液 | 固体均溶解 |
①用醋酸铵溶液与氢氧化镁反应的原因是 。
②实验证明猜想正确的是 (填“1”或“2”)。
(4)实验Ⅱ观察到沉淀不溶解。该实验的目的是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com