
下列有关沉淀溶解平衡的说法中,正确的是( )
A.在AgCl的沉淀溶解平衡体系中,加入蒸馏水,Ksp(AgCl)增大
B.在CaCO3的沉淀溶解平衡体系中,加入稀盐酸,平衡不移动
C.可直接根据Ksp的数值大小比较难溶物在水中的溶解度大小
D.25 ℃时,Ksp(AgCl)>Ksp(AgI),向AgCl的悬浊液中加入KI固体,有黄色沉淀生成
科目:高中化学 来源:2014高考化学名师知识点精编 专题16硫及其化合物练习卷(解析版) 题型:选择题
下列有关实验现象和解释或结论都正确的选项是( )
选项实验操作现象解释或结论
A把SO2通入紫色石蕊试液中紫色褪去SO2具有漂白性
B把浓硫酸滴到pH试纸上试纸变红浓硫酸具有酸性
C将充满NO2的密闭玻璃球浸泡在热水中红棕色变浅反应2NO2
N2O4的ΔH<0
D向AgCl沉淀中滴加KI溶液白色沉淀
变为黄色溶度积:AgI比
AgCl更小
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题12钠、铝及其重要化合物练习卷(解析版) 题型:选择题
下列物质转化在给定条件下能实现的是( )
①Al2O3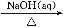 NaAlO2(aq)
NaAlO2(aq)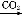 Al(OH)3
Al(OH)3
②S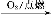 SO3
SO3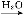 H2SO4
H2SO4
③饱和NaCl(aq)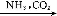 NaHCO3
NaHCO3 Na2CO3
Na2CO3
④Fe2O3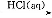 FeCl3(aq)
FeCl3(aq) 无水FeCl3
无水FeCl3
⑤MgCl2(aq) Mg(OH)2
Mg(OH)2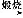 MgO
MgO
A.①③⑤B.①④⑤C.②③④D.②④⑤
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题11电化学练习卷(解析版) 题型:选择题
1 L K2SO4和CuSO4的混合溶液中c(S )=2.0 mol·L-1,用石墨电极电解此溶液,当通电一段时间后,两极均收集到22.4 L(标准状况)气体,则原溶液中c(K+)为( )
)=2.0 mol·L-1,用石墨电极电解此溶液,当通电一段时间后,两极均收集到22.4 L(标准状况)气体,则原溶液中c(K+)为( )
A.2.0 mol·L-1 B.1.5 mol·L-1
C.1.0 mol·L-1 D.0.5 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题10盐类水解与沉淀溶解平衡练习卷(解析版) 题型:选择题
一定温度下的难溶电解质AmBn在水溶液中达到沉淀溶解平衡时,其平衡常数Ksp=cm(An+)×cn(Bm-),称为难溶电解质的溶度积。已知下表数据:
物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
Ksp/25 ℃ | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | ≥3 |
对含等物质的量的CuSO4、FeSO4、Fe2(SO4)3的混合溶液的下列说法,正确的是( )
A.向该混合溶液中逐滴加入NaOH溶液,最先看到的是蓝色沉淀
B.该溶液中c(S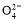 )∶[c(Cu2+)+c(Fe2+)+c(Fe3+)]>5∶4
)∶[c(Cu2+)+c(Fe2+)+c(Fe3+)]>5∶4
C.向该溶液中加入适量氯水,调节pH到4~5后过滤,可获得纯净的CuSO4溶液
D.向该溶液中加入适量氨水,调节pH到9.6后过滤,将所得沉淀灼烧,可得等物质的量的CuO、FeO、Fe2O3三种固体的混合物
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题10盐类水解与沉淀溶解平衡练习卷(解析版) 题型:选择题
蒸干FeCl3水溶液后再加强热,得到的固体物质主要是( )
A.FeCl3 B.FeCl3·6H2O C.Fe(OH)3 D.Fe2O3
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题9电化学原理练习卷B(解析版) 题型:选择题
图中X为电源,Y为浸透饱和食盐水和酚酞试液的滤纸,滤纸中央滴有一滴KMnO4溶液,通电后Y中央的紫红色色斑向d端扩散。下列判断正确的是( )
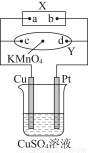
A.滤纸上c点附近会变红色
B.Cu电极质量减小,Pt电极质量增大
C.烧杯中溶液的pH先减小,后增大
D.烧杯溶液中SO42-向Cu电极定向移动
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题8电解质溶液练习卷B(解析版) 题型:填空题
常温下,向100 mL 0.01 mol·L-1 HA溶液中逐滴加入0.02 mol·L-1 MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。
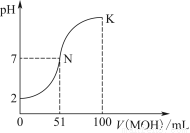
回答下列问题:
(1)由图中信息可知HA为________酸(填“强”或“弱”),理由是________________________________________________。
(2)常温下一定浓度的MA稀溶液的pH=a,则a________________________________________________________7
(填“>”“<”或“=”),用离子方程式表示其原因为_____________________________________________________
此时,溶液中由水电离出的c(OH-)=________。
(3)请写出K点所对应的溶液中离子浓度的大小关系:_________________________________________。
(4)K点对应的溶液中,c(M+)+c(MOH)________2c(A-)(填“>”“<”或“=”);若此时溶液中,pH=10,则c(M+)-c(OH-)=________mol·L-1。
查看答案和解析>>
科目:高中化学 来源:2014高考化学二轮复习限时集训 专题7化学反应速率和化学平衡练习卷A(解析版) 题型:选择题
一定条件下,向某密闭容器中加入一定量的N2和H2发生可逆反应:N2(g)+3H2(g) 2NH3(g) ΔH=-92.2 kJ·mol-1,测得0到10 s内,c(H2)减小了0.75 mol·L-1,下列说法正确的是( )
2NH3(g) ΔH=-92.2 kJ·mol-1,测得0到10 s内,c(H2)减小了0.75 mol·L-1,下列说法正确的是( )
A.10 s到15 s内c(NH3)增加量等于0.25 mol·L-1
B.10 s内氨气的平均反应速率为0.025 mol·L-1·s-1
C.达平衡后,分离出少量NH3,v正增大
D.该反应的逆反应的活化能不小于92.2 kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com