
下列说法正确的是 ( )
A.有些活泼金属如铝可用作热还原法的还原剂
B.用电解NaCl溶液的方法来冶炼金属钠
C.用加热分解氧化物的办法制取铜
D.使元素由化合态转化成游离态的过程就是还原的过程
科目:高中化学 来源:2017届天津一中高三上第一次月考化学试卷(解析版) 题型:选择题
短周期元素W、X、Y、Z的原子序数依次增大,其中W的阴离子的核外电子数与X、Y、Z原子的核外内层电子数相同.X的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气分馏方法来生产Y的单质,而Z不能形成双原子分子.根据以上叙述,下列说法中正确的是( )
A. W、X、Y、Z原子的核外最外层电子数的总和为22
B. 上述四种元素的原子半径大小为W<X<Y<Z
C. 有W与X组成的化合物的沸点总低于由W与Y组成的化合物的沸点
D. W与Y可形成既含极性共价键又含非极性共价键的化合物
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三小二调考化学试卷(解析版) 题型:实验题
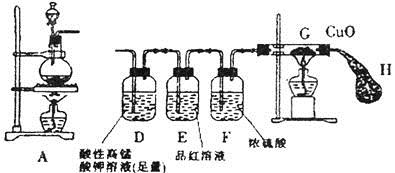
实验目的:研究铁与浓硫酸的反应
实验药品:铁钉、浓硫酸、酸性KMnO4溶液,品红溶液、CuO
实验步骤:
实验步骤 | 实验现象 | 结论 |
将铁钉(足量)加入烧瓶中,再向其中滴加含amol硫酸的浓硫酸溶液 | 未见明显现象 | 原因: |
点燃A、G处酒精灯 | 片刻后,烧瓶中溶液的颜色发生变化,并有气泡产生。 | 烧瓶中发生的所有反应 |
填完上述实验报告并回答下列问题:
(1)连接好装置后,盛放药品前,首先要进行 操作。
(2)为了测定产生的SO2的量,实验后向烧瓶中加足量的盐酸至无气泡产生,再加足量的BaCl2溶液至沉淀完全,为判断沉淀完全,应该进行的操作是: ,然后进行过滤、洗涤、干燥、称量。
(3)若(2)中所得沉淀的质量为mg,则反应产生的SO2在标准状况的体积为(列出计算式即可): L
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三小二调考化学试卷(解析版) 题型:选择题
工业上用固体硫酸亚铁制取颜料铁红,反应原理是:2FeSO4  Fe2O3+SO2↑+SO3↑。某学生欲检验该反应所产生的气态物质,他依次将气体通过盛有(I)BaCl2溶液、( II ) x 溶液、(III)NaOH 溶液的三个装置。则下列对该方案的评价中正确的是 ( )
Fe2O3+SO2↑+SO3↑。某学生欲检验该反应所产生的气态物质,他依次将气体通过盛有(I)BaCl2溶液、( II ) x 溶液、(III)NaOH 溶液的三个装置。则下列对该方案的评价中正确的是 ( )
A.(I)中会生成 BaSO3、BaSO4两种沉淀
B.可将(I)中的 BaCl2溶液改为 Ba ( NO3 )2溶液
C.(II)所盛 x应为品红溶液
D.( III)的作用是检验生成的SO2 气体
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三小二调考化学试卷(解析版) 题型:选择题
某溶液既能溶解Al(OH)3,又能溶解H2SiO3,在该溶液中可以大量共存的离子组是( )
A.Na+、SO42-、 、ClO- B.K+、Na+、HCO3-、NO3-
、ClO- B.K+、Na+、HCO3-、NO3-
C.H+、Mg2+、SO42-、NO3- D.Ag+、K+、NO3-、Na+
查看答案和解析>>
科目:高中化学 来源:2017届河北省等五校高三上学期第一次模拟化学试卷(解析版) 题型:实验题
工业上生产高氯酸时,还同时生产了一种常见的重要含氯消毒剂和漂白剂亚氯酸钠(NaClO2),其工艺流程如下:
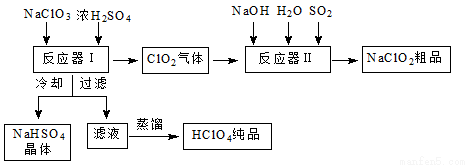
已知:①NaHSO4溶解度随温度的升高而增大,适当条件下可结晶析出。
②高氯酸是至今为止人们已知酸中的最强酸,沸点90 ℃。
请回答下列问题:
(1)反应器Ⅰ中发生反应的化学方程式为 ,冷却的目的是 ,能用蒸馏法分离出高氯酸的原因是___________________。
(2)反应器Ⅱ中发生反应的离子方程式为__________________。
(3)通入反应器Ⅱ中的SO2用H2O2代替同样能生成NaClO2,请简要说明双氧水在反应中能代替SO2的原因是_________________________。
(4)Ca(ClO)2、ClO2、NaClO2等含氯化合物都是常用的消毒剂和漂白剂,是因为它们都具有________________,请写出工业上用氯气和NaOH溶液生产消毒剂NaClO的离子方程式: 。
查看答案和解析>>
科目:高中化学 来源:2017届河北省等五校高三上学期第一次模拟化学试卷(解析版) 题型:选择题
一定温度下,在甲、乙、丙、丁四个恒容密闭容器中投入SO2(g)和O2(g),进行反应,
2SO2+O2 2SO3,其起始物质的量及SO2的平衡转化率如下表所示。下列判断中正确的是
2SO3,其起始物质的量及SO2的平衡转化率如下表所示。下列判断中正确的是
甲 | 乙 | 丙 | 丁 | ||
密闭容器体积/L | 2 | 2 | 2 | 1 | |
起始物质的量 | n(SO2)/mol | 0.40 | 0.80 | 0.80 | 0.40 |
n(O2)/mol | 0.24 | 0.24 | 0.48 | 0.24 | |
SO2的平衡转化率% | 80 |
|
|
| |
A.甲中反应的平衡常数小于乙
B.该温度下,该反应的平衡常数K为400
C.SO2的平衡转化率: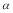 1>
1>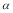 2 =
2 = 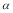 3
3
D.容器中SO3的物质的量浓度:丙=丁<甲
查看答案和解析>>
科目:高中化学 来源:2017届广东省高三上学期开学考试化学试卷(解析版) 题型:填空题
铁炭混合物(铁屑和活性炭的混合物)、纳米铁粉均可用于处理水中污染物。
(1)铁炭混合物在水溶液中可形成许多微电池。将含有Cr2O72-的酸性废水通过铁炭混合物,在微电池正极上Cr2O72-转化为Cr3+,其电极反应式为_____________。
(2)在相同条件下,测量总质量相同、铁的质量分数不同的铁炭混合物对水中Cu2+和Pb2+的去除率,结果如右图所示。
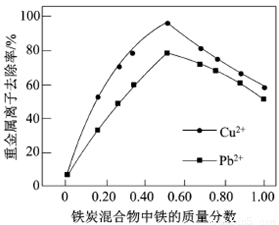
①当铁炭混合物中铁的质量分数为0时,也能去除水中少量的Cu2+和Pb2+,其原因是__________。
②当铁炭混合物中铁的质量分数大于50%时,随着铁的质量分数的增加,Cu2+和Pb2+的去除率不升反降,其主要原因是_____________。
(3)纳米铁粉可用于处理地下水中的污染物。
①一定条件下,向FeSO4溶液中滴加碱性NaBH4溶液,溶液中BH4-(B元素的化合价为+3)与Fe2+反应生成纳米铁粉、H2和B(OH)4-,其离子方程式为 。
②纳米铁粉与水中NO3-反应的离子方程式为 4Fe+ NO3-+10H+=4Fe2++NH4++3H2O,研究发现,若pH偏低将会导致NO3-的去除率下降,其原因是 。
③相同条件下,纳米铁粉去除不同水样中NO3-的速率有较大差异(见右图),产生该差异的可能原因是 。

查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高一上学期第一次月考化学试卷(解析版) 题型:选择题
有BaCl2和NaCl的混合溶液a L,将它均分成两份。一份滴加稀硫酸,使Ba2+离子完全沉淀;另一份滴加AgNO3溶液,使Cl-离子完全沉淀。反应中消耗x mol H2SO4、y mol AgNO3。据此得知原混合溶液中的Na+的物质的量浓度(单位:mol·L-1)为( )
A.(y-2x)/a B.(y-x)/a C.(2y-4x)/a D. (2y-2x)/a
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com