
【题目】下列物质中含有非极性键的分子是
A. CaF2 B. H2O2 C. CO2 D. NaOH
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:
【题目】苯是实验室常用的萃取剂,下列关于苯的说法错误的是( )
A. 常温下是液体B. 密度比水小
C. 能和液溴发生加成反应D. 能和硝酸发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常压下羰基化法精炼镍的原理为:Ni(s)+4CO(g)![]() Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
第一阶段:将粗镍与CO反应转化成气态Ni(CO)4;
第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。
下列判断正确的是
A. 增加c(CO),平衡向正向移动,反应的平衡常数增大
B. 第一阶段,在30℃和50℃两者之间选择反应温度,选50℃
C. 第二阶段,Ni(CO)4分解率较低
D. 该反应达到平衡时,v生成[Ni(CO)4]=4v生成(CO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某氯化钡样品23.1g中含有少量的氯化钠,某同学进行了如图所示的实验.请计算: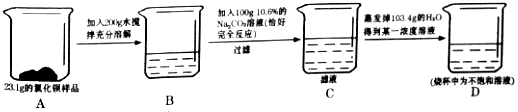
①过滤后得到沉淀多少克?
②原样品中氯化钡的质量分数?(计算结果精确到0.1%)
③求D烧杯中所得溶液的溶质质量分数是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,重水( D2O)的离子积常数为1.6×10-15,若用定义pH一样规定pD= -lgc(D+),则在该温度下,下列叙述正确的是
A. 纯净的重水中,c(D+) ·c(OD-)>1.0×10-14
B. l L溶解有0.01 mol DCl的重水溶液,其pD=2
C. 1 L溶解有0. 01 mol NaOD的重水溶液,其pD=12
D. 纯净的重水中,pD=7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一定体积的恒容密闭容器中进行可逆反应:X(g)+Y(g![]() Z(g) + W(s) △H>0,下列叙述正确的是
Z(g) + W(s) △H>0,下列叙述正确的是
A. 加入少量Z,逆反应速率增大
B. 当容器中气体压强不变时,反应达到平衡
C. 升高温度,平衡向逆反应方向移动
D. 平衡后,加入X,该反应的△H增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃、101 kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5 kJ/mol、285.8 kJ/mol、890.3 kJ/mol、2800 kJ/mol,则下列热化学方程式正确的是( )
A. C(s)+![]() O2(g)=CO(g) ΔH =-393.5 kJ/mol
O2(g)=CO(g) ΔH =-393.5 kJ/mol
B. 2H2(g)+O2(g)=2H2O(l) ΔH = +571.6 kJ/mol
C. CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH =-890.3 kJ/mol
D. C6H12O6(s) +6O2(g)=6CO2(g)+6H2O(l) ΔH =-2800 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案不能达到预期目的的是
A. 用钠、镁分别与水反应,可证明钠、镁的金属性强弱
B. 用氯化镁、氯化铝分别与过量浓氨水反应,可证明镁、铝的金属性强弱
C. 用铁、石墨与硫酸铜溶液组成原电池,可证明铁、铜的金属性强弱
D. 把氯气通入到硫化钠的水溶液中,看到淡黄色沉淀,可证明氯气、硫的非金属性强弱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com