
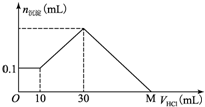
 某一固体物质可能由NaOH、AlCl3、MgCl2中的几种组成,取一定量该固体物质溶于水,有沉淀产生,在所得悬浊液中逐滴加入5mol/L的盐酸,如图表示沉淀量随盐酸加入量的变化关系,图中M点表示已加入的盐酸的体积,则M点的体积是( )
某一固体物质可能由NaOH、AlCl3、MgCl2中的几种组成,取一定量该固体物质溶于水,有沉淀产生,在所得悬浊液中逐滴加入5mol/L的盐酸,如图表示沉淀量随盐酸加入量的变化关系,图中M点表示已加入的盐酸的体积,则M点的体积是( )| A. | 70 mL | B. | 100 mL | C. | 120 mL | D. | 130 mL |
分析 逐滴加入1mol/L盐酸,由加入盐酸的体积和生成沉淀的质量关系图分析:
①0-10mL,随盐酸的体积增加,生成沉淀的质量不变,则盐酸和氢氧化钠中和,说明该过程产生的沉淀是Mg(OH)2,n[Mg(OH)2]=0.1mol,
NaOH、AlCl3、MgCl2组成的混合物,溶于足量水发生反应是:MgCl2+2NaOH=Mg(OH)2↓+2NaCl;AlCl3+4NaOH=NaAlO2+3NaCl+2H2O,NaOH有剩余,溶液是NaCl、NaAlO2和NaOH的混合液,该阶段发生反应是:NaOH+HCl=NaCl+H2O;
②10mL处,加入10ml盐酸刚好中和未反应的NaOH,溶液为NaCl、NaAlO2;
③10mL-30mL,随盐酸的体积增加,生成沉淀的质量增加,该阶段发生反应是:NaAlO2+HCl+H2O=Al(OH)3↓+NaCl,离子方程式是:H2O+AlO2-+H+=Al(OH)3↓
④30mL处,NaAlO2与盐酸恰好反应,需盐酸体积为:30mL-10mL=20mL,沉淀质量达到最大,溶液为NaCl溶液;
⑤30mL-M点,随盐酸的体积增加,沉淀的质量减少,发生反应是:Mg(OH)2+2HCl=MgCl2+2H2O;Al(OH)3+3HCl=AlCl3+3H2O;
⑥M点,Mg(OH)2和Al(OH)3完全反应,溶液为MgCl2、AlCl3和NaCl混合液,然后结合方程式、原子守恒求出各个物理量,最后根据V=$\frac{n}{c}$计算出M点盐酸的体积.
解答 解:向所得浊液中,逐滴加入1mol/L盐酸,由加入盐酸的体积和生成沉淀的质量关系图分析:
①0-10mL,随盐酸的体积增加,生成沉淀的质量不变,则盐酸和氢氧化钠中和,说明该过程产生的沉淀是Mg(OH)2,n[Mg(OH)2]=0.1mol,
NaOH、AlCl3、MgCl2组成的混合物,溶于足量水发生反应是:MgCl2+2NaOH=Mg(OH)2↓+2NaCl;AlCl3+4NaOH=NaAlO2+3NaCl+2H2O,NaOH有剩余,溶液是NaCl、NaAlO2和NaOH的混合液,该阶段发生反应是:NaOH+HCl=NaCl+H2O;
②10mL处,加入10ml盐酸刚好中和未反应的NaOH,溶液为NaCl、NaAlO2;
③10mL-30mL,随盐酸的体积增加,生成沉淀的质量增加,该阶段发生反应是:NaAlO2+HCl+H2O=Al(OH)3↓+NaCl,离子方程式是:H2O+AlO2-+H+=Al(OH)3↓
④30mL处,NaAlO2与盐酸恰好反应,需盐酸体积为:30mL-10mL=20mL,沉淀质量达到最大,溶液为NaCl溶液;
⑤30mL-M点,随盐酸的体积增加,沉淀的质量减少,发生反应是:Mg(OH)2+2HCl=MgCl2+2H2O;Al(OH)3+3HCl=AlCl3+3H2O;
⑥M点,Mg(OH)2和Al(OH)3完全反应,溶液为MgCl2、AlCl3和NaCl混合液,
选30mL处,计算NaOH的质量,此时溶液为NaCl溶液,溶液中Cl-来源于原混合物中的AlCl3、MgCl2和加入的30mLHCl,溶液中Na+来源于原混合物中的NaOH.
NaAlO2 +HCl+H2O=Al(OH)3↓+NaCl
0.1mol 0.02L×5mol/L
由Al原子守恒得原混合物中:n(AlCl3)=n(NaAlO2)=0.1mol
由Mg原子守恒得原混合物中:n(MgCl2)=n[Mg(OH)2]=0.1mol,
由Na+离子和Cl-离子守恒得,原混合物中:n(NaOH)=n(NaCl)=n(Cl-)=2n(MgCl2)+3n(AlCl3)+n(HCl)=0.1mol×2+0.1mol×3+0.03L×5mol/L=0.65mol
M点溶液为MgCl2、AlCl3和NaCl混合液,M点所加盐酸用于中和原混合物中的NaOH,此时所加盐酸物质的量:n(HCl)=n(NaOH)=0.65mol,
所以M点所表示盐酸的体积为:V=$\frac{0.65mol}{5mol/L}$=0.13L=130mL,
故选D.
点评 本题考查了有关方程式的计算,题目难度中等,注意把握各段发生的反应,对于图象分析题的解题规律:要明确每一段图象发生的化学反应、知道拐点代表的含义及溶液中溶质的成分,结合方程式对有关问题进行分析.


科目:高中化学 来源: 题型:解答题
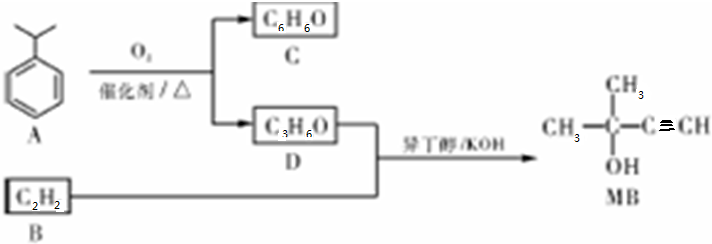
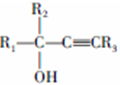
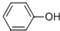 ,D的官能团名称为羰基.
,D的官能团名称为羰基.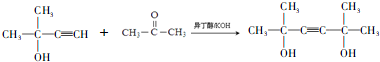 .
.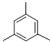 .
.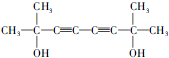 ,医药中间体,材料中间体)的合成路线
,医药中间体,材料中间体)的合成路线 或
或 .
.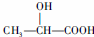 $→_{△}^{浓硫酸}$CH2=CH-COOH$→_{浓硫酸/△}^{CH_{3}OH}$CH-COOH3.
$→_{△}^{浓硫酸}$CH2=CH-COOH$→_{浓硫酸/△}^{CH_{3}OH}$CH-COOH3.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol氯化钾含有6.02×1023个KCl分子 | |
| B. | 6.02×1024个CO2分子的物质的量是1mol | |
| C. | 1molN2O4含有1molN2分子和4molO原子 | |
| D. | 1molH2分子和1molH2O分子所含的氢原子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
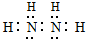 .
. HCO3-+OH-. 0.2mol/L该溶液中离子浓度由大到小的顺序为c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+).
HCO3-+OH-. 0.2mol/L该溶液中离子浓度由大到小的顺序为c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 治理拥堵,减少汽车尾气排放,大力发展清洁能源可以有效减少雾霾 | |
| B. | 铜的金属活动性比铝弱,可以用铜罐代替铝罐储运浓硝酸 | |
| C. | 光化学烟雾的形成和氮的氧化物有关,硫的氧化物是形成硫酸型酸雨的主要物质 | |
| D. | 硫化钠和亚硫酸钠的固体如果长期暴露在空气中容易变质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
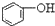 >HCO3-,下列化学方程式正确的是( )
>HCO3-,下列化学方程式正确的是( )| A. | 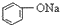 +H2O+CO2→ +H2O+CO2→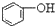 +Na2CO3 +Na2CO3 | B. | 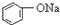 +NaHCO3→ +NaHCO3→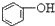 +Na2CO3 +Na2CO3 | ||
| C. | 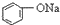 +H2O+CO2→ +H2O+CO2→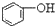 +NaHCO3 +NaHCO3 | D. | 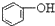 +NaHCO3→ +NaHCO3→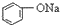 +H2O+CO2 +H2O+CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
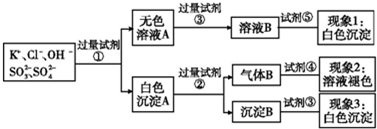
| A. | 试剂③是AgNO3溶液,试剂⑤是稀硝酸,现象1中白色沉淀是AgCl | |
| B. | 现象3中白色沉淀是BaSO4 | |
| C. | 产生现象2的离子方程式是:Br2+2H2O+SO2═4H++2Br-+SO42- | |
| D. | 试剂②是稀盐酸,试剂③是稀硝酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com