
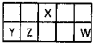
 I��������Ԫ��X��Y��Z��W��Ԫ�����ڱ������λ����ͼ��ʾ������Y������������������������ȣ���Ҫ��ش��������⣺
I��������Ԫ��X��Y��Z��W��Ԫ�����ڱ������λ����ͼ��ʾ������Y������������������������ȣ���Ҫ��ش��������⣺| �¶�/�� | 400 | 500 | 600 |
| ƽ�ⳣ��K | 9.94 | 9 | 1 |
 ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��| x?x |
| (1-x)?(1-x) |
| 0.75mol/L |
| 1mol/L |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��A��E��R��X��Y��Z����ǰ������Ԫ�أ�ԭ��������������̬Aԭ�ӵ�2p����������״̬��ԭ�ӵĵ�һ������E��A��R�ǵؿ��к�����ߵĽ���Ԫ�أ�Xԭ�Ӻ����M���������ԳɶԵ��ӣ�YΪ���ڱ�ǰ�������е縺����С��Ԫ�أ�Zԭ�Ӻ��������Ϊ24��
��A��E��R��X��Y��Z����ǰ������Ԫ�أ�ԭ��������������̬Aԭ�ӵ�2p����������״̬��ԭ�ӵĵ�һ������E��A��R�ǵؿ��к�����ߵĽ���Ԫ�أ�Xԭ�Ӻ����M���������ԳɶԵ��ӣ�YΪ���ڱ�ǰ�������е縺����С��Ԫ�أ�Zԭ�Ӻ��������Ϊ24���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

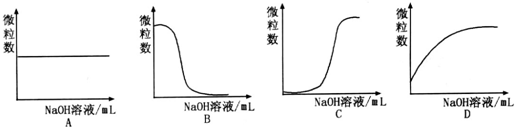
| A�����ܷ����ӳɷ�Ӧ���ܷ���ȡ����Ӧ |
| B������Һ�и÷��ӵ��ǻ����Ե����H+ |
| C���÷����к������ֹ����� |
| D���÷���������̼ԭ�ڲ�������ȫ��ƽ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��HCOOH |
| B��CH3COOH |
| C��CH3CH2OH |
| D��CH3CHO |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com