
研究NO2、SO2.CO等大气污染气体的处理具有重要意义。
(1) NO2可用水吸收,相应的化学反应方程式为__________ ___ 利用反应6 NO2+8NH3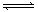 7N2+12H2O也可处理NO2.当转移1.2mol电子时,消耗的NO2,在标准状况下是_____________L。
7N2+12H2O也可处理NO2.当转移1.2mol电子时,消耗的NO2,在标准状况下是_____________L。
(2)已知:2SO2(g)+O2(g) 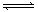 2SO3(g) △H=-196.6kJ·mol-1
2SO3(g) △H=-196.6kJ·mol-1
2NO(g)+O2(g)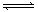 2NO2(g) △H=-113.0 kJ·mol -1
2NO2(g) △H=-113.0 kJ·mol -1
则反应NO2(g)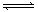 SO2(g)+ NO2的△H=________ kJ·mol -1 一定条件下,将NO2与SO2以体积比之于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是________
SO2(g)+ NO2的△H=________ kJ·mol -1 一定条件下,将NO2与SO2以体积比之于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是________
A.体系压强保持不变 B.混合气体颜色保持不变
C.SO2和NO的体积比保持不变 D.每消耗1molSO3的同时生成1mol NO2 测得
上述反应平衡是NO2与SO2体积比为1:6则平衡比常数k=________
| |
| |
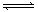 CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如右图所示。该反应△H___0(填“>”或“<”)实际生产条件控制在250℃、1.3ⅹ104 kPa左右,选择此压强的理由是_______。
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如右图所示。该反应△H___0(填“>”或“<”)实际生产条件控制在250℃、1.3ⅹ104 kPa左右,选择此压强的理由是_______。 
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
下列各组混合物无论以何种比例混合,只要总的物质的量一定,完全燃烧时消耗氧气的量是定值的是( )
A.CH2O、C2H4O2、C6H12O6
B.C6H6 、C5H12 、C7H6O2
C.CH2=CH2 、C2H5OH、HOCH2CH2COOH
D.H2 、CO CH3OH
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室有三种酸碱指示剂,其pH变色范围如下:甲基橙:3.1~4.4 石蕊:5.0~8.0酚酞: 8.2~10.0用0.1000 mol/L 的NaOH溶液滴定未知浓度的CH3COOH溶液,反应恰好完全时,下列说法中正确的是 ( )
A.溶液呈中性,可选用甲基橙或酚酞作指示剂
B.溶液呈中性,只能选用石蕊作指示剂
C.溶液呈碱性,可选用甲基橙或酚酞作指示剂
D.溶液呈碱性,只能选用酚酞作指示剂
查看答案和解析>>
科目:高中化学 来源: 题型:
t℃时,水的离子积为Kw,该温度下将a mol·L-1 一元酸HA与b mol·L-1 一元碱BOH等体积混合,混合液一定呈中性的是( )
A. 混合液的pH=7 B. 混合液中c(B+)=c(A-)
C. a=b D. 加入甲基橙显橙色
查看答案和解析>>
科目:高中化学 来源: 题型:
关于CCl2F2(二氟二氯甲烷,商品名称为氟利昂)的叙述,正确的是( )
A.是平面型分子 B.有两种结构
C.只有一种结构 D.空间构型为正四面体
查看答案和解析>>
科目:高中化学 来源: 题型:
可以用来鉴别甲烷和乙烯,还可以用来除去甲烷中乙烯的操作方法是( )
A.将混合气体通过盛有酸性高锰酸钾溶液的洗气瓶
B.将混合气体通过盛有足量溴水的洗气瓶
C.将混合气体通过盛有水的洗气瓶
D.将混合气体通过盛有澄清石灰水的洗气瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
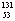 I是常规核裂变产物之一,可以通过测定大气或水中
I是常规核裂变产物之一,可以通过测定大气或水中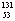 I的含量变化来监测核电站是否发生放射性物质泄漏。下列有关
I的含量变化来监测核电站是否发生放射性物质泄漏。下列有关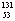 I的叙述中错误的是
I的叙述中错误的是
A.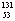 I的化学性质与
I的化学性质与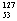 I相同
I相同
B.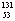 I的原子序数为53
I的原子序数为53
C.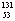 I的原子核外电子数为78
I的原子核外电子数为78
D.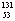 I的原子核内中子数多于质子数
I的原子核内中子数多于质子数
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化还原反应在生产、生活中具有广泛的用途,贯穿古今。
(1)水是人体的重要组成成分,是人体中含量最多的一种物质。而“四种基本反应类型与氧化还原反应的关系”也可用如图表达。
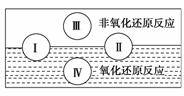
试写出有水参加的符合反应类型Ⅳ的一个化学方程式:
________________________________________________________________________其中水为________剂。
(2)氯化铵常用作焊接。如:在焊接铜器时用氯化铵除去铜器表面的氧化铜以便焊接,其反应为:
CuO+____NH4Cl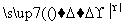
Cu+____CuCl2+N2↑+____H2O。
①配平此氧化还原反应方程式。
②该反应中,被氧化的元素是________ (填元素名称),氧化剂是________(填化学式)。
(3)磷酸钙与焦炭、石英砂混合,在电炉中加热到1 500 ℃生成白磷,反应为:
2Ca3(PO4)2+6SiO2===6CaSiO3+P4O10,
10C+P4O10===P4+10CO。
每生成1 mol P4时,就有________mol电子发生转移。
mol P4时,就有________mol电子发生转移。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com