
235 92 |
238 92 |
| A、中子数相同 |
| B、同种原子 |
| C、同位素 |
| D、同种核素 高温 |
235 92 |
238 92 |
235 92 |
238 92 |
235 92 |
238 92 |
235 92 |
238 92 |


科目:高中化学 来源: 题型:
| A、此时,反应混合物总物质的量为1mol |
| B、B反应的物质的量为0.1mol |
| C、A的平均反应速率为0.1mol/(L?min) |
| D、a值为1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分液时,分液漏斗中下层液体从下口放出后,换个洁净的烧杯,将上层液体从上口放入烧杯中 |
| B、蒸馏时,应使温度计水银球位于蒸馏烧瓶支管口处 |
| C、用酒精萃取溴水溶液中的溴 |
| D、称量时,将称量物体放在称量纸或烧杯中,置于托盘天平的左盘,砝码放在托盘天平的右盘 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe3+与I-在水溶液中不能大量共存 |
| B、氧化性:Cl2>Br2>I2 |
| C、将足量Br2加入到FeCl2溶液中,离子反应方程式为Br2+2Cl-═2Br-+Cl2 |
| D、将Cl2通入到FeBr2溶液中,Cl2应优先氧化Fe2+,再氧化Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铁跟稀H2SO4反应:2Fe+6H+=2Fe3++3H2↑ |
| B、碳酸钙溶于稀盐酸中:CaCO3+2H+=Ca2++H2O+CO2↑ |
| C、铜与硝酸银溶液反应:Cu+Ag+=Cu2++Ag |
| D、氢氧化钡溶液与稀H2SO4 反应:Ba2++SO42-=BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、H+、I-、MnO4- |
| B、Fe3+、Fe2+、SO42-、NO3- |
| C、Al3+、Na+、SO42-、CO32- |
| D、Fe3+、H+、SO42-、ClO- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol氢气完全燃烧吸热246.8 kJ |
| B、1mol水蒸气和1mol硫化氢的能量相差221.7 kJ |
| C、由①②知,水的热稳定性小于硫化氢 |
| D、若反应②中改用固态硫,放热将小于20.1 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
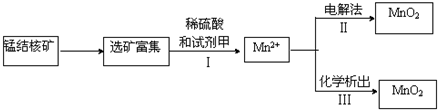
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com