
【题目】下列水溶液一定呈中性的是( )
A. 由非电解质溶于水得到的溶液
B. [H+]、[OH–]均为5.0×10–7mol·L–1的溶液
C. 等物质的量的强酸与强碱反应得到的溶液
D. 将pH=9的烧碱溶液稀释100倍所得到的溶液
科目:高中化学 来源: 题型:
【题目】关于甲烷和乙烯,下列说法正确的是
A. 甲烷能燃烧,乙烯不能 B. 甲烷和乙烯都能使溴水褪色
C. 甲烷和乙烯都能使酸性高锰酸钾溶液褪色 D. 甲烷和乙烯完全燃烧的产物都是CO2和H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各表述与示意图一致的是 ( )
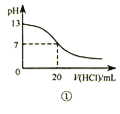


A. 图①表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1 NaOH溶液,溶液的pH随加入酸体积的变化
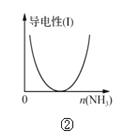
B. 图②表示CH3COOH溶液中通入NH3至过量的过程中溶液导电性的变化
C. 图③表示10 mL 0.01 mol·L-1 KMnO4 酸性溶液与过量的0.1 mol·L-1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化
D. 图中④表示分别稀释10 mL pH=2的盐酸和醋酸时溶液pH的变化,图中b>100
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合金是指两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的物质。分析下表中的数据,不能形成合金的是
Na | Cu | Al | Fe | |
熔点/℃ | 97.8 | 1083 | 660 | 1535 |
沸点/℃ | 883 | 2567 | 2467 | 2750 |
A.Cu和Al B.Fe和Cu C.Cu和Na D.Al和Na
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学在生产和日常生活中有着重要的应用。下列说法正确的是( )
A. 相同温度下,HCN溶液的导电性比同物质的量浓度的盐酸弱可以证明HCN是弱电解质
B. 强电解质溶液稀释后,溶液中各种离子浓度一定都减小
C. 盐酸滴定氨水,可以选择酚酞为指示剂
D. 醋酸铵的水溶液显中性,所以该溶液中水的电离程度与相同条件下氯化钠溶液中水的电离程度相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、某学生用0.2000 mol·L-1的标准NaOH溶液滴定未知浓度盐酸,其操作可分为如下几步:
①用蒸馏水洗涤碱式滴定管,并注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④量取20.00mL待测液注入用待测液润洗过的锥形瓶中,并加入3滴甲基橙溶液
⑤用标准液滴定至终点,记下滴定管液面读数

请回答:
(1)以上步骤有错误的是(填编号)________。
(2)用标准NaOH溶液滴定时,应将标准NaOH溶液注入______中。(从图中选填“甲”或“乙”)
(3)滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视_______________。
(4)判断到达滴定终点的现象是:锥形瓶中溶液_________________________。
(5)下列操作会引起实验结果偏大的是:______(填编号)
A.滴定终点时,有一滴标准液悬挂在滴定管尖嘴处
B.观察计数时,滴定前俯视,滴定后仰视
C.锥形瓶先用蒸馏水洗涤后,未用待测液润洗
D.用酸式滴定管量取液体时,释放液体前滴定管前端有气泡,之后消失
E.滴定时振荡锥形瓶有溶液飞溅出去
F.配制标准NaOH溶液定容时仰视观察刻度线
II、某课外活动小组为了测定某(CuCl22H2O)样品的纯度,设计了如下方案:
称取1.0 g样品溶解于适量水中,向其中加入含AgNO3 2.38 g的AgNO3溶液(溶液中除Cl-外,不含其他与Ag+反应生成沉淀的离子),Cl-即被全部沉淀。然后用含Fe3+的溶液作指示剂,用0.2 mol·L-1的KSCN标准溶液滴定剩余的AgNO3,使剩余的Ag+以AgSCN白色沉淀的形式析出,以测定样品的纯度。
请回答下列问题:
(6)判断滴定达到终点的现象是___________________。
(7)在终点到达之前的滴定过程中,两种沉淀表面会吸附部分Ag+,需不断剧烈摇动锥形瓶,否则会使n(Cl-)的测定结果_____________(选填“偏高”、“偏低”或“无影响”)。
(8)若到达滴定终点时,用去KSCN标准溶液20.00mL,求此样品的纯度__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水泥厂、发电厂、电石厂排放的气体加剧了温室效应,使全球气候变暖,加剧冰雪的消融。要想减缓这一现象发生,未来人类最理想的燃料是( )
A. 无烟煤 B. 石油 C. 天然气 D. 氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20.00mL0.1000 mol·L-1的醋酸溶液中逐滴加入0.1000 mol·L-1的NaOH溶液,pH随NaOH溶液体积的变化如图所示。下列说法不正确的是
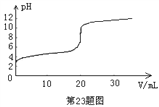
A. 在反应过程中,c(Na+)+ c(H+)= c(CH3COO-)+ c(OH-)
B. pH=5时,c(CH3COO-)> c(Na+)> c(H+)> c(OH-)
C. pH=6时,c(Na+)+ c(H+)-c(OH-)+ c(CH3COOH)=0.1000 mol·Lˉ1
D. pH=7时,消耗NaOH溶液的体积小于20.00mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关溶液组成描述合理的是( )
A.无色溶液中可能大量存在Al3+、NH4+、Cl-、Cu2+
B.中性溶液中可能大量存在Na+、K+、Cl-、SO42-
C.酸性溶液中可能大量存在Na+、ClO-、SO42-、I-
D.强碱性溶液中可能大量存在Na+、K+、Cl-、HCO3-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com