
| A. | 氧原子的得失 | B. | 化合价的升降 | ||
| C. | 分子中原子重新组合 | D. | 电子的转移 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | Na2O2、NH4Cl、NaCl、Na2SO4 | B. | FeO、AlCl3、Na2SiO3、硝酸 | ||
| C. | KHCO3、Ca(OH)2、MgCl2、硫酸 | D. | NaCO3、BaCl2、K2S、盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与铝粉反应放出氢气的无色溶液中:NO3-、Al3+、Na+、SO42- | |
| B. | 使红色石蕊试纸变蓝的溶液SO42-、HCO3-、Na+、K+ | |
| C. | 中性溶液:Fe3+、Al3+、NO3-、SO42- | |
| D. | 常温下,$\frac{C({H}^{+})}{C(O{H}^{-})}$=10-12的溶液:K+、AlO2-、CO32-、Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
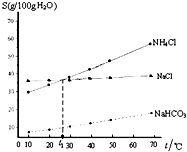
| A. | t1℃时,饱和NaCl和NH4Cl 溶液的物质的量浓度相同 | |
| B. | 相同温度下,NaHCO3在水中的溶解度比NaCl和NH4Cl小很多 | |
| C. | NH4Cl 溶解度随温度变化较大 | |
| D. | 工业上制纯碱可以向饱和的NaCl溶液中通入NH3和CO2,会有NaHCO3固体析出 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 根据较强酸可以制取较弱酸的规律,推出CO2通入NaClO溶液中能生成HClO | |
| B. | 金属钠可以通过电解熔融NaCl制得,推出金属铝可以通过电解熔融AlCl3制得 | |
| C. | 金属钠在纯氧中燃烧生成Na2O2,推出金属锂在纯氧中燃烧生成Li2O2 | |
| D. | CaCO3与稀硝酸反应生成CO2,推出CaSO3也能与稀硝酸反应生成SO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com