
【题目】合成氨工艺的一个重要工序是铜洗,其目的是用铜液[醋酸二氨合铜(I)、氨水]吸收在生产过程中产生的CO和CO2等气体。铜液吸收CO的反应是放热反应,其反应方程式为:Cu(NH3)2Ac+CO+NH3![]() [Cu(NH3)3CO]Ac
[Cu(NH3)3CO]Ac
完成下列填空:
(1)如果要提高上述反应的反应速率,可以采取的措施是_________。(选填编号)
a.减压b.增加NH3的浓度 c.升温 d.及时移走产物
(2)铜液中的氨可吸收二氧化碳,写出该反应的化学方程式。_____________________
(3)简述铜液吸收CO及铜液再生的操作步骤(注明吸收和再生的条件)__________________。
(4)铜液的组成元素中,短周期元素原子半径从大到小的排列顺序为___________。其中氮元素原子最外层电子排布的轨道表达式是_____________。通过比较_____________可判断氮、磷两种非金属元素的非金属性强弱。
(5)已知CS2与CO2分子结构相似,CS2的电子式是_______。醋酸二氨合铜中铜的配位数为______。
【答案】 bc 2NH3+CO2+H2O=(NH4)2CO3、(NH4)2CO3+CO2+H2O=2NH4HCO3 低温加压下吸收CO,然后将铜液洗涤转移至另一容器中,高温低压下释放CO,然后将铜洗液循环利用 C>N>O>H 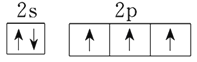 NH3和PH3的稳定性
NH3和PH3的稳定性 ![]() 2
2
【解析】(1)增大浓度、升高温度等,可增大反应速率,减压反应速率减小,减小生成物浓度,反应速率减小,故答案为:bc;
(2)氨气、水、二氧化碳可反应生成碳酸铵或碳酸氢铵,方程式为2NH3+CO2+H2O=(NH4)2CO3、(NH4)2CO3+CO2+H2O=2NH4HCO3,故答案为:2NH3+CO2+H2O=(NH4)2CO3、(NH4)2CO3+CO2+H2O=2NH4HCO3;
(3)正反应放热,铜液吸收CO,应使平衡向正向移动,则可在低温加压下吸收CO,然后将铜洗液转移至另一容器中,高温低压下释放CO,然后将铜洗液循环利用,故答案为:低温加压下吸收CO,然后将铜洗液转移至另一容器中,高温低压下释放CO,然后将铜洗液循环利用;
(4)铜液的组成元素中,短周期元素有H、C、N、O等元素,H原子半径最小,同周期元素从左到右原子半径逐渐减小,则原子半径C>N>O>H;氮元素原子最外层电子排布的轨道表示式是![]() ;比较非金属性强弱,可根据氢化物的稳定性强弱,故答案为:C>N>O>H;
;比较非金属性强弱,可根据氢化物的稳定性强弱,故答案为:C>N>O>H;![]() ;NH3和PH3的稳定性;
;NH3和PH3的稳定性;
(5)CS2的电子式类似于CO2,电子式为![]() ,根据醋酸二氨合铜的化学式Cu(NH3)2Ac,铜离子为中心原子,配体为NH3,配位数为2,故答案为:
,根据醋酸二氨合铜的化学式Cu(NH3)2Ac,铜离子为中心原子,配体为NH3,配位数为2,故答案为:![]() ;2。
;2。


 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:
【题目】在密闭容器中进行X2(g)+Y2(g)![]() 2Z(g)的反应,已知起始时其中X2、Y2、Z各物质浓度分别为0.1molL﹣1、0.3molL﹣1、0.2molL﹣1 , 反应达到平衡时,各物质浓度可能是( )
2Z(g)的反应,已知起始时其中X2、Y2、Z各物质浓度分别为0.1molL﹣1、0.3molL﹣1、0.2molL﹣1 , 反应达到平衡时,各物质浓度可能是( )
A.c(X)=0.2molL﹣1
B.c(Y2)=0.35molL﹣1
C.c(Y2)=0.2molL﹣1
D.c(Z)=0.4molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从薄荷油中得到一种烃A(C10H16),叫ɑ—非兰烃,与A相关反应如下:

(1)H的分子式为_________________。
(2)B所含官能团的名称为________、_________。
(3)含两个—COOCH3基团的C的同分异构体共有__________种(不考虑手性异构),其中核磁共振氢谱呈现2个吸收峰的异构体结构简式为_________。
(4)B→D,D→E的反应类型分别为____________、________________。
(5)G为含六元环的化合物,写出D→G化学反应方程式式:________________________。
(6)F在一定条件下发生聚合反应可得到一种高级吸水性树脂,该树脂名称为_______________。
(7)A的结构简式为______________,A与等物质的量的Br2进行加成反应的产物共有_____________种(不考虑立体异构)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图甲所示,纯电动公交车逐渐成为杭州街头常见的身影,磷酸铁锂电池是杭州市纯电动公交车所用的电池,现要从废旧磷酸铁锂电池中回收Fe、Al、Li等物质,采用图乙所示方法.已知:磷酸铁锂电池溶解在H2SO4中含有Fe3+、Al3+、Li+、SO ![]() 、PO
、PO ![]() 等离子及少量不溶物,滤液c中含有大量Li+离子,Li2CO3可溶于冷水,不溶于热水.下列说法不正确的是( )
等离子及少量不溶物,滤液c中含有大量Li+离子,Li2CO3可溶于冷水,不溶于热水.下列说法不正确的是( ) 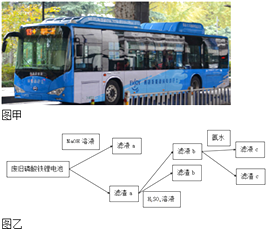
A.向滤液a中加入适量H2SO4溶液,可以得到白色沉淀
B.滤液b中加入氨水的目的是使Fe3+沉淀,滤渣c为红褐色
C.要将Li从溶液中析出,可在滤液c中加入足量Na2CO3溶液,加热浓缩,冷却结晶
D.图中的氨水可以用适量NaOH溶液代替
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X,Y,Z,W原子序数依次增大,m是W的单质,r是X的单质,s是Y的单质,n、p及q是这些元素组成的二元化合物;t由其中的三种元素组成,其水溶液呈碱性;p是淡黄色固体,q是一种耐高温材料,它们的关系如图所示.下列说法正确的是( ) 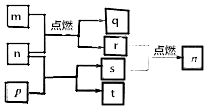
A.Y,Z,W的简单离子的电子层结构相同
B.原子半径:r(X)<r(Y)<r(Z)<r(W)
C.简单氢化物的稳定性:X>Y
D.Y与Z两种元素形成的化合物一定只含离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.将氯气通入水中:Cl2+H2O═2H++Cl﹣+ClO﹣
B.碳酸钙溶于醋酸:CaCO3+2H+═Ca2++CO2↑+H2O
C.铁与FeCl3溶液反应:Fe+Fe3+═2Fe2+
D.硫酸溶液与氯化钡溶液混合:Ba2++SO ![]() ═BaSO4↓
═BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质用途的说法错误的是
A. 液氨可用作制冷剂B. 二氧化硫可作食物和干果的防腐剂
C. Fe3O4可用作红色涂料D. 碳酸氢钠可用作面粉发酵
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4A(g )+3B(g)═2C(g)+D(g),经2min B的浓度减少0.6molL﹣1 , 对此反应速率的表示正确的是( ) ①用A表示的反应速率是0.4molL﹣1min﹣1
②分别用B、C、D表示的反应速率其比值为3:2:1
③在2min末的反应速率,用B表示是0.3molL﹣1min﹣1
④在这2min内B的瞬时速率始终相等.
A.①②
B.③
C.①
D.②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com