
| A、x值为2 |
| B、混合气体的密度变大 |
| C、L的转化率为80% |
| D、平衡时M的浓度为0.6mol/L |
| m |
| V |
| 消耗量 |
| 起始量 |
| 平衡时M的物质的量 |
| V |
| m |
| V |
| 1.6mol |
| 2mol |
| 0.6mol |
| 2L |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、Na2CO3溶液呈碱性:CO32-+2H2O?H2CO3+2OH- |
| B、氢氧化铁与稀硫酸反应:Fe(OH)3+3H+═Fe3++3H2O |
| C、FeCl3溶液与Na2S溶液混合:2Fe3++3S2-+6H2O═2Fe(OH)3↓+3H2S↑ |
| D、碳酸氢钠溶液与少量石灰水反应:HCO3-+Ca2++OH-═CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、葡萄糖不可能由纤维素制取 |
| B、葡萄糖在酒化酶作用下转化为乙醇和二氧化碳 |
| C、葡萄糖是人体能量的重要来源 |
| D、葡萄糖能与银氨溶液发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、离子半径:S2->Cl->Ca2+ |
| B、原子半径:Ca>S>Cl |
| C、酸性:HClO4<HBrO4<HIO4 |
| D、热稳定性:HCl>H2S>H2Se |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、单质①是最活泼的非金属单质 |
| B、单质②能使品红溶液褪色 |
| C、单质③在常温下是液态 |
| D、单质的氧化性强弱顺序是④>③>②>① |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、甲池中通甲烷的极是负极,溶液中Na+向Pt电极移动 | ||||
| B、C电极的电极反应为:O2+4e-+4H+═2H2O | ||||
C、乙池中的总反应为:Cu+H2SO4
| ||||
| D、反应过程中,甲、乙装置中溶液的pH都逐渐减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、33.6L(常温常压)氯气与2.7g铝充分反应,转移电子数为0.3NA |
| B、在标准状况下,22.4L CH2Cl2中含有的氢原子数为2NA |
| C、标准状况下,22.4L己烷含有的共价键数目为19NA |
| D、46gNO2气体在标准状况下的体积为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、苯酚是一种弱酸,滴加指示剂变色 |
B、苯酚在水溶液中能按下式电离: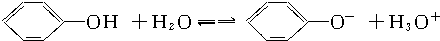 |
| C、苯酚钠在水溶液中几乎不能存在,会水解生成苯酚,所以苯酚钠溶液显碱性 |
| D、苯酚有腐蚀性,溅在皮肤上可用酒精冲洗 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com