
| A. | 化合反应都是氧化还原反应 | |
| B. | 复分解反应都不是氧化还原反应 | |
| C. | 在反应 2H2S+SO2=3S+2H2O中,还原剂是SO2 | |
| D. | 在一个氧化还原反应中,同一种反应物不可能既是氧化剂又是还原剂 |
分析 A.化合反应中可能没有元素的化合价变化;
B.复分解反应中一定不存在元素的化合价变化;
C.二氧化硫中S元素的化合价降低;
D.同一物质可能失去电子也得到电子.
解答 解:A.化合反应中可能没有元素的化合价变化,如二氧化硫与水反应生成亚硫酸为非氧化还原反应,故A错误;
B.复分解反应中一定不存在元素的化合价变化,则一定不是氧化还原反应,故B正确;
C.二氧化硫中S元素的化合价降低,则二氧化硫为氧化剂,故C错误;
D.同一物质可能失去电子也得到电子,如氯气与水的反应中,氯气既是氧化剂又是还原剂,故D错误;
故选B.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及与四种基本反应类型关系的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | H2Se的沸点高于H2S,可推测PH3的沸点高于NH3 | |
| B. | 17g羟基(-OH)所含有的电子数是9NA | |
| C. | σ键是镜面对称,而π键是轴对称 | |
| D. | 标准状况下,11.2 L三氯甲烷所含分子数为0.5 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | ①中Se是氧化产物,I2是还原产物 | |
| B. | SeO2、H2SO4(浓)、I2的氧化性由强到弱的顺序是 H2SO4(浓)>SeO2>I2 | |
| C. | 常温常压下,Se是固体,其最高价氧化物对应的水化物是H2SeO4 | |
| D. | 反应①中每有0.6 mol I2生成,转移电子数目为2.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5.4 g | B. | 3.6g | C. | 2.7 g | D. | 1.8 g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉属于天然有机高分子化合物 | B. | 遇I-能变蓝色 | ||
| C. | 淀粉不溶于冷水 | D. | 淀粉在人体内能水解生成葡萄糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在化合物中呈+2价 | B. | 单质能与水反应放出H2 | ||
| C. | 它的氢氧化物为强碱 | D. | 镭元素的金属性比钡元素的弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
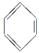 ,B是CH≡CH,C是CH2═CH2,D是CH3CH3.
,B是CH≡CH,C是CH2═CH2,D是CH3CH3. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com