
【题目】属于苯的同系物是( )
A. 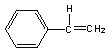 B.
B. 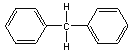
C. ![]() D.
D. 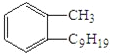
【答案】D
【解析】A. ![]() 为苯乙烯,分子中含有碳碳双键,与苯的结构不相似,该物质的分子式为C8H8,分子组成上与苯相差的不是CH2原子团,不符合同系物的定义,所以不是苯的同系物,故A不选;B.
为苯乙烯,分子中含有碳碳双键,与苯的结构不相似,该物质的分子式为C8H8,分子组成上与苯相差的不是CH2原子团,不符合同系物的定义,所以不是苯的同系物,故A不选;B. ![]() 分子中含有2个苯环,与苯的结构不相似,该物质的分子式为C13H12,分子组成上与苯相差的不是CH2原子团,不符合同系物的定义,所以不是苯的同系物,故B不选;C.
分子中含有2个苯环,与苯的结构不相似,该物质的分子式为C13H12,分子组成上与苯相差的不是CH2原子团,不符合同系物的定义,所以不是苯的同系物,故B不选;C. ![]() 含有2个苯环,与苯的结构不相似,该物质的分子式为C10H8,分子组成上与苯相差的不是CH2原子团,不符合同系物的定义,所以不是苯的同系物,故C不选;D.
含有2个苯环,与苯的结构不相似,该物质的分子式为C10H8,分子组成上与苯相差的不是CH2原子团,不符合同系物的定义,所以不是苯的同系物,故C不选;D. 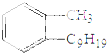 分子中只含有一个苯环,侧链均为饱和烃基,与苯的结构相似,该物质的分子式为C16H26,分子组成上与苯相差10个CH2原子团,符合同系物的定义,所以是苯的同系物,故D选;答案选D。
分子中只含有一个苯环,侧链均为饱和烃基,与苯的结构相似,该物质的分子式为C16H26,分子组成上与苯相差10个CH2原子团,符合同系物的定义,所以是苯的同系物,故D选;答案选D。


科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 在化学反应过程中,发生物质变化的同时不一定发生能量变化
B. 煤、石油、天然气均为化石能源,是非再生能源
C. 生成物的总焓大于反应物的总焓时,反应吸热,ΔH<0
D. ΔH的大小与热化学方程式的化学计量数无关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃,c(HCN)+c(CN-)=0.1mol/L的一组HCN和NaCN的混合溶液,溶液中c(HCN)、c(CN-)与pH的关系如图所示。下列有关离子浓度关系叙述正确的是
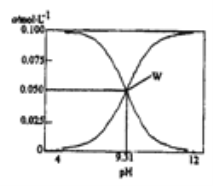
A. 将0.1mol/L的HCN溶液和0.1mol/LNaCN溶液等体积混合(忽略溶液体积变化): c(Na+)>c(HCN)>c(CN-)>c(OH-)>c(H+)
B. W点表示溶液中: c(Na+)+c(H+)=c(HCN)
C. pH=8的溶液中: c(Na+)+c(H+)+c(HCN)=0.1mol/L +c(OH-)
D. 将0.3mol/LHCN溶液和0.2mol/LNaOH溶液等体积混合(忽略溶液体积变化):c(CN-)+ 3c(OH-)=2c(HCN)+ 3c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂的工业废水中含有大量的FeSO4、较多的Cu2+和少量的Na+。为了减少污染并变废为宝,工厂计划从该工业废水中回收硫酸亚铁和金属铜。请根据流程图,回答下列问题。

(1)写出对应物质的化学式:①为________________________,②为_____________________________,A中含有的物质____________________。
(2)操作②的名称为__________________。
(3)母液中含有的离子主要有(填离子符号):__________________。
(4)操作③包括_______________________________和过滤,再经洗涤、干燥操作可以得到纯净的FeSO47H2O晶体,。
(5)在上述流程中,涉及到的离子方程式有______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛(22Ti)由于其特殊的性能被誉为“未来世纪的金属”。宝鸡因钛产业发达被称为中国钛谷,其钛产品产量占全国80%以上,占世界产量的20%以上。请回答下列问题:
(1)钛元素位于周期表中第4周期_____族,基态铁原子的价电子的电子排布式为______。
(2)钛元素在化合物中有+2、+3、+4等多种价态,试分析因显著的“压电效应“面被广泛应用于超声波发生装置中的偏钛酸钡(BaTiO3)中Ti的化合价为______。
(3)TiCl3是一种不稳定的氯化物,主要用作强还原制、烯烃聚合的催化剂以及偶氮染料分析等。
①溶波中的Ti3+易被FeCl3氧化,发生反应的离子方程式为________;若利用此反应原理,用已知标准浓度FeCl3溶液来滴定某含Ti3+的溶液时,可选用______溶液作指示剂判断滴定的终点。
②化学式为[Ti(H2O)6]Cl3的绿色晶体是TCl3的六水合物的一种晶型,该晶体中,与Ti3+T形成配位键的原子是_____(填元素符号),该原子的杂化类型为________;该晶体所含元素中,电负性最大的元素是_______(写出元素符号)。
③化学式为[Ti(H2O)5Cl]Cl2·H2O的绿色晶体是TiCl3的六水合物的另一种晶型,取1mol绿色晶体溶于水配成500mL溶液,加入足量AgNO3使Cl-完全沉淀,消耗AgNO3的物质的量为____mol。
④写出一种与H2O互为等电子体的阳离子______(填化学式)。
(4)TiO2的熔点为1800℃,TiCl4的熔点为-25℃,同为Ti的+4价化合物,熔点相差悬殊的原因是___________。
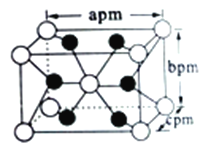
(5)自然界的钛主要以金红石( 主要成分为TiO2)的形式存在。TiO2 的晶胞属于四方晶系,其长方体结构如图所示,已知TiO2 的摩尔质量为M g/mol,阿伏加德罗常数的值为NA,根据图中所示数据列出该晶体密度的计算式ρ=_______g·cm-3(用NA表示阿伏伽德罗常数,用含M、a、b、c的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在同体积0.3 mol·L-1的H2SO4、HCl、CH3COOH溶液中,加入足量的Zn粉,下列说法中错误的是
A. 硫酸中放出氢气量最多 B. 醋酸中放出氢气速率最慢
C. 盐酸中放出的氢气量最多 D. 盐酸和醋酸中放出的氢气相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组以苯为主要原料,采用以下路线合成医药中间体G和可降解聚合物C。

已知:![]()
(1)写出X的结构式_______________________________。
(2)对于高分子化合物C的说法正确的是_____________(填序号)。
A.1molC能与2n mol NaOH反应
B.(C9H8O3)n即是高分子化合物C的化学式,也是链节的化学式
C.高分子化合物C是缩聚产物
D.酸性条件下降解时有气泡产生
(3)在一定条件下,E可以生成一种含有3个六元环的化合物(C18H16O4),请写出该反应的化学方程式___________________________________。
(4)写出符合要求的G的同分异构体(含有![]() 的有机物不能稳定存在)________。
的有机物不能稳定存在)________。
a.遇FeCl3溶液显紫色; b.能与Br2按1︰2发生加成反应; c.苯环上只有两种等效氢
(5)根据题目所给信息,以F和乙烯为原料,设计合成G的反应路线(用流程图表示,无机试剂任选)______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO+H2的混合气体又称“合成气”,在合成有机物中应用广泛。工业上常采用天然气与水蒸气或二氧化碳反应等方法来制取合成气。请回答下列问题:
(1)已知在一定条件下,0.25molCH4 与水蒸气完全反应制备“合成气”时吸收51.5kJ 的热量,请写出该反应的热化学方程式__________________________________________________。
(2)天然气与CO2反应也可制备合成气,在10L 密闭容器中通入lmolCH4 与1molCO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如下图1所示。

①1100℃、P2时气体混合后反应经过10min 至x 点的平衡,用CO 的变化量表示反应速率v(CO)=_____________;
②下列选项中能表示该反应已达到平衡状态的是____________;
A.v(H2)逆=3v (CO)正 B.密闭容器中混合气体的密度不变
C.密闭容器中总压强不变 D.c(CH4)=c(CO)
③由图1可知,压强P1_______P2 (填“大于”或“小于”);压强为P2时,在y点: v(正)____ v(逆) (填“大于”“小于”或“等于”)。求y点对应温度下的该反应的平衡常数K= __________。
(3)天然气中的H2S 杂质常用氨水吸收,产物为NH4HS。
已知: 25℃时,NH3·H2O 的电离常数K=1.8×10-5,H2S 的两步电离常数分别为Ka1=1.3×10-7,Ka2=7.1×10-15。求NH4HS溶液中离子浓度大小关系_____________________(由大到小)。
(4)合成气制甲醚的反应方程式为2CO(g)+4H2(g)![]() CH3OCH3(g)+H2O(g) △H= b kJ/mol。有研究者在催化剂、压强为5.0MPa 的条件下,由H2和CO 直接制备甲醚,结果如图2 所示。
CH3OCH3(g)+H2O(g) △H= b kJ/mol。有研究者在催化剂、压强为5.0MPa 的条件下,由H2和CO 直接制备甲醚,结果如图2 所示。

①290℃前,CO转化率和甲醚产率的变化趋势不一致的原因是___________________________;
②b______0 (填“ >”或“<”或“=”) ,理由是___________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com