
| A、分子式为C4H8有机物最多存在4个C-C单键 |
B、 和 和 均是芳香烃, 均是芳香烃, 既是芳香烃又是芳香化合物 既是芳香烃又是芳香化合物 |
C、 和 和 分子组成相差一个-CH2-,因此是同系物关系 分子组成相差一个-CH2-,因此是同系物关系 |
| D、分子式为C2H6O的红外光谱图上发现有C-H键和C-O键的振动吸收,由此可以初步推测有机物结构简式为C2H5-OH |
 含有氮、氧元素,不是烃,故B错误;
含有氮、氧元素,不是烃,故B错误;

 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:
| 物质 | Na2O | NaCl | AlF3 | AlCl3 |
| 熔点℃ | 920 | 801 | 1291 | 190 |
| 物质 | BCl3 | Al2O3 | CO2 | SiO2 |
| 熔点℃ | -107 | 2073 | -57 | 1723 |
| A、铝的化合物的晶体中不完全是离子晶体 |
| B、同族元素的氧化物可形成不同类型的晶体 |
| C、表中只有BCl3和干冰是分子晶体 |
| D、不同族元素的氧化物可形成相同类型的晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、KOH═K++OH- |
| B、CH3COOH═CH3COO-+H+ |
| C、NH3?H2O?NH4++OH- |
| D、Na2CO3═2Na++CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| O | 2- 7 |
| O | 2- 4 |
| A、向该溶液中加入过量浓NaOH溶液后,溶液呈橙红色 | ||||||
| B、该反应不是氧化还原反应 | ||||||
| C、向该溶液中滴加适量的浓硫酸,平衡向逆反应方向移动,再次达到平衡后,氢离子浓度比原溶液大 | ||||||
D、该反应的平衡常数表达式是K=
|
查看答案和解析>>
科目:高中化学 来源: 题型:
 的物质.下列叙述错误的是( )
的物质.下列叙述错误的是( )| A、能与Br2/CCl4溶液发生加成反应 |
| B、能与银氨溶液发生氧化(银镜)反应 |
| C、能与NaOH溶液发生中和反应 |
| D、能与冰醋酸发生酯化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 碳元素是构成物质种类最多的一种元素,许多物质与我们的生活息息相关.
碳元素是构成物质种类最多的一种元素,许多物质与我们的生活息息相关.查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
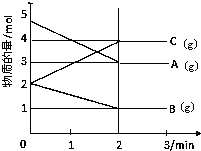 某可逆反应从0-2分钟进行过程中,在不同反应时间各物质的量的变化情况如图所示.
某可逆反应从0-2分钟进行过程中,在不同反应时间各物质的量的变化情况如图所示.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com