
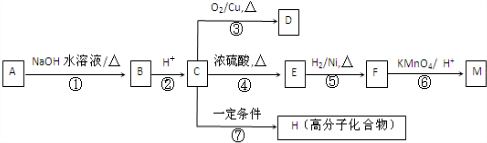
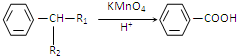 ��R1��R2������������ԭ�ӣ�
��R1��R2������������ԭ�ӣ�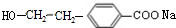 ��
��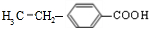 ��
�� ����Ӧ�ߵĻ�ѧ����ʽΪ
����Ӧ�ߵĻ�ѧ����ʽΪ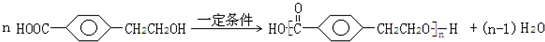 ��
������ A��F����������̼ԭ������ͬ���Ҿ����� NaHCO3��Һ��Ӧ��������-COOH��F�ķ���ʽΪC9H10O2���䲻���Ͷ�Ϊ$\frac{2��9+2-10}{2}$=5��F����������Ӧ����M��M��NaOH��Һ��Ӧ��IJ���䱽����һ�ȴ���ֻ��һ�֣�˵��F���б�����F��Ӧ�����һ��������Ȼ����ڶ�λ����FΪ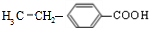 ��MΪ
��MΪ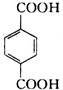 ����A��B��C��ת����֪��C�к���-COOH��C����������Ӧ����D��D�ܷ���������Ӧ�����F�Ľṹ��֪��CΪ
����A��B��C��ת����֪��C�к���-COOH��C����������Ӧ����D��D�ܷ���������Ӧ�����F�Ľṹ��֪��CΪ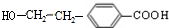 ����DΪ
����DΪ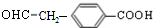 ��BΪ
��BΪ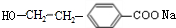 ��A����Է���������180〜260֮�䣬��A�б����ϵ��һ��в����������ǻ���ӦΪ±��ԭ�ӣ�A�ĽṹΪ
��A����Է���������180〜260֮�䣬��A�б����ϵ��һ��в����������ǻ���ӦΪ±��ԭ�ӣ�A�ĽṹΪ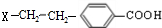 ��X���ԭ����������180-28-76-45=31��С��260-28-76=111��X����ΪCl��Br��C������ȥ��Ӧ����EΪ
��X���ԭ����������180-28-76-45=31��С��260-28-76=111��X����ΪCl��Br��C������ȥ��Ӧ����EΪ ��E�����������ӳɷ�Ӧ����F��C�������۷�Ӧ���ɸ߾���HΪ
��E�����������ӳɷ�Ӧ����F��C�������۷�Ӧ���ɸ߾���HΪ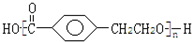 ��
��
��� �⣺A��F����������̼ԭ������ͬ���Ҿ����� NaHCO3��Һ��Ӧ��������-COOH��F�ķ���ʽΪC9H10O2���䲻���Ͷ�Ϊ$\frac{2��9+2-10}{2}$=5��F����������Ӧ����M��M��NaOH��Һ��Ӧ��IJ���䱽����һ�ȴ���ֻ��һ�֣�˵��F���б�����F��Ӧ�����һ��������Ȼ����ڶ�λ����FΪ ��MΪ
��MΪ ����A��B��C��ת����֪��C�к���-COOH��C����������Ӧ����D��D�ܷ���������Ӧ�����F�Ľṹ��֪��CΪ
����A��B��C��ת����֪��C�к���-COOH��C����������Ӧ����D��D�ܷ���������Ӧ�����F�Ľṹ��֪��CΪ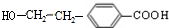 ����DΪ
����DΪ ��BΪ
��BΪ ��A����Է���������180〜260֮�䣬��A�б����ϵ��һ��в����������ǻ���ӦΪ±��ԭ�ӣ�A�ĽṹΪ
��A����Է���������180〜260֮�䣬��A�б����ϵ��һ��в����������ǻ���ӦΪ±��ԭ�ӣ�A�ĽṹΪ ��X���ԭ����������180-28-76-45=31��С��260-28-76=111��X����ΪCl��Br��C������ȥ��Ӧ����EΪ
��X���ԭ����������180-28-76-45=31��С��260-28-76=111��X����ΪCl��Br��C������ȥ��Ӧ����EΪ ��E�����������ӳɷ�Ӧ����F��C�������۷�Ӧ���ɸ߾���HΪ
��E�����������ӳɷ�Ӧ����F��C�������۷�Ӧ���ɸ߾���HΪ ��
��
��1��B��F�Ľṹ��ʽ�ֱ�Ϊ ��
�� ��
��
�ʴ�Ϊ�� ��
�� ��
��
��2����Ӧ������ȡ����Ӧ���������кͷ�Ӧ����Ӧ�����ڸ��ֽⷴӦ����Ӧ�ۢ�����������Ӧ����Ӧ��������ȥ��Ӧ����Ӧ�����ڼӳɷ�Ӧ����Ӧ���������۷�Ӧ��
�ʴ�Ϊ���ܣ�
��3��D����������Ӧ�Ļ�ѧ����ʽΪ�� ��
��
��Ӧ�ߵĻ�ѧ����ʽΪ��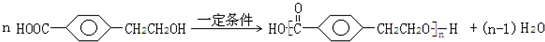 ��
��
�ʴ�Ϊ�� ��
��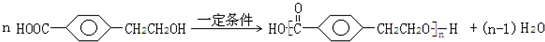 ��
��
��4����������ķ�����֪��X����ΪCl��Br��Ҫȷ��X�����ֹ����ŵ�ʵ�鲽�������Ϊ��ȡ��Ӧ�ٺ�Ļ��Һ�����������м���ϡHNO3�����ԣ��μ�AgNO3��Һ�������ɰ�ɫ��������A�к���ԭ�ӣ�������dz��ɫ��������A�к���ԭ�ӣ�
�ʴ�Ϊ��ȡ��Ӧ�ٺ�Ļ��Һ�����������м���ϡHNO3�����ԣ��μ�AgNO3��Һ�������ɰ�ɫ��������A�к���ԭ�ӣ�������dz��ɫ��������A�к���ԭ�ӣ�
��5����������������F�� ����ͬ���칹�壺a���ܷ���������Ӧ��˵�������д���ȩ����b������FeCl3��Һ������ɫ��Ӧ��˵�������д��ڷ��ǻ���c���˴Ź������������ĸ��壬������֮��Ϊ1��1��2��6��˵����4����ԭ�ӣ���������������F��������2������1�����ǻ���1��-CHO����2�������ڼ�λ����2���ֱ��ڶ�λ���ṹ��ʽΪ
����ͬ���칹�壺a���ܷ���������Ӧ��˵�������д���ȩ����b������FeCl3��Һ������ɫ��Ӧ��˵�������д��ڷ��ǻ���c���˴Ź������������ĸ��壬������֮��Ϊ1��1��2��6��˵����4����ԭ�ӣ���������������F��������2������1�����ǻ���1��-CHO����2�������ڼ�λ����2���ֱ��ڶ�λ���ṹ��ʽΪ ������F��ͬ���칹����2�֣�
������F��ͬ���칹����2�֣�
�ʴ�Ϊ��2��
���� ���⿼���л��ƶϡ��л���Ӧ���͡�ͬ���칹�塢��ѧ����ʽ����д�ȣ��ۺϷ���ȷ��F�Ľṹ�ǹؼ����ϺõĿ���ѧ������������������Ҫѧ���������չ����ŵ�������ת����ͬ���칹����ж����״��㣬�Ѷ��еȣ�


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���³�ѹ�£�28 g 14CO��N2�Ļ����������������Ϊ14NA | |
| B�� | �����£�100 mL 1 mol•L-1Na2CO3��Һ����������������0.1 NA | |
| C�� | ��NA��NH3��������1 Lˮ�еõ�1 mol•L-1�İ�ˮ | |
| D�� | 1 mol Cl2�ֱ�����������������������Һ��Ӧ��ת�Ƶ�������Ϊ2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
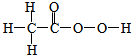 ��
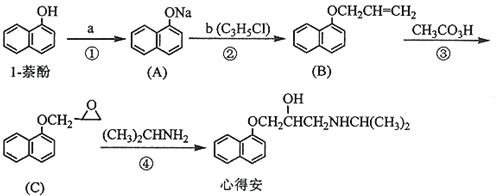
�� ����F����һ��������Ļ�ѧ����ʽΪ
����F����һ��������Ļ�ѧ����ʽΪ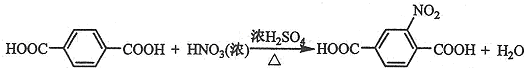 ���ò����������2-����-1��4-�������ᣮ
���ò����������2-����-1��4-�������ᣮ�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���

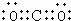 ��Y��������Ũ����
��Y��������Ũ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ���������� | ���� | |
| A | ���������ữ��FeCl2��Һ���Թ��м�������NaNO2��Һ���ڹܿڹ۲쵽����ɫ���� | ��Ҫԭ���ǣ�H++NO2-�THNO2�� 2HNO2�TNO��+NO2��+H2O |
| B | �������Һ�м���ϡH2SO4�����ȼ����ӣ���ȴ���ټ�������Cu��OH��2��Һ�����ȣ�û�к�ɫ�������ɣ� | ����û��ˮ��������� |
| C | ��˾ƥ�֣�����ˮ���ᣩ�м���������NaHCO3��Һ���д������ݲ����� | ��˾ƥ�ֳ���ˮ�� |
| D | ��1mL1.0mol•L-1AlCl3��Һ�еμ�2mL10% NH4F��Һ���ٵμ�1mL 3.0mol•L-1NH3•H2O��Һ���������ɣ� | Al3+������F-��ϳ�AlF63- |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ڷǽ�����Y��R����X��Y��ɻ�����ķе����X��R��ɵĻ����� | |
| B�� | ��Z��Y�γɵ��������ӻ��������������ӵĸ����ȷֱ�Ϊ1��2��1��1 | |
| C�� | ԭ�Ӱ뾶�ɴ�С���е��ǣ�Z��R��W��Y��X | |
| D�� | Y��Z��W����Ԫ����ɻ������ˮ��Һһ���Լ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����еIJ������մɡ�ˮ�������������β��ϣ�������ԭ�϶���Ҫʹ��ʯ��ʯ | |
| B�� | ����װ�����绯�˵�̺�����ϰ塢�����ҵȾ����ͷų���Ⱦ�����ļ�ȩ���� | |
| C�� | �����Ƽ��������ȡ���չ����о�Ӧ���������ܽ�ȵIJ��� | |
| D�� | ij��ˮ��Ʒ����һ��ʱ���pH��4.68��Ϊ4.28������Ϊ������CO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ZnΪ��صĸ��� | |
| B�� | ������ӦʽΪ2FeO42-+10H++6e-=Fe2O3+5H2O | |
| C�� | �õ�طŵ�����е������ҺŨ�Ȳ��� | |
| D�� | ��ع���ʱOH-��Ǩ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �о�CO2�����öԴٽ���̼���Ĺ���������Ҫ���壮
�о�CO2�����öԴٽ���̼���Ĺ���������Ҫ���壮 CO��NH2��2+H2O��ʱ��̼��=3���з�Ӧ����ƽ��ʱCO2��ת����Ϊ60%����NH3��ƽ��ת����Ϊ40%��
CO��NH2��2+H2O��ʱ��̼��=3���з�Ӧ����ƽ��ʱCO2��ת����Ϊ60%����NH3��ƽ��ת����Ϊ40%���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com