
 ĮņĖįÉś²śÖŠĀÆĘų×Ŗ»Æ·“Ó¦ĪŖ£ŗ2SO2£Øg£©+O2£Øg£©?2SO3£Øg£©£®ŃŠ¾æ·¢ĻÖ£¬SO3µÄĢå»ż·ÖŹż£ØSO3%£©ĖęĪĀ¶Č£ØT£©µÄ±ä»ÆČēĒśĻßIĖłŹ¾£®ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ£Ø””””£©
ĮņĖįÉś²śÖŠĀÆĘų×Ŗ»Æ·“Ó¦ĪŖ£ŗ2SO2£Øg£©+O2£Øg£©?2SO3£Øg£©£®ŃŠ¾æ·¢ĻÖ£¬SO3µÄĢå»ż·ÖŹż£ØSO3%£©ĖęĪĀ¶Č£ØT£©µÄ±ä»ÆČēĒśĻßIĖłŹ¾£®ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ£Ø””””£©| A£® | øĆ·“Ó¦ŌŚøßĪĀŹ±±ČµĶĪĀøüŅ××Ō·¢½ųŠŠ | |
| B£® | ĒśĻßIÉĻA”¢CĮ½µć·“Ó¦ĖŁĀŹµÄ¹ŲĻµŹĒ£ŗvA£¼vC | |
| C£® | T0Ź±øĆ·“Ó¦µÄĘ½ŗā³£ŹżĪŖ160 | |
| D£® | ŅŃÖŖV2O5µÄ“߻Ɗ§¹ū±ČFe2O3ŗĆ£¬ČōI±ķŹ¾ÓĆV2O5“߻ƼĮµÄĒśĻߣ¬ŌņIIŹĒFe2O3×÷“߻ƼĮµÄĒśĻß |
·ÖĪö ÓÉĶ¼æÉÖŖT0Ē°·“Ó¦Ī““ļĘ½ŗā£¬T0Ź±“¦ÓŚĘ½ŗāדĢ¬£¬T0ŗóÉżøßĪĀ¶ČĘ½ŗāĻņÄę·“Ó¦ŅĘ¶Æ£¬ŌņøĆ·“Ó¦ĪŖ·ÅČČ·“Ó¦£®
A£®øł¾Ż”÷H-T”÷S£¼0×Ō·¢½ųŠŠÅŠ¶Ļ£»
B£®ĪĀ¶ČŌ½øß·“Ó¦ĖŁĀŹŌ½æģ£»
C£®SO2ŗĶO2µÄĘšŹ¼ÅØ¶Č²»ÖŖµĄ£¬ĪŽ·Ø¼ĘĖć£»
D£®Ź¹ÓĆ“ß»Æ¼Į£¬¼Óæģ»Æѧ·“Ó¦ĖŁĀŹ£¬Ėõ¶Ģµ½“ļĘ½ŗāŹ±¼ä£¬µ«Ę½ŗā²»ŅĘ¶Æ£®
½ā“š ½ā£ŗÓÉĶ¼æÉÖŖT0Ē°·“Ó¦Ī““ļĘ½ŗā£¬T0Ź±“¦ÓŚĘ½ŗāדĢ¬£¬T0ŗóÉżøßĪĀ¶ČĘ½ŗāĻņÄę·“Ó¦ŅĘ¶Æ£¬ŌņøĆ·“Ó¦ĪŖ·ÅČČ·“Ó¦£®
A£®2SO2£Øg£©+O2£Øg£©?2SO3£Øg£©øĆ·“Ó¦ÖŠ”÷S£¼0£¬·ÅČČ·“Ó¦”÷H£¼0£¬”÷H-T”÷S£¼0×Ō·¢½ųŠŠ£¬ĖłŅŌµĶĪĀøüŅ××Ō·¢½ųŠŠ£¬¹ŹA“ķĪó£»
B£®CµćµÄĪĀ¶ČøßÓŚAµć£¬ĪĀ¶ČÉżøߣ¬»Æѧ·“Ó¦ĖŁĀŹ¼Óæģ£¬ĖłŅŌvA£¼vC£¬¹ŹBÕżČ·£»
C£®Ę½ŗā³£Źżk=$\frac{{c}^{2}£ØS{O}_{3}£©}{c£Ø{O}_{2}£©•{c}^{2}£ØS{O}_{2}£©}$£¬ÓÉÓŚSO2ŗĶO2µÄĘšŹ¼ÅØ¶Č²»ÖŖµĄ£¬ĪŽ·Ø¼ĘĖćĘ½ŗāŹ±ÅØ¶Č£¬ĖłŅŌĪŽ·Ø¼ĘĖćĘ½ŗā³£Źż£¬¹ŹC“ķĪó£»
D£®Ź¹ÓĆ“ß»Æ¼Į£¬¼Óæģ»Æѧ·“Ó¦ĖŁĀŹ£¬Ėõ¶Ģµ½“ļĘ½ŗāŹ±¼ä£¬µ«Ę½ŗā²»ŅĘ¶Æ£¬ÓĆV2O5“߻ƼĮÓėFe2O3×÷“߻ƼĮ£¬µ½“ļĘ½ŗāŹ±ČżŃõ»ÆĮņµÄŗ¬ĮæĻąĶ¬£¬¹ŹD“ķĪó£®
¹ŹŃ”£ŗB£®
µćĘĄ ±¾Ģāæ¼²éĶā½ēĢõ¼ž¶Ō»Æѧ·“Ó¦ĖŁĀŹŗĶ»ÆŃ§Ę½ŗāµÄÓ°Ļģ”¢·“Ó¦×Ō·¢ŠŌµÄÅŠ¶ĻµČ£¬ĢāÄæÄѶČÖŠµČ£®ŅŖ×¢Ņā“߻ƼĮÖ»øıä»Æѧ·“Ó¦ĖŁĀŹ£¬¶Ō»ÆŃ§Ę½ŗāĪŽÓ°Ļģ£¬²ąÖŲÓŚæ¼²éѧɜµÄ·ÖĪöÄÜĮ¦ŗĶÓ¦ÓĆÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | µ±b£¾2aŹ±£¬·¢ÉśµÄĄė×Ó·“Ó¦ĪŖ£ŗCO32-+2H+=H2O+CO2”ü | |
| B£® | µ±b£¼aŹ±£¬·¢ÉśµÄĄė×Ó·“Ó¦ĪŖ£ŗCO32-+H+=HCO3- | |
| C£® | µ±4a=3bŹ±£¬·¢ÉśµÄĄė×Ó·“Ó¦ĪŖ£ŗ3CO32-+4H+=2HCO3-+CO2”ü+H2O | |
| D£® | µ±a£¼b£¼2aŹ±£¬·“Ӧɜ³ÉµÄHCO3-ÓėCO2µÄĪļÖŹµÄĮæÖ®±ČĪŖ£Øb-a£©£ŗ£Ø2b-a£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
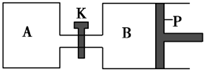 ČēĶ¼ĖłŹ¾µÄ×°ÖĆÖŠ·¢Éś·“Ó¦2A2£Øg£©+B2£Øg£©?2C£Øg£©”÷H=-a kJ•mol-1£Øa£¾0£©£¬ŅŃÖŖPŹĒæÉ×ŌÓÉ»¬¶ÆµÄ»īČū£®ŌŚĻąĶ¬ĪĀ¶ČŹ±¹Ų±ÕK£¬ĻņA”¢BČŻĘ÷ÖŠ·Ö±š³äČė2mol A2ŗĶ1mol B2£¬Į½ČŻĘ÷·Ö±šŌŚ500”ꏱ“ļĘ½ŗā£¬AÖŠCµÄÅضČĪŖw1 mol•L-1£¬·Å³öČČĮæb kJ£¬BÖŠCµÄÅضČĪŖw2 mol•L-1£¬·Å³öČČĮæc kJ£®ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ£Ø””””£©
ČēĶ¼ĖłŹ¾µÄ×°ÖĆÖŠ·¢Éś·“Ó¦2A2£Øg£©+B2£Øg£©?2C£Øg£©”÷H=-a kJ•mol-1£Øa£¾0£©£¬ŅŃÖŖPŹĒæÉ×ŌÓÉ»¬¶ÆµÄ»īČū£®ŌŚĻąĶ¬ĪĀ¶ČŹ±¹Ų±ÕK£¬ĻņA”¢BČŻĘ÷ÖŠ·Ö±š³äČė2mol A2ŗĶ1mol B2£¬Į½ČŻĘ÷·Ö±šŌŚ500”ꏱ“ļĘ½ŗā£¬AÖŠCµÄÅضČĪŖw1 mol•L-1£¬·Å³öČČĮæb kJ£¬BÖŠCµÄÅضČĪŖw2 mol•L-1£¬·Å³öČČĮæc kJ£®ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ£Ø””””£©| A£® | “Ė·“Ó¦µÄĘ½ŗā³£Źż±ķ“ļŹ½ĪŖK=$\frac{{c}^{2}£ØC£©}{{c}^{2}£Ø{A}_{2}£©•c£Ø{B}_{2}£©}$ | |
| B£® | CµÄÅØ¶Č“óŠ”±Č½ĻĪŖ£ŗw2£¼w1 | |
| C£® | a”¢b”¢cÓɓ󵽊”µÄ¹ŲĻµĪŖa£¾c£¾b | |
| D£® | Čō“ņæŖK£¬Ņ»¶ĪŹ±¼äŗóÖŲŠĀ“ļĘ½ŗā£¬ČŻĘ÷BµÄĢå»ż½«¼õŠ” |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
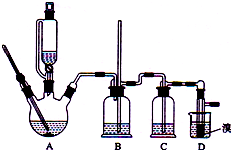 ŹµŃéŹŅÖʱø1£¬2-¶žäåŅŅĶéµÄ·“Ó¦ŌĄķČēĻĀ£ŗ
ŹµŃéŹŅÖʱø1£¬2-¶žäåŅŅĶéµÄ·“Ó¦ŌĄķČēĻĀ£ŗ| ŅŅ“¼ | 1£¬2-¶žäåŅŅĶé | ŅŅĆŃ | |
| דĢ¬ | ĪŽÉ«ŅŗĢå | ĪŽÉ«ŅŗĢå | ĪŽÉ«ŅŗĢå |
| ĆܶČ/g•cm-3 | 0.79 | 2.2 | 0.71 |
| ·Šµć/”ę | 78.5 | 132 | 34.6 |
| ČŪµć/”ę | Ņ»l30 | 9 | -1l6 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| 1.0MPa | 2.0MPa | 3.0MPa | |
| 810”ę | 54.0% | a | b |
| 915”ę | c | 75.0% | d |
| 1000”ę | e | f | 83.0% |
| A£® | 1øö | B£® | 2øö | C£® | 3øö | D£® | 4øö |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| Ź±¼ä/s | 20 | 40 | 60 | 80 | 100 |
| c£ØNO2 £©/£Ømol/L£© | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś¢Ū¢Ü | B£® | ¢Ś¢Ū¢Ü | C£® | ¢Ś¢Ū | D£® | ¢Ü |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com