
请从图中选用必要的装置进行电解饱和食盐水的实验,要求测定产生的氢气的体积(大于25 mL),并检验氯气的氧化性。
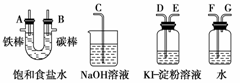
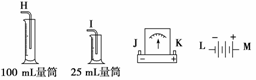
A极发生的电极反应式是_______________________________________________;
B极发生的电极反应式是_____________________________________________。
(2)电源、电流表与A、B两极的正确连接顺序为
L→( )→( )→( )→( )→M
(3)设计检测上述气体实验装置时,各接口的正确连接顺序为____接____、____接A,B接____、____接____。
(4)实验中,在盛有KI淀粉溶液的容器中发生反应的离子方程式为________________________________________________________________________。
答案 (1)2H++2e-—→H2↑
2Cl-—→Cl2↑+2e-
(2)A B J K (3)H F G D E C
(4)Cl2+2I-===2Cl-+I2
解析 对于解答实验题,首先要明确实验的目的是什么,然后围绕实验目的去设计实验步骤,连接实验仪器,回答实验问题。同时还要提高观察能力,若观察不仔细,会造成实验失败。本题融电解、实验、计算于一体。
(1)要达到电解食盐水的目的,则电解池中铁棒必须连接电源的负极而作阴极,碳棒则连接电源的正极而作阳极,反之,铁作阳极则Fe2+进入溶液,无法实现电解食盐水的目的。
(2)电源负极接电解池的铁棒,碳棒接电流计“-”端,“+”端接电源正极。
(3)电解池左边A导管口产生H2,右边B导管口产生Cl2,以电解池为中心,则有:H←F、G←A、B→D、E→C,相应装置的作用:
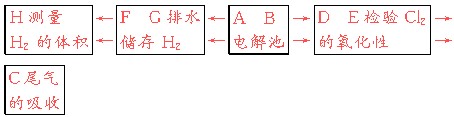
(4)Cl2+2I-===2Cl-+I2。


科目:高中化学 来源: 题型:
设NA 为阿伏加德罗常数,下列有关说法正确的是]( )
A.0.5 mol苯分子中含有C=C双键数为1.5 NA
B.1 mol甲基(—CH3)所含的电子总数为10 NA
C.标准状况下,1L甲醇完全燃烧后生成的CO2分子数目约为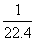 NA
NA
D.2.8 g乙烯和丙烯的混合气体中所含碳原子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
在下图装置中,通电后可观察到Cu极溶解,则下列说法中不正确的是( )
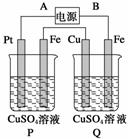
A.直流电源中,A是正极
B.两池内CuSO4溶液浓度均不改变
C.两铁极上最初析出物相同
D.P池内溶液的质量逐渐减小
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法或表示方法正确的是( )
A.等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出的能量多
B.由H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1可知,若将含1 mol CH3COOH的稀溶液与含1 mol NaOH的稀溶液混合,放出的热量小于57.3 kJ
C.由C(石墨)===C(金刚石) ΔH=1.9 kJ·mol-1可知,金刚石比石墨稳定
D.在100 kPa时,1 g H2完全燃烧生成液态水,放出285.8 kJ热量,则H2燃烧的热化学方程式表示为:2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
用如图所示的装置进行实验,反应一段时间后断开K,向右侧烧杯中加入0.1 mol
CuO后CuSO4溶液恰好恢复到反应前的浓度和pH。下列说法中不正确的是( )
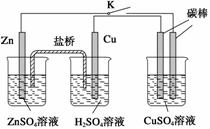
A.铜棒为正极,其电极反应式为2H++2e-—→H2↑
B.烧杯右侧碳棒为阴极,其电极表面有红色物质析出
C.反应中消耗锌的质量为13 g
D.导线中通过的电子的物质的量为0.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
为了实现铜质奖牌镀银,下列说法正确的是( )
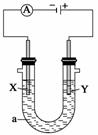
A.X为银,Y为Cu,a为AgNO3溶液
B.X的电极反应式Ag++e-—→Ag
C.电镀液的浓度减小
D.电解过程中溶液的pH值下降
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示,A为直流电源,B为浸透饱和氯化钠溶液和酚酞溶液的滤纸,C为电镀槽,接通电路后,发现B上的c点显红色,请填空:
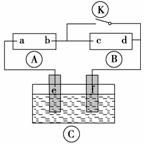
(1)电源A上的a为_________________________________________________极。
(2)滤纸B上发生的总化学反应方程式为___________________________________。
(3)欲在电镀槽中实现铁上镀锌,接通K点,使c、d两点短路,则电极e上发生的反应为
________________________________________________________________________,
电极f上发生的反应为______________________________________________,
槽中盛放的电镀液可以是__________或__________(只要求填两种电解质溶液)。
查看答案和解析>>
科目:高中化学 来源: 题型:
随着现代工业的发展,能源问题已经越来越引起人们的重视。科 学家们预言,未来最理想的燃料是绿色植物,即将植物的秸秆(主要成分是纤维素)用适当的催化剂作用水解成葡萄糖,再将葡萄糖转化成乙醇,用作燃料。
学家们预言,未来最理想的燃料是绿色植物,即将植物的秸秆(主要成分是纤维素)用适当的催化剂作用水解成葡萄糖,再将葡萄糖转化成乙醇,用作燃料。
(1)写出将绿色植物的秸秆转化为乙醇的化学方程式
______________________ _____________________________。
_____________________________。
(2)已知:C2H5OH(l)+3O2(g)―→2CO2(g)+3H2O(l)
ΔH=-1 367 kJ·mol-1
CH4(g)+2O2(g)―→CO2(g)+2H2O(l)
ΔH=-890 kJ·mol-1
若某种植物的秸杆含纤维素约50%,由植物秸杆经过一系列转化得到乙醇原料的总利用率为80%,则用1 000 g秸杆为原料制得的乙醇燃料燃烧所产生的热量与 L甲烷完全燃烧产生的热量相当(标准状况下)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com