

分析 乙烯与氯气发生加成反应生成A,A为ClCH2CH2Cl,在氢氧化钠水溶液、加入条件下发生水解反应生成乙二醇.乙烯与水发生加成反应生成乙醇,乙醇氧化生成B,B氧化生成乙酸,故B为CH3CHO.乙酸与乙二醇发生酯化反应生成C,C可能为CH3COOCH2CH2OH或CH3COOCH2CH2OOCCH3,以此解答该题.
解答 解:(1)乙醇、乙酸中含氧官能团的名称分别为羟基、羧基,故答案为:羟基;羧基;
(2)反应①为乙烯在催化剂条件下与水发生加成反应生成乙醇;反应⑥为乙酸与乙二醇的酯化反应,也为取代反应,
故答案为:加成反应;酯化反应(或取代反应);
(3)反应④为乙醇催化氧化生成乙醛,反应方程式为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O,
故答案为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;
(4)乙醇在浓硫酸的催化作用下发生分子内脱水制取乙烯,乙醇发生了消去反应,反应方程式为:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O,
故答案为:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O;
(5)HOCH2CH2OH与CH3COOH按物质的量比1:2反应,化学方程式为:HOCH2CH2OH+2CH3COOH$→_{△}^{浓硫酸}$CH3COOCH2CH2OOCCH3+2H2O,
故答案为:HOCH2CH2OH+2CH3COOH$→_{△}^{浓硫酸}$CH3COOCH2CH2OOCCH3+2H2O.
点评 本题考查有机推断题,为高考常见题型,题目难度中等,涉及官能团名称、物质的结构简式的书写、化学反应的类型判断、化学方程式的书写等知识,熟悉各种物质的结构和性质是解题关键,试题知识点较多,充分考查了学生的分析、理解能力及灵活应用基础知识的能力.


 一线名师权威作业本系列答案
一线名师权威作业本系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向饱和碳酸钠溶液中通入二氧化碳:CO32-+CO2+H2O═2HCO3- | |
| B. | 二氧化锰与浓盐酸反应:MnO2+4HCl(浓)═Mn2++2Cl2↑+2H2O | |
| C. | 亚硫酸氢钠溶液中加过量澄清石灰水:2HSO3-+Ca2++2OH-═CaSO3↓+2H2O+SO32- | |
| D. | 金属钠与硫酸铜溶液反应:2Na+2H2O+Cu2+$\frac{\underline{\;\;△\;\;}}{\;}$2Na++Cu(OH)2↓+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 尿素[CO(NH2)2]是首个由无机物人工合成的有机物.
尿素[CO(NH2)2]是首个由无机物人工合成的有机物.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

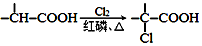

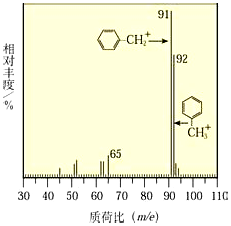
 +NaOH $→_{△}^{水}$
+NaOH $→_{△}^{水}$ +NaCl.
+NaCl. .
. 为原料制取
为原料制取  的合成路线图.合成路线图示例如下:
的合成路线图.合成路线图示例如下:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 +CH2═CH-M$→_{碱}^{Pb}$
+CH2═CH-M$→_{碱}^{Pb}$ =CH-M+HX(X为卤原子,M为烃基或含酯基的取代基等),由有机物A合成G(香豆素)的步骤如下:
=CH-M+HX(X为卤原子,M为烃基或含酯基的取代基等),由有机物A合成G(香豆素)的步骤如下: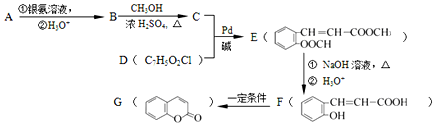
 .
. 中任意2种.
中任意2种. 的路线流程图:
的路线流程图: .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L1mol•L-1KClO3溶液中含有的氯离子数目为NA | |
| B. | 22.4LH2含有的分子数目为NA | |
| C. | 等质量的C2H2与C6H6含有的原子总数相等 | |
| D. | 1molZn变为Zn2+时失去的电子数目为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com