
【题目】在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g) + Y(g)![]() 2Z(g) △H<0,一段时间后达到平衡,反应过程中测定的数据如下表:
2Z(g) △H<0,一段时间后达到平衡,反应过程中测定的数据如下表:
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是
A. 0~2min的平均速率ν(Z) = 2.0×10-3mol·L-1·min-1
B. 其他条件不变,降低温度,反应达到新平衡前ν(逆)>ν(正)
C. 该温度下此反应的平衡常数K =1.44
D. 其他条件不变,再充入0.2molZ,平衡时X的体积分数增大
【答案】C
【解析】试题分析:A、由表中数据可求得前2min内生成Z为0.08mol,故v(Z)=0.08mol/(10L×2min)=4×103molL1min1,A错误;B、该反应的正反应是放热反应,降低温度平衡正向移动,反应达到新平衡前v(逆)<v(正),B错误;C、由表中数据可知7min时,反应到达平衡,Y的物质的量为0.10mol,此时X的物质的量也为0.10mol,Z的物质的量也为0.12mol,X、Y、Z的物质的量浓度分别为:0.01molL-1、0.01molL-1、0.012molL-1,故平衡常数K=c2(Z)/c(X)c(Y)=0.0122/0.01×0.01=1.44,C正确;D、因该反应前后气体的体积不变,其他条件不变,再充入0.2 mol Z,因为在等温等容条件下,左右气体化学计量数相等,原平衡环境和D 选项的平衡环境互为等效平衡,平衡不移动,X的体积分数不变,D错误,答案选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F 六种物质的转化关系如图所示(反应条件和部分产物未标出).
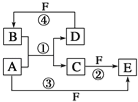
(1)若A为短周期金属单质,D为短周期非金属单质,且所含元素的原子序数A是D的2倍,所含元素的原子最外层电子数D是A的2倍,F的浓溶液与A、D反应都有红棕色气体生成,则A的原子结构示意图为 ,反应④的化学方程式 .
(2)若A是常见的变价金属的单质,D、F是气态单质,且反应①在水溶液中进行.反应②也在水溶液中进行,其离子方程式是 ,已知光照条件下D与F方可以反应.
(3)若A、D、F都是短周期非金属元素单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式为 .将标准状况下3.36L 物质E 与10.0g 氢氧化钠溶液充分反应,所得溶液溶质成分为 (写出化学式和对应的物质的量).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在溶液中能大量共存的是
A.H+、 Na+、HCO3-、Cl- B.Cu2+、Na+、 Cl-、、SO42-
C.Mg2+、K+、SO42-、OH- D.Ag+、Al3+、NO3- 、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列物质与NaOH溶液、稀H2SO4、H2O2溶液均能发生反应的是
A. Fe(NO3)2 B. SiO2 C. Al(OH)3 D. CuSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各反应中,生成物不随反应条件或反应物用量的变化而变化的是( )
A. Na和O2 B. Fe和稀HNO3 C. Cu和FeCl3溶液 D. Na2CO3和稀HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,A气体与B气体反应生成C气体。反应过程中A、B、C浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示,则下列结论正确的是
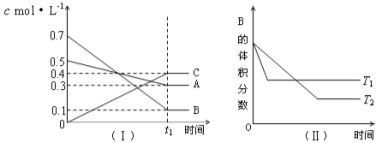
A.在(t1+10)min时,保持其他条件不变,增大压强,平衡向逆反应方向移动
B.在(t1+10)min时,保持容器总压强不变,通入稀有气体,平衡向正反应方向移动
C.T℃时,在相同容器中,若由0.3mol·L—1 A 、0.1 mol·L—1 B和0.4 mol·L—1 C反应,达到平衡后,C的浓度仍为0.4 mol·L—1
D.其他条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)一定条件下,向容积为2L的恒容密闭容器中充入1 mol CH3OH(g)和3 mol H2O(g),CH3OH(g) + H2O(g)![]() CO2(g) + 3H2(g)
CO2(g) + 3H2(g) ![]() H(298K)=+ 49.4 kJ/mol。实验测得:达到平衡状态时,吸收热量19.76 kJ。则
H(298K)=+ 49.4 kJ/mol。实验测得:达到平衡状态时,吸收热量19.76 kJ。则
①达平衡时混合气体的压强是反应前的 倍。
②该条件下反应达平衡状态的依据是(填序号) 。
A.v正(CH3OH)=v正(CO2) B.混合气体的密度不变
C.c(CH3OH)=c(H2O) D.混合气体的总物质的量不变
(2)在25 ℃、101 kPa下,1 g甲醇燃烧生成CO2和液态水时放热Q kJ。则表示甲醇燃烧热的热化学方程式为_____________________。
(3)对于H2O2分解反应,Cu2+也有一定的催化作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
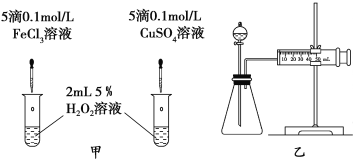
①定性分析:如图甲可通过观察__________________,定性比较得出结论。有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是______________。
②定量分析:用图乙所示装置做对照实验,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。检查该装置气密性的方法是 ,实验中需要测量的数据是_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com