
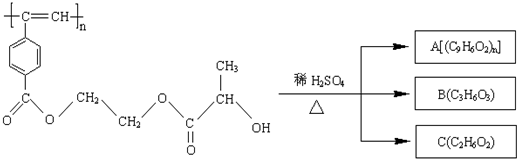
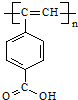
 、HOCH2CH2OH和CH3CHOHCOOH,由此可知A为
、HOCH2CH2OH和CH3CHOHCOOH,由此可知A为 ,B为CH3CHOHCOOH,C为HOCH2CH2OH,结合有机物的结构和官能团的性质解答该题.
,B为CH3CHOHCOOH,C为HOCH2CH2OH,结合有机物的结构和官能团的性质解答该题. 、HOCH2CH2OH和CH3CHOHCOOH,由此可知A为
、HOCH2CH2OH和CH3CHOHCOOH,由此可知A为 ,B为CH3CHOHCOOH,C为HOCH2CH2OH,
,B为CH3CHOHCOOH,C为HOCH2CH2OH, ,B为CH3CHOHCOOH,含有羧基和羟基,故答案为:
,B为CH3CHOHCOOH,含有羧基和羟基,故答案为: ;羧基;羟基;
;羧基;羟基;| 浓H2SO4 |
| △ |
| 浓H2SO4 |
| △ |
 ,故答案为:
,故答案为: ;
;

科目:高中化学 来源: 题型:
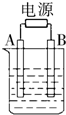 如图用石墨作电极的电解池中,放入某足量蓝色溶液500mL进行电解,观察到A电极表面有红色固体生成,B电极有无色气体生成;通电一段时间后,取出A电极,洗涤、干燥、称量,A电极增重1.6g.下列说法错误的是( )
如图用石墨作电极的电解池中,放入某足量蓝色溶液500mL进行电解,观察到A电极表面有红色固体生成,B电极有无色气体生成;通电一段时间后,取出A电极,洗涤、干燥、称量,A电极增重1.6g.下列说法错误的是( )| A、图中B极同电源正极相连 |
| B、该蓝色溶液可能是Cu(NO3)2或CuCl2溶液 |
| C、电解后溶液的pH约为1(溶液体积变化忽略不计) |
| D、要使电解后溶液恢复到电解前的状态,则可加入2gCuO |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
| n(CO) | n(H2O) | n(H2) | n(CO2) | |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 3 | 3 | 0 | 0 |
| D | 0.5 | 2 | 1 | 1 |
| E | 3 | 1 | 2 | 1 |

查看答案和解析>>
科目:高中化学 来源: 题型:
 X、Y、Z、W、R、E是六种短周期元素,如图是这六种元素的主要化合价与其原子序数的关系,下列说法不正确的是( )
X、Y、Z、W、R、E是六种短周期元素,如图是这六种元素的主要化合价与其原子序数的关系,下列说法不正确的是( )| A、原子半径:Z>W>R>E |
| B、R的气态氢化物比X的气态氢化物沸点高 |
| C、Z与Y可形成既含离子键又含共价键的化合物 |
| D、Z的最高价氧化物对应水化物与W的最高价氧化物对应水化物能发生反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com