
【题目】某学习小组为测定放置已久的小苏打样品中纯碱的质量分数,设计如下实验方案:
(1)方案一:称取一定质量的样品,置于坩埚中加热至恒重后,冷却,称取剩余固体质量,计算。
①完成本实验需要不断用玻璃棒搅拌,其目的是______________________。
②若实验前所称样品的质量为m g,加热至恒重时固体质量为a g,则样品中纯碱的质量分数为____________。
(2)方案二:按如图所示装置进行实验,并回答下列问题:
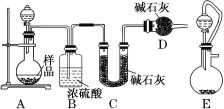
①实验前先检查装置的气密性,并称取一定质量的样品放入A中,将稀硫酸装入分液漏斗中。D装置的作用是_____________________________。
②实验中除称量样品质量外,还需分别称量_______装置反应前、后质量(填装置字母代号)。
③根据此实验得到的数据,测定结果有误差。因为实验装置还存在一个明显的缺陷,该缺陷是__________________________。
④有同学认为,用E装置替代A装置能提高实验准确度。你认为是否正确? (填“是”或“否”)。
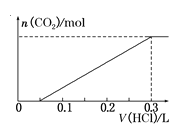
(3)方案三:称取一定量的样品置于锥形瓶中,加适量水,用盐酸进行滴定,从开始至有气体产生到气体不再产生,所滴加的盐酸体积如图所示,则小苏打样品中纯碱的质量分数为 (保留两位有效数字)。
【答案】(1)①使固体样品受热均匀,避免局部温度过高,造成样品外溅
②![]() ×100%
×100%
(2)①避免空气中的水蒸气和二氧化碳进入C装置中,造成实验误差
②C;
③反应产生的二氧化碳残留在A、B装置内,不能完全被吸收
④否
(3)24%
【解析】
试题分析:小苏打久置会发生反应:2NaHCO3![]() Na2CO3+CO2↑+H2O,该样品成分为NaHCO3、Na2CO3,测定样品中纯碱的质量分数方法有:测定二氧化碳的质量、测定碳酸钠的质量、测定碳酸氢钠的质量.
Na2CO3+CO2↑+H2O,该样品成分为NaHCO3、Na2CO3,测定样品中纯碱的质量分数方法有:测定二氧化碳的质量、测定碳酸钠的质量、测定碳酸氢钠的质量.
(1)①使用玻璃棒搅拌,使固体受热均匀,避免局部温度过高,造成固体外溅,
故答案为:使固体受热均匀,避免局部温度过高,造成固体外溅;
②设样品中碳酸氢钠的质量为x,则:
2NaHCO3![]() Na2CO3+CO2↑+H2O 质量减少
Na2CO3+CO2↑+H2O 质量减少
168 62
x (m-a)g
则x=![]() =
=![]() g,故m(Na2CO3)=[m-
g,故m(Na2CO3)=[m-![]() ]g,
]g,
则样品中Na2CO3的质量分数为{[m-![]() ]g÷mg}×100%=
]g÷mg}×100%=![]() ×100%。
×100%。
故答案为:![]() ×100%;
×100%;
(2)①利用C中碱石灰增重测定反应生成二氧化碳的质量,进而计算样品中碳酸钠的质量分数,由于碱石灰可以吸收空气中的二氧化碳与水蒸气,故D装置的作用是吸收空气中的二氧化碳与水蒸气,避免空气中的二氧化碳与水蒸气加入C中,防止测定误差。故答案为:避免空气中的二氧化碳与水蒸气加入C中,造成实验误差;
②C装置反应前后质量之差为反应生成二氧化碳的质量,根据样品总质量、二氧化碳的质量可以计算混合物中碳酸钠的质量,还需分别称量C装置反应前、后的质量。故答案为:C;
③该实验装置有一个明显的缺陷是反应产生的二氧化碳残留在A、B装置内,不能完全被吸收,使C中吸收二氧化碳质量减小,造成较大的误差。故答案为:反应产生的二氧化碳残留在A、B装置内,不能完全被吸收;
④有同学认为,用E装置替代A装置能提高实验准确度,这种说法不正确。因为, E装置用恒压分液漏斗,部分二氧化碳为残留在分液漏斗上部,使C中吸收二氧化碳质量减小,造成较大的误差。故答案为:否;
(3)由图可知,开始发生反应:Na2CO3+HCl=NaHCO3,产生二氧化碳的反应为:HCl+NaHCO3![]() NaCl+CO2↑+H2O,横坐标每个刻度为50mL,令每个刻度为1molHCl,由方程式可知,样品中n(Na2CO3)=1mol,碳酸钠反应生碳酸氢钠为1mol,故原样品中碳酸氢钠的物质的量为5mol-1mol=4mol,则原混合物中碳酸钠的质量分数为
NaCl+CO2↑+H2O,横坐标每个刻度为50mL,令每个刻度为1molHCl,由方程式可知,样品中n(Na2CO3)=1mol,碳酸钠反应生碳酸氢钠为1mol,故原样品中碳酸氢钠的物质的量为5mol-1mol=4mol,则原混合物中碳酸钠的质量分数为![]() ×100%=24%。故答案为:24%.
×100%=24%。故答案为:24%.


科目:高中化学 来源: 题型:
【题目】氮及其化合物在生产、生活中有极其重要的作用。
(1)我国长征系列运载火箭用肼(N2H4)作燃料。N2H4与NH3有相似的化学性质。
①写出肼与盐酸反应的离子方程式:_______________。
②在火箭推进剂中装有液态肼和双氧水,当它们混合时迅速反应生成氮气和水蒸气,写出反应的化学方程式:______________。
③火箭发射时以肼为燃料,也可以用一氧化氮作氧化剂,在此反应过程中若转移2 mol电子,则消耗燃料肼的质量为__________。
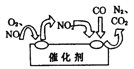
(2)汽车尾气中的氮氧化物是形成酸雨、酸雾的有毒气体之一,为了减少污染,可尝试使用汽车尾气净化装置,其原理如图所示。写出净化过程中总反应的化学方程式:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学在生产和日常生活中有着重要的应用。下列说法不正确的是( )
A.明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化
B.在海轮外壳上镶入锌块,可减缓船体的腐蚀速率
C.根据是否具有丁达尔效应,将分散系分为溶液、浊液、胶体
D.工业上电解熔融的MgCl2,可制得金属镁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 碘单质的升华过程中不存在化学键破坏的过程
B. NaCl溶于水后,因为共价键被破坏,从而形成了Na+和Cl-
C. 在N2、CO2和SiO2物质中,都存在共价键,它们都是由分子构成
D. H2S分子中,所有原子的最外层都达到了8电子的稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuSO4是一种重要的化工原料,其有关制备途径及性质如下图所示。下列说法正确的是
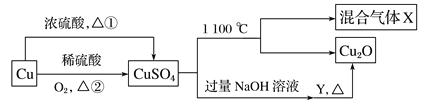
A.相对于途径②,途径①更好地体现了绿色化学思想
B.X可能是SO2和SO3的混合气体
C.Y可以是葡萄糖溶液
D.将CuSO4溶液蒸发,利用余热蒸干,可制得胆矾晶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体血红蛋白中含有Fe2+,如果误食亚硝酸盐,会使人中毒,因为亚硝酸盐会使Fe2+转变为Fe3+,生成高铁血红蛋白而丧失与O2结合的能力。服用维生素C可缓解亚硝酸盐的中毒,这说明维生素C具有 ( )
A. 酸性 B. 碱性 C. 氧化性 D. 还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图如图1可简单表示如下,其中配位键和氢键均采用虚线表示。
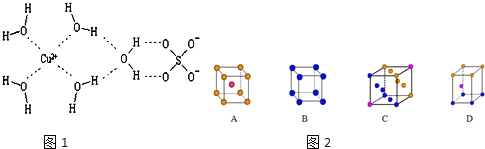
(1)金属铜采用下列______________堆积方式。
(2)Cu2+还能与NH3、Cl-等形成配位数为4的配合物。
①[Cu(NH3)4]2+中存在的化学键类型有______________(填序号)。
A.配位键 B.离子键 C.极性共价键 D.非极性共价键
②元素金(Au)处于周期表中的第六周期,与Cu同族,一种铜合金晶体具有立方最密堆积的结构,在晶胞中Cu原子处于面心,Au原子处于顶点位置,则该合金中Cu原子与Au原子数量之比为______________;
(3)在硫酸铜溶液中逐滴滴加氨水至过量,先出现蓝色沉淀,最后溶解形成深蓝色溶液.写出此蓝色沉淀溶解的离子方程式:______________;
(4)向黄色的三氯化铁溶液中加入无色的KSCN溶液,溶液变成血红色.该反应在有的教材中用方程式FeCl3+3KSCN═Fe(SCN)3+3KCl表示.经研究表明,Fe(SCN)3是配合物,Fe3+与SCN-不仅能以1:3的个数比配合,还可以其他个数比配合.请按要求填空:
①Fe3+与SCN-反应时,Fe3+提供______________,SCN-提供______________,二者通过配位键结合.
②所得Fe3+与SCN-的配合物中,主要是Fe3+与SCN-以个数比1:1配合所得离子显血红色.含该离子的配合物的化学式是______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com