
����Ŀ��ij�������������Al��(NH4)2SO4��MgCl2��FeCl2��AlCl3�е����ֻ������ɣ��ֶԸû����������ʵ�飬����������й�������ͼ��ʾ��������������ѻ���ɱ�״���µ��������

���ڸù����������˵����ȷ����
A. һ������Al��������Ϊ4.5g
B. һ������FeCl2�����ܺ���MgCl2��AlCl3
C. һ������MgCl2��FeCl2
D. һ������(NH4)2SO4��MgCl2�������ʵ������
���𰸡�D
�����������������14.05g����������������������Һ�������壬����κͼӦ�������ɵİ�����Ҳ�����ǽ�����������������Һ��Ӧ����������5.60L����ͨ����ʯ���ޱ仯��˵�������������ʯ�ҷ�Ӧ�����壬��ˮ�����Ĵ��ڣ�ͨ��Ũ���ᣬ����ʣ��3.36L���������5.60L-3.36L=2.24L����ϻ������ܴ��ڵ����ʿ�֪��һ��������������������Ʒ�Ӧ���ɰ���Ϊ2.24L��ʣ�������ֻ�������������Ϊ3.36L��˵��ԭ�������һ����������14.05g����������������������Һ�в�����ɫ����2.9g�������ޱ仯������������������ǿ����������ɰ�ɫ������һ���Ȼ�þ���ɵ�������þ��ɫ����������Ϊ2.90g��������ͭΪ��ɫ���������Թ���������һ��������FeCl2��14.05g����������������������Һ�õ���ɫ��Һ�������������� �����ɳ�����˵�����������Ȼ���������Ӧ���ɵ�ƫ�����������ᷴӦ���ɵ������������������������������ܽ��һ��֤������������������A������������һ������Al�����Ը��ݱ����3.36L�������Լ�����������ʵ���Ϊ0.1mol������Ϊ2.7g����A����B���������Ϸ�����֪������������һ������MgCl2����B����C�����ݼ�������������Һ�����ɰ�ɫ�������Ұ�ɫ����û�б仯�������������һ������MgCl2��һ������FeCl2����C����D���������Ϸ�����֪��ԭ����������һ������(NH4)2SO4��MgCl2����D��ȷ����ѡD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ӦCH3OH(g) + NH3(g)![]() CH3NH2(s) + H2O(g)�ڸ����²����Է����ҽ��У���÷�Ӧ�Ħ�H����SӦΪ( )
CH3NH2(s) + H2O(g)�ڸ����²����Է����ҽ��У���÷�Ӧ�Ħ�H����SӦΪ( )
A����H��0����S��0
B����H��0����S��0
C����H��0����S��0
D����H��0����S��0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����-Fenton��������ˮ�����л���Ⱦ�オ��ĸ������������䷴Ӧԭ����ͼ��ʾ�����е�������H2O2��Fe2+����Fenton��Ӧ��Fe2++H2O2![]() Fe3++OH- +��OH�����ɵ��ǻ����ɻ�(��OH)�����������л���Ⱦ�����˵������ȷ����
Fe3++OH- +��OH�����ɵ��ǻ����ɻ�(��OH)�����������л���Ⱦ�����˵������ȷ����

A����Դ��A���Ǹ���
B��������ֻ��O2��Fe3+������ԭ��Ӧ
C�������Ϸ����缫��Ӧ��H2O-e-![]() ��OH + H+
��OH + H+
D������1molO2�����Բ���4mol ��OH
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йؽ����˵����ȷ����
A������һ���ǻ����
B����������Һ�ı����������ж����ЧӦ
C���������Ȼ�����Һ����ϡ����������Һ�м��ȣ��ɵ�������������
D��������ͨ����Ĥ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��X��Y��Z��W��R�Ļ��ϼ���ԭ�������Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ� �� 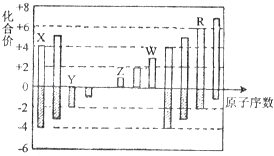
A.ԭ�Ӱ뾶��Z��Y��X
B.��̬�⻯����ȶ��ԣ�Y��R
C.Z��Y�γɵĻ����������ӻ�����
D.�����µ���W������R������������Ӧˮ�����Ũ��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ������ľ̿��ʢ�е������������������ܱ�������ȼ�պ�����CO��CO2���Ҳ�÷�Ӧ������CO��CO2��N2�Ļ��������̼Ԫ�ص���������Ϊ24������Ӧ�������е�����������������Ϊ�� ��
A. 10�� B. 30�� C. 50�� D. 70��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����ԭ��HSO3-��I-��������IO3-��I2���ں�3 mol NaHSO3����Һ����μ���NaIO3��Һ������NaIO3�����ʵ����ͺ�������I2�����ʵ����Ĺ�ϵ������ͼ������˵����ȷ���ǣ���

A����Ӧ�����е����������ΪNa2SO4
B��a ��ʱ����NaHSO3�����ʵ���Ϊ1.0mol
C��0��b��ķ�Ӧ�����������ӷ���ʽ��ʾ��3HSO3-+IO3-+3OH-=3SO42-+I-+3H2O
D������Һ��I-��I2�����ʵ���֮��Ϊ5:3ʱ�������NaIO3Ϊ1.1mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾһЩ�����е�ijЩ�ṹ�����Ƿֱ���NaCl���ɱ������ʯ��ʯī�ṹ�е�ijһ�ֵ�ijһ���֣� 
��1�����д������ʯ���ǣ�������ĸ����ͬ����
��2�����д���ʯī���� ��
��3�����ʯ��ʯī����̼�� ��
��4�������ɱ�����C������������
��5��CO2���Ӽ�ͨ�����������
��6������������A��B��C�����۵��ɸߵ��͵�����˳��Ϊ �� ������ĸ��ʾ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����2Na(s) +![]() O2(g)=Na2O(s) ��H=-414 kJ/mol
O2(g)=Na2O(s) ��H=-414 kJ/mol
��2Na(s) +O2 (g)=Na2O2(s) ��H=-511 kJ/mol
����˵������ȷ����
A. ��Ӧ�ٺ͢ھ����ڷ��ȷ�Ӧ
B. �ٺ͢ڲ�����������Ӹ�������ͬ
C. �ٺ͢����ɵ����ʵ����IJ��ת�Ƶ�������ͬ
D. ��ӦNa2O2(s)+2Na(s)=2 Na2O(s)����H =- 317 kJ/mol
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com