
| A£® | ÖŹĮæ±ČŹĒ9£ŗ22 | B£® | ĻąĶ¬Ģõ¼žĻĀµÄĆܶČŅ»¶ØĻąĶ¬ | ||
| C£® | Ō×ÓøöŹż²»Ķ¬ | D£® | ĻąĶ¬Ģõ¼žĻĀĢå»żŅ»¶ØĻąĶ¬ |
·ÖĪö øł¾Żm=nM£¬V=nVm£¬$¦Ń=\frac{m}{V}$£¬½įŗĻ·Ö×Ó¹¹³É¼ĘĖć£®
½ā“š ½ā£ŗA£®amolH2OŗĶamolCO2µÄÖŹĮæ±ČŹĒ18a£ŗ44a=9£ŗ22£¬¹ŹAÕżČ·£»
B£®ĻąĶ¬Ģõ¼žĻĀµÄĆܶČÖ®±ČµČӌĦ¶ūÖŹĮæÖ®±Č£¬ĖłŅŌĆܶČŅ»¶Ø²»ĻąĶ¬£¬¹ŹB“ķĪó£»
C£®amolH2OÖŠŗ¬ÓŠ3amolŌ×Ó£¬amolCO2ÖŠŗ¬ÓŠ3amolŌ×Ó£¬Ō×ÓøöŹżĻąĶ¬£¬¹ŹC“ķĪó£»
D£®ŌŚ±ź×¼×“æöĻĀ£¬Ė®ĪŖŅŗĢ壬ĖłŅŌamolH2OŗĶamolCO2µÄĢå»ż²»ĻąĶ¬£¬¹ŹD“ķĪó£®
¹ŹŃ”A£®
µćĘĄ ±¾Ģāæ¼²éĪļÖŹµÄĮæµÄ¼ĘĖć”¢°¢·ü¼ÓµĀĀŽ¶ØĀɼ°ĶĘĀŪ£¬²ąÖŲӌѧɜµÄ·ÖĪöÄÜĮ¦ŗĶ¼ĘĖćÄÜĮ¦µÄ漲飬ĢāÄæÄѶČÖŠµČ£¬×¢ŅāĪļÖŹµÄĮæÓėĢå»ż”¢Ō×ÓŹżÄæµÄ¼ĘĖć¹«Ź½µÄŌĖÓĆ£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ćŗ”¢ŹÆÓĶŹĒ²»æÉŌŁÉśÄÜŌ“£¬ĢģČ»ĘųŹĒæÉŌŁÉśÄÜŌ“ | |
| B£® | ŌŚ»Æѧ·“Ó¦ÖŠ£¬·“Ó¦Īļ×Ŗ»ÆĪŖÉś³ÉĪļµÄĶ¬Ź±£¬±ŲČ»·¢ÉśÄÜĮæµÄ±ä»Æ | |
| C£® | ČČÖµÖøŌŚŅ»¶ØĢõ¼žĻĀ£¬1molµÄĪļÖŹĶźČ«Č¼ÉÕĖł·Å³öµÄČČĮæ | |
| D£® | Čō»Æѧ¹ż³ĢÖŠ¶ĻæŖ»Æѧ¼ü·Å³öµÄÄÜĮæ“óÓŚŠĪ³É»Æѧ¼üĖłĪüŹÕµÄÄÜĮ棬Ōņ·“Ó¦·ÅČČ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
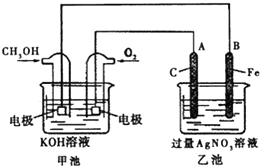 ČĖĆĒÓ¦ÓĆŌµē³ŲŌĄķÖĘ×÷ĮĖ¶ąÖÖµē³Ų£¬ŅŌĀś×ć²»Ķ¬µÄŠčŅŖ£®ŅŌĻĀĆ抔ĢāÖŠµÄµē³Ų¹ć·ŗŹ¹ÓĆÓŚČÕ³£Éś»ī”¢Éś²śŗĶæĘѧ¼¼ŹõµČ·½Ćę£¬Ēėøł¾ŻĢāÖŠµÄŠÅĻ¢£¬ĢīŠ“æÕøń£®
ČĖĆĒÓ¦ÓĆŌµē³ŲŌĄķÖĘ×÷ĮĖ¶ąÖÖµē³Ų£¬ŅŌĀś×ć²»Ķ¬µÄŠčŅŖ£®ŅŌĻĀĆ抔ĢāÖŠµÄµē³Ų¹ć·ŗŹ¹ÓĆÓŚČÕ³£Éś»ī”¢Éś²śŗĶæĘѧ¼¼ŹõµČ·½Ćę£¬Ēėøł¾ŻĢāÖŠµÄŠÅĻ¢£¬ĢīŠ“æÕøń£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
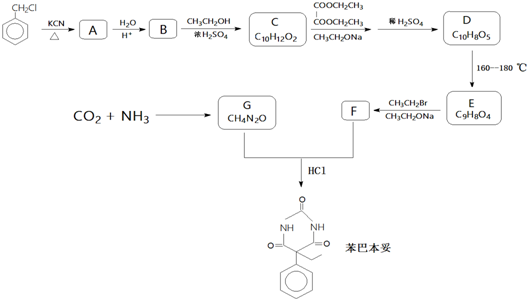
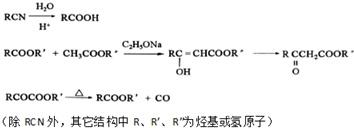
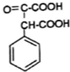 £»E”śFµÄ·“Ó¦ĄąŠĶČ”“ś·“Ó¦
£»E”śFµÄ·“Ó¦ĄąŠĶČ”“ś·“Ó¦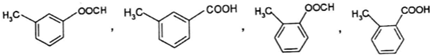 £ØĘäÖŠŅ»ÖÖ£©£®
£ØĘäÖŠŅ»ÖÖ£©£® ŗĶ±½»·½į¹¹£»
ŗĶ±½»·½į¹¹£»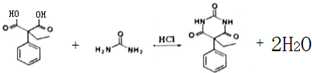 £®
£®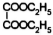 £©µÄŗĻ³ÉĀ·ĻߣØÓĆĮ÷³ĢĶ¼±ķŹ¾£»ĪŽ»śŹŌ¼ĮČĪŃ”£©£®
£©µÄŗĻ³ÉĀ·ĻߣØÓĆĮ÷³ĢĶ¼±ķŹ¾£»ĪŽ»śŹŌ¼ĮČĪŃ”£©£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
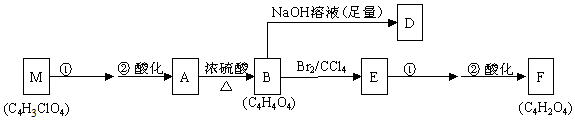
 +£Ø2n-1£©H2O £®
+£Ø2n-1£©H2O £® £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
 ijŠĖȤŠ”×éµÄĶ¬Ń§Éč¼ĘĮĖČēĶ¼×°ÖĆ½ųŠŠŹŌŃéĢ½¾æ£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
ijŠĖȤŠ”×éµÄĶ¬Ń§Éč¼ĘĮĖČēĶ¼×°ÖĆ½ųŠŠŹŌŃéĢ½¾æ£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ| ŠņŗÅ | ÉÕĘæÖŠµÄĪļÖŹ | ²āµĆĘųĢåĢå»ż |
| ŹµŃé1 | 20mL H2O2£¬×ćĮæMnO2 | V1 |
| ŹµŃé2 | 20mL H2O2£¬×ćĮæMnO2ŗĶĻ”ĮņĖį | V1£¼V2£¼2V1 |
| ±ąŗÅ | Ć¾ĀĮŗĻ½šÖŹĮæ | ĮæĘų¹ÜµŚŅ»“Ī¶ĮŹż | ĮæĘų¹ÜµŚ¶ž“Ī¶ĮŹż |
| ¢ń | 1.0g | 10.00mL | 346.30mL |
| ¢ņ | 1.0g | 10.00mL | 335.50mL |
| ¢ó | 1.0 g | 10.00mL | 346.00mL |
| ¢ō | 1.0g | 10.00mL | 345.70mL |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com