
| A.等于0.1mol/L | B.等于0.2mol/L |
| C.小于0.1mol/L | D.在0.1~0.2mol/L之间 |
 (2)C (3)S2- +H2O HS-+ OH-
(2)C (3)S2- +H2O HS-+ OH-  HS-+H+、HS-
HS-+H+、HS- S2-+H+可知,H2S第一步电离出的H+,对HS-的电离起到抑制作用,使HS-更难电离出H+,所以K1远大于K2。
S2-+H+可知,H2S第一步电离出的H+,对HS-的电离起到抑制作用,使HS-更难电离出H+,所以K1远大于K2。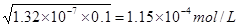 ,所以答案选C。
,所以答案选C。 HS-+ OH-。
HS-+ OH-。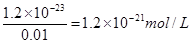 。根据电离平衡常数表达式可知
。根据电离平衡常数表达式可知 ,所以此时溶液中氢离子浓度是
,所以此时溶液中氢离子浓度是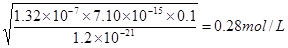 ,即溶液中氢离子不能低于0.28mol/L。
,即溶液中氢离子不能低于0.28mol/L。

科目:高中化学 来源:不详 题型:单选题
| A.常温下,稀释0.1 mol/L的氨水,溶液中c(OH-)、c(NH4+)、c(H+)均下降 |
| B.常温下,c(NH4+)相等的①(NH4)2SO4②(NH4)2Fe(SO4)2③NH4Cl④(NH4)2CO3溶液中,溶质物质的量浓度大小关系是:②<①<④<③ |
| C.pH相等的CH3COONa、NaHCO3和Na2CO3三种溶液:c(CH3COONa)<c(NaHCO3) <c(Na2CO3) |
| D.某温度时水的离子积常数KW=10-13若将此温度下pH=11的NaOH溶液aL与pH=1的稀硫酸bL混合,若所得混合液PH=2,则a:b=2:9 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.明矾溶液加热 | B.CH3COONa溶液加热 |
| C.氨水中加入少量NH4Cl固体 | D.NaHCO3溶液中加入少量NaCl固体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 弱酸的化学式 | CH3COOH | HCN | H2S |
| 电离常数(25℃) | 1.8×10-5 | 4.9×10-10 | K1=1.3×10-7 K2=7.1×10-15 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.常温时, 溶液的 溶液的 ,则该溶液中 ,则该溶液中 |
B. 溶液与 溶液与 溶液反应至中性的离子方程式为: 溶液反应至中性的离子方程式为: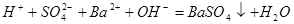 |
C.常温下物质的量浓度相等的下列四种溶液:① ;② ;② ;③ ;③ ;④ ;④ ,四种溶液中 ,四种溶液中 比较:② 比较:② ① ① ④ ④ ③ ③ |
D.常温下 的溶液: 的溶液: 、 、 、 、 、 、 可以常量共存 可以常量共存 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 溶质 | Na2CO3 | NaHCO3 | NaClO | NaHSO3 |
| pH | 11.6 | 9.7 | 10.3 | 4.0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | A | B | C | D |
| 碱性 | AOH>BOH | AOH<BOH | AOH>BOH | AOH<BOH |
| 酸性 | HC>HD | HC>HD | HC<HD | HC<HD |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.BeCl2溶液的pH<7,将其蒸干,灼烧后可得残留物Be(OH)2 |
| B.Na2BeO2溶液的pH>7,将其蒸干,灼烧后可得残留物BeO |
| C.Be(OH)2既能溶于盐酸,又能溶于NaOH溶液 |
| D.BeCl2水溶液导电性强,因此BeCl2应该是离子化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com