
相同物质的量的KClO3分别发生下述反应:①有催化剂MnO2存在时,受热分解得到氧气;②若不使用催化剂,加热至470 ℃左右,得到KClO4(高氯酸钾)和KCl。下列关于①和②的说法不正确的是( )
A.都属于氧化还原反应
B.发生还原反应的元素相同
C.发生氧化反应的元素不同
D.生成KCl的物质的量相同
科目:高中化学 来源: 题型:
已知:
甲醇脱水反应
2CH3OHg)===CH3OCH3g)+H2Og)ΔH1=-23.9 kJ·mol-1
甲醇制烯烃反应
2CH3OHg)===C2H4g)+2H2Og)ΔH2=-29.1 kJ·mol-1
乙醇异构化反应
C2H5OHg)===CH3OCH3g)ΔH3=+50.7 kJ·mol-1
则乙烯气相直接水合反应C2H4g)+H2Og)===C2H5OHg)的ΔH=________kJ·mol-1。
2)[2012·广东理综,314)]碘也可用作心脏起搏器电源——锂碘电池的材料。
该电池反应为:2Lis)+I2s)===2Lis) ΔH
已知:4Lis)+O2g)===2Li2Os) ΔH1
4LiIs)+O2g)===2I2s)+2Li2Os) ΔH2
则电池反应的ΔH=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
有一种锂电池,用金属锂和石墨作电极材料,电解质溶液是由四氯铝锂(LiAlCl4)溶解在亚硫酰氯(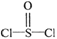 )中而形成的,电池总反应方程式为:8Li+3SOCl2=6LiCl+Li2SO3+2S,下列叙述中正确的是( )
)中而形成的,电池总反应方程式为:8Li+3SOCl2=6LiCl+Li2SO3+2S,下列叙述中正确的是( )
A.电解质溶液中混入水,对电池反应无影响。
B.金属锂作电池的正极,石墨作电池的负极。
C.电池工作过程中,亚硫酰氯(SOCl2)被还原为Li2SO3。
D.电池工作过程中,金属锂提供的电子与正极区析出硫的物质的量之比为4:l。
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上用赤铁矿生产铁,可以选择的还原剂有C和H2。根据所学的知识判断:哪一种还原剂可使反应自发进行的温度较低?
已知:Fe2O3(s)+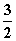 C(s)===2Fe(s)+
C(s)===2Fe(s)+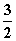 CO2(g)
CO2(g)
ΔH=233.8 kJ·mol-1,ΔS=0.279 kJ·mol-1·K-1
Fe2O3(s)+3H2(g)===2Fe(s)+3H2O(g)
ΔH=98 kJ·mol-1,ΔS=0.144 2 kJ·mol-1·K-1
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室可用浓盐酸分别与KMnO4、MnO2、KClO3等多种物质在一定条件下反应制取氯气
①上述反应中,HCl表现的性质是________、________。
②在常温下,浓盐酸与KMnO4可反应生成氯气,KMnO4中的Mn被还原为+2价,该反应的化学方程式:__________________________________________________________________
________________________________________________________________________。
③KMnO4、MnO2和Cl2的氧化性由强到弱的顺序是:
________________________________________________________________________。
④已知KClO3+6HCl(浓)===KCl+3Cl2↑+3H2O,用双线桥表示该反应的电子转移情况:
________________________________________________________________________。
⑤用上述三种物质分别制取标准状况下3.36 L氯气时,转移的电子数分别是__________________(NA表示阿伏加德罗常数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质氧化性或还原性强弱的叙述错误的是( )
A.Cl2、Br2、I2的氧化性能作为氯、溴、碘元素非金属性递变规律的判断依据[2014·福建理综,23(2)b]
B.同主族元素的简单阴离子还原性越强,水解程度越大(2013·天津理综,3C)
C.将少量溴水加入KI溶液中,再加入CCl4,振荡,静置,可观察到下层液体呈紫色,验证Br2的氧化性强于I2(2014·四川理综,4C)
D.将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡,静置,下层溶液显紫红色,说明氧化性:Fe3+>I2(2014·广东理综,22D)
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应①Fe(s)+CO2(g)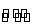 FeO(s)+CO(g)的平衡常数为K1;反应②Fe(s)+H2O(g)
FeO(s)+CO(g)的平衡常数为K1;反应②Fe(s)+H2O(g)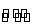 FeO(s)+H
FeO(s)+H 2(g)的平衡常数为K2。 反应CO2(g)+H2(g)
2(g)的平衡常数为K2。 反应CO2(g)+H2(g) 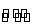 CO(g)+H2O(g)的平衡常数K为( )
CO(g)+H2O(g)的平衡常数K为( )
A.K1+K2 B.K1-K2 C.K1· K2 D.K1/K2
K2 D.K1/K2
查看答案和解析>>
科目:高中化学 来源: 题型:
1 000 K时反应C(s)+2H2(g)
 CH4(g)的K=8.28×107 (mol·L-1)-1,当各气体物质的量浓度分别为H2 0.7 mol·L-1、CH4 0.2 mol·L-1时,上述反应( )
CH4(g)的K=8.28×107 (mol·L-1)-1,当各气体物质的量浓度分别为H2 0.7 mol·L-1、CH4 0.2 mol·L-1时,上述反应( )
A.正向移动 B.逆向移动 C.达到平衡 D.不一定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com