
下列关于化学平衡常数的说法中,正确的是( )
|
| A. | 在任何条件下,化学平衡常数都是一个定值 |
|
| B. | 当改变反应物的浓度时,化学平衡常数会发生改变 |
|
| C. | 化学平衡常数K只与温度、反应物浓度、体系的压强都有关 |
|
| D. | 化学平衡常数K可以推断一个可逆反应进行的程度 |
考点:
化学平衡常数的含义.
专题:
化学平衡专题.
分析:
平衡常数指各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,化学平衡常数只与温度有关,与浓度、压强无关,平衡常数越大,说明可逆反应进行的程度越大.
解答:
解:A、化学平衡常数只受温度影响,同一反应温度不同,平衡常数不同,故A错误;
B、同一反应,平化学衡常数只受温度影响,与反应物的浓度无关,故B错误;
C、同一反应,平化学衡常数只受温度影响,与反应物浓度、体系的压强无关,故C错误;
D、平衡常数越大,说明可逆反应进行的程度越大,故D正确;
故选D.
点评:
本题考查了化学平衡常数、影响因素及应用,难度不大,注意化学平衡常数只与温度有关,同一转化关系化学计量数不同,平衡常数不同,温度相同,同一可逆反应的正、逆反应平衡常数互为倒数.


科目:高中化学 来源: 题型:
对于以下反应:A(s)+3B(g)⇌2C(g)+D(g),在一定温度和容积固定的容器中,下列判断正确的是( )
|
| A. | 当容器内的压强不再变化,可以判断反应已经达到平衡 |
|
| B. | 往容器中通入稀有气体He,由于压强增大,所以反应速率增大 |
|
| C. | 往容器中加入少量A,反应速率增大 |
|
| D. | 若反应是放热反应,升高温度,正反应速率增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
现在要分离下列物质,请根据分离实例,将合适的分离方法填在后面的直线上.
(1)要除去NaCl溶液中的泥沙
(2)用CCl4提取溴水中的溴单质
(3)分离乙酸(沸点118℃)与乙酸乙酯(沸点77.1℃)
(4)分离汽油和水
(5)从含有少量NaCl的KNO3溶液中提取KNO3
(6)分离Fe(OH)3胶体中含有的FeCl3 .
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E、F六种物质有如下变化关系,E是淡黄色粉末,判断:
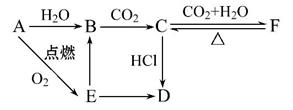
(1)写出A、B、C、D、E、F的化学式:
A. ;B. ;C. ;
D. ;E. ;F. 。
(2)写出有关反应的化学方程式(是离子反应的直接写出离子方程式)
B C: ___________________________________________________,
C: ___________________________________________________,
E B: __________________________________________________,
B: __________________________________________________,
C F: __________________________________________________,
F: __________________________________________________,
F C: __________________________________________________。
C: __________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在铁制品上镀上一定厚度的锌层,以下设计方案正确的是( )
|
| A. | 锌作阳极,镀件作阴极,溶液中含有锌离子 |
|
| B. | 铂作阴极,镀件作阳极,溶液中含有锌离子 |
|
| C. | 铁作阳极,镀件作阴极,溶液中含有亚铁离子 |
|
| D. | 锌用阴极,镀件作阳极,溶液中含有锌离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
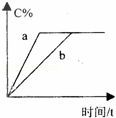
在a、b两个相同的容器中,分别加入相同量的A和B,发生可逆反应:A(g)+3B(g)⇌2C(g)(正反应为放热反应),两容器中C的体积分数与时间的关系如图所示,则a、b两线不同的可能原因是( )
|
| A. | a的温度高于b | B. | a使用了催化剂,而b未用 |
|
| C. | a的压强大于b | D. | a的温度低于b |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各基态原子或离子的电子排布式正确的是( )
|
| A. | O2﹣1s22s22p4 | B. | Ca[Ar]3d2 |
|
| C. | Fe[Ar]3d54s3 | D. | Si 1s22s22p63s23p2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列判断正确的是( )
|
| A. | 根据同周期元素的第一电离能变化趋势,推出P的第一电离能比S大 |
|
| B. | 根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正化合价都是+7 |
|
| C. | 晶体中一定存在化学键 |
|
| D. | 正四面体分子中键角只能是109°28′ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com