
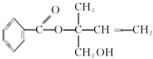
| A. | X的分子式为C12H16O3 | |
| B. | 可用酸性高锰酸钾溶液区分苯和X | |
| C. | 若单键可以旋转,有机物X中一定在同一平面上的碳原子数为8 | |
| D. | 在Ni作催化剂的条件下,1 molX最多只能与1molH2加成 |
分析 有机物含有酯基,可发生水解,含有碳碳双键,可发生加成、加聚和氧化反应,含有羟基,可发生取代、氧化反应,以此解答该题.
解答 解:A.由有机物结构简式可知有机物分子式为C12H14O3,故A错误;
B.X含有碳碳双键,可与酸性高锰酸钾发生氧化还原反应,可用于区别苯,故B正确;
C.苯环具有平面形结构,与苯环直接相连的原子在同一个平面上,若单键可以旋转,有机物X中一定在同一平面上的碳原子数为至少为7,故C错误;
D.能与氢气发生加成反应的为苯环和碳碳双键,则1mol X最多只能与4mol H2加成,故D错误.
故选B.
点评 本题考查有机物的结构和性质,为高考常见题型,侧重于学生的分析能力的考查,注意把握有机物的结构和官能团的性质,为解答该类题目的关键,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 乙酸与乙醇生成乙酸乙酯,苯与硝酸生成硝基苯属于同一类型的反应 | |
| B. | C3H8与C4H10一定互为同系物,分子式为C2H6O的有机物有2种 | |
| C. | 石油裂解可以得到丙烯,煤干馏可以得到苯,丙烯和苯均可使溴水褪色且原理相同 | |
| D. | 植物秸秆和土豆淀粉在一定条件下水解的产物都可以转化为酒精 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
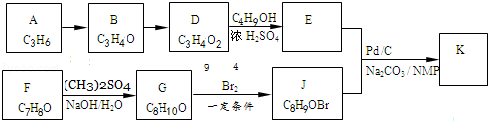
 .
. 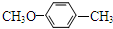 ;K
;K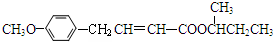 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
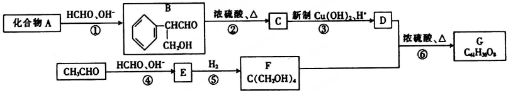
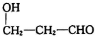
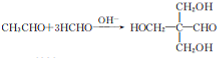 .
.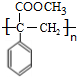 (填结构简式).
(填结构简式).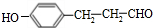 (填结构简式).
(填结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
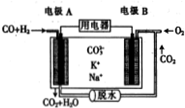 水煤气(CO、H2)作燃料电池的燃料可提高利用率和减少碳的排放,以水煤气为燃料的某熔融碳酸盐燃料电池的工作原理如图所示.下列说法正确的( )
水煤气(CO、H2)作燃料电池的燃料可提高利用率和减少碳的排放,以水煤气为燃料的某熔融碳酸盐燃料电池的工作原理如图所示.下列说法正确的( )| A. | 电极A上H2参与的电极反应为H2+2OH--2e-=2H2O | |
| B. | 电极B上发生的电极反应为O2+2CO2+4e-=2CO32- | |
| C. | 电池工作时,K+向电极A移动 | |
| D. | 若电极B上消耗2molO2,则电极A上消耗4molCO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 解释与结论 |
| A | 向某溶液中加入BaCl2溶液 | 有白色沉淀产生 | 生成了难溶于水的BaSO4,该溶液中一定含有SO42- |
| B | 向少量AgNO3溶液中滴加适量NaCl溶液,再滴加适量稀NaI溶液 | 开始有白色沉淀生成,后有黄色沉淀生成 | Ksp(AgI)<Ksp(AgCl) |
| C | 向苯中滴入少量浓溴水,振荡,静置 | 溶液分层,上层呈橙红色,下层几乎无色 | 苯和溴水发生取代反应,使溴水褪色 |
| D | 向蔗糖中加入浓硫酸 | 变黑,放热,体积膨胀,放出刺激性气体 | 浓硫酸具有吸水性和强氧化性,反应中生成C、SO2和CO2等 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 有机物 | A | B | C |
| 结构(分子式)及性质 | 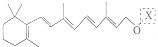 ,水解生成B和C ,水解生成B和C | 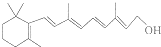 | ①分子式为C7H6O3; ②遇FeCl3水溶液呈紫色 ③与NaHCO3溶液反应产生CO2气体. |

 、
、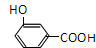 .
.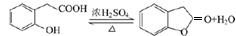 ;
;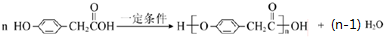 .
.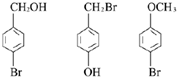 任意一种.
任意一种.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a与其他三种元素形成的二元化合物中其化合价均为+1 | |
| B. | b与其他三种元素均可形成至少两种二元化合物 | |
| C. | c的原子半径是这些元素中最大的 | |
| D. | d与a形成的化合物的溶液呈弱酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com