
【题目】研究发现,含Pm2.5的雾霾主要成分有CO2、SO2、NOx、CxHy及可吸入颗粒等。为减少雾霾要进行脱硝、脱硫、脱碳,请回答下列问题:
(1)脱硝。为消除NOx对环境的污染,利用NH3在一定条件下与NO反应生成无污染气体。
已知:4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) △H=-905kJ/mol
4NO(g)+6H2O(g) △H=-905kJ/mol
N2(g)+O2(g)![]() 2NO(g) △H=+180 kJ/mol
2NO(g) △H=+180 kJ/mol
①NH3(g)与NO(g)在一定条件下反应的热化学方程式为:______________________。
②下图是①中反应过程中NH3的体积分数随X变化的示意图,X代表的物理量可能是___________,原因是___________。

(2)脱硫。下图电解装置可将雾霾中的SO2、NO转化为(NH4)2SO4。

①装置中发生反应的化学方程式为___________。
②阴极的电极反应式是___________。
③某种脱硫工艺中将废气处理后,与一定量的氨气、空气反应,生成硫酸铵和硝酸铵的混合物,可作为化肥。硫酸铵和硝酸铵的水溶液pH<7,其原因用离子方程式表示为___________;常温下,在一定物质的量浓度的硝酸铵溶液中滴加适量的NaOH溶液,使溶液的pH=7,则溶液中c(Na+)___________c(NO3-)(填写“>”“=”或“<”)。

(3)脱碳。将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H 取五份等体积的CO2和H2的混合气体(物质的量之比均为1:3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数
CH3OH(g)+H2O(g) △H 取五份等体积的CO2和H2的混合气体(物质的量之比均为1:3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数![]() (CH3OH)与反应温度T的关系曲线如下图所示,则上述CO2转化为甲醇的反应的△H=___________0(填“>”“<”或“=”)。请解释b比a纵坐标大的原因___________。
(CH3OH)与反应温度T的关系曲线如下图所示,则上述CO2转化为甲醇的反应的△H=___________0(填“>”“<”或“=”)。请解释b比a纵坐标大的原因___________。
【答案】4NH3(g)+6NO(g)![]() 5N2(g)+6H2O(g) △H= -1805 kJ/mol 温度或压强 因为该反应是放热及体积增大的可逆反应,升高温度或增大压强,平衡均逆向移动,使NH3的体积分数增大 5SO2+2NO+8H2O
5N2(g)+6H2O(g) △H= -1805 kJ/mol 温度或压强 因为该反应是放热及体积增大的可逆反应,升高温度或增大压强,平衡均逆向移动,使NH3的体积分数增大 5SO2+2NO+8H2O![]() (NH4)2SO4+ 4H2SO4 NO+5e-+6H+=NH4++H2O NH4++H2O
(NH4)2SO4+ 4H2SO4 NO+5e-+6H+=NH4++H2O NH4++H2O![]() NH3·H2O+H+ < < 由图可知a、b均未达到平衡状态,随温度升高,反应速率加快,即v(b)>v(a),在相同时间内,b生成的甲醇多,体积分数大
NH3·H2O+H+ < < 由图可知a、b均未达到平衡状态,随温度升高,反应速率加快,即v(b)>v(a),在相同时间内,b生成的甲醇多,体积分数大
【解析】
(1)①根据盖斯定律,将两个热化学方程式叠加,就可得到相应反应的热化学方程式;
②根据该反应的正反应是放热反应,且是体积增大的可逆反应,利用温度、压强对平衡的影响分析;
(2)①SO2失电子形成硫酸;
②NO得电子生成铵根;
③溶液中铵根离子水解显示酸性,硝酸铵溶液中滴加适量的NaOH溶液溶液的pH=7,则反应后溶液中氢离子和氢氧根离子浓度相等,根据电荷守恒来判断;
(3)根据图象分析,甲醇含量随温度变化的曲线特征,开始反应进行,平衡后,升温平衡逆向进行,根据温度对化学平衡移动的影响知识来回答,a、b两点均为平衡状态,温度升高,反应速率加快,产物甲醇的体积分数会增大。
(1)①已知a:4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H=-905kJ/mol
b:N2(g)+O2(g)=2NO(g) △H=180kJ/mol
依据盖斯定律,b×5,整理可得热化学方程式合并计算:Ⅰ×5+Ⅱ得到:4NH3(g)+6NO(g)=5N2(g)+6H2O(g) △H=-1805kJ/mol,
②该反应的正反应是气体体积增大的放热反应,升高温度或增大压强,平衡均逆向移动,从而使NH3的体积分数增大;
(2)①SO2中的S元素化合价为+4价,在反应中失电子变为+6价的硫酸,反应方程式:5SO2+2NO+8H2O![]() (NH4)2SO4+4H2SO4;
(NH4)2SO4+4H2SO4;
②在阴极上NO得电子生成NH4+,电极反应式为:NO+5e-+6H+=NH4++H2O;
③硫酸铵和硝酸铵都是强酸弱碱盐,在水溶液中NH4+发生水解反应,消耗水电离产生的OH-,当最终达到平衡时,溶液中c(H+)>c(OH-),所以溶液的pH<7,其原因用离子方程式表示为NH4++H2O![]() NH3H2O+H+,常温下,向一定物质的量浓度的硝酸铵溶液中滴加适量的氨水溶液,使溶液的pH=7,则c(H+)=c(OH-),由于溶液中存在电荷守恒,所以c(H+)+c(NH4+)+c(Na+)=c(NO3-)+c(OH-),而c(H+)=c(OH-),因此c(NH4+)+c(Na+)=c(NO3-),所以c(Na+)<c(NO3-);
NH3H2O+H+,常温下,向一定物质的量浓度的硝酸铵溶液中滴加适量的氨水溶液,使溶液的pH=7,则c(H+)=c(OH-),由于溶液中存在电荷守恒,所以c(H+)+c(NH4+)+c(Na+)=c(NO3-)+c(OH-),而c(H+)=c(OH-),因此c(NH4+)+c(Na+)=c(NO3-),所以c(Na+)<c(NO3-);
(3)根据图象分析知道:在温度不很高时,升高温度,更多的反应物转化为甲醇,甲醇的含量增大,当反应达到平衡后,再温度升高,甲醇的体积分数φ(CH3OH)减小,说明是个温度,化学平衡逆向移动,逆反应是吸热反应,因此该反应的正反应是放热反应,属于△H<0;另外图中a、b均是未达到平衡状态,由于温度b>a,温度越高,化学反应速率加快,所以v(b)>v(a);在相同时间内,速率越快,产生的甲醇就越多,由于v(b)>v(a),所以b生成的甲醇多,甲醇的体积分数大,即比a纵坐标大。


科目:高中化学 来源: 题型:
【题目】填空题。
(1)47.5g某二价金属的氯化物中含有1molCl-,则该金属氯化物的摩尔质量为_______ ;该金属的相对原子质量为_______ 。
(2)标准状况下,3.4g NH3 的体积为_______ ;它与标准状况下_______ L H2S含有相同数目的氢原子。
(3)已知CO、CO2混合气体的质量共10.0g,在标准状况下的体积为6.72L,则混合气体中CO的质量为_______ ;CO2在相同状况下的体积为_______ 。
(4)将4g NaOH 溶解在10mL水中,再稀释成1L,从中取出10mL,这10mL溶液的物质 的量浓度为_______。
(5)已知ag氢气中含有b个氢原子,则阿伏加德罗常数的值可表示为 _______ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某晶体的晶胞结构为正三棱柱(如图所示),这种晶体中A、B、C三种微粒数目之比为

A. 2∶9∶4 B. 3∶9∶4
C. 1∶4∶2 D. 3∶8∶4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮元素的单质和常见的化合物在工、农业生产中用途广泛.
(1)工业上利用分离空气的方法得到氮气.空气各主要成分的沸点如下:
N2 | O2 | Ar | CO2 |
-196℃ | -183℃ | -186℃ | -78℃ |
现将空气深度冷却液化,然后缓慢升温,则最先分离出来的气体是____________;
(2)雷雨时空气中的N2转化为NO,生成物NO是______色的气体,________(填“易”或“难”)溶于水;NO在空气中很容易被氧化成NO2,NO2能与水发生化学反应. NO2与水反应的化学方程式为_______________________________;
(3)实验室可用固体NH4Cl与固体Ca(OH)2加热反应制取氨气.
①制取氨气的化学方程式为_____________________________;
②要制取标准状况下4.48L的氨气,至少需要称取固体NH4Cl的质量为______g;
(4)已知:4NH3+6NO![]() 5N2+6H2O化学研究性学习小组的同学在技术人员的指导下,按下列流程,探究不同催化剂对NH3还原NO反应的催化性能.
5N2+6H2O化学研究性学习小组的同学在技术人员的指导下,按下列流程,探究不同催化剂对NH3还原NO反应的催化性能.
![]()
将经催化反应后的混合气体,通过一定体积滴有酚酞的稀硫酸溶液.NH3与稀硫酸溶液反应的化学方程式为____________________________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用C、Mg和Al组成的混合物进行如下图所示实验。填写下列空白。
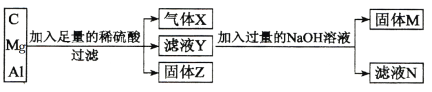
(1)气体X为 _________,固体Z为_____________。
(2)滤液Y中除H+外,还含有的阳离子为_________与__________;其中镁和稀硫酸反应的化学方程式为_________________________________________。
(3)滤液N中除Na2SO4和NaOH外,还含有的溶质为____________(填化学式);生成该物质的离子方程式为:________________________________。
(4)生成固体M的离子方程式为:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁和钴是两种重要的过渡元素。
(1)钴位于元素周期表第四周期Ⅷ族,其基态原子中未成对电子个数为___________。
(2)基态Fe3+的核外电子排布式___________
(3)铁氧体是一种磁性材料,工业上制备时常采用水解法,制备时常加入尿素(CO(NH2)2)、醋酸钠等碱性物质。尿素分子中所含非金属元素的电负性由大到小的顺序是___________,分子中σ键与π键的数目之比为___________。醋酸钠中碳原子的杂化类型___________。
(4)铁氧体也可使用沉淀法,制备时常加入氨(NH3)、联氨(N2H4)等弱碱,已知氨(NH3熔点:-77.8%℃、沸点:-33.5%℃),联氨(N2H4熔点:2℃、沸点:113.5°C)解释其熔沸点高低的主要原因______________________。
(5)Co(NH3)5BrSO4可形成两种钴的配合物,已知Co3+的配位数为6,为确定钻的配合物的结构,现对两种配合物进行如下实验:在第一种配合物溶液中加入硝酸银溶液产生白色沉淀,则第一种配合物的配体为___________。在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀。则第二种配合物的配体为___________。

(6)奥氏体是碳溶解在r-Fe中形成的一种间隙固溶体,无磁性,其晶胞为面心立方结构,如上图所示,则该物质的化学式为___________。若品体密度为dg·cm-3,则晶胞中最近的两个碳原子的距离为___________pm(阿伏加德罗常数的值用NA表示,写出简化后的计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2H2(g)+O2(g)→2H2O (g)+ 483.6 kJ,2H2(g)+O2(g)→2H2O (l)+ 571.6 kJ;图中示意正确的是
A.  B.
B. 
C.  D.
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是( )
A. 漂白粉露置在空气中失效:2ClO-+CO2+H2O===2HClO+CO32-
B. 银氨溶液中滴加过量的盐酸:Ag(NH3)2++2H+===Ag++2NH4+
C. 二氧化锰与浓盐酸共热制取氯气:MnO2+2Cl-+4H+![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
D. 用碱性NaClO溶液吸收冶金工业尾气中的NO2:ClO-+2NO2+H2O===Cl-+2NO3-+2H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某双原子分子构成的气体,其摩尔质量为32g/mol,该气体质量为16g,阿伏加德罗常数为NA,则:
(1)该气体的物质的量为________
(2)该气体在标准状况下的体积约为________
(3)该气体所含原子总数为________
(4)该气体的一个分子的质量为________
(5)该气体在标准状况下的密度约为________(保留两位小数)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com