
����Ŀ������ʵ������ܵó���Ӧ���۵���
ѡ�� | ʵ����������� | ʵ����� |
A | �ں� NaOH �� Mg(OH)2 ����Һ�еμ� CoCl2 ��Һ�������ۺ�ɫ���� | Ksp[Co(OH)2]��Ksp[Mg(OH)2] |
B | ������Һ��ͨ�� CO2��������ɫ��״���� | ԭ��Һ��һ������ SiO32�� |
C | ��������ˮ�м���̼��Ʒ�ĩ�����裬���� | ��ˮ��Ư���Ի���ǿ |
D | �� Fe �ۡ�Cu �۷ֱ�����ۻ�ϼ��ȣ��ֱ����� FeS��Cu2S | ��ԭ�ԣ�Fe��Cu |
A.AB.BC.CD.D
���𰸡�C
��������
A.NaOH��������CoCl2��Ӧֱ�����ɳ��������ܱȽ����ܵ���ʵ�Ksp����A����
B.��ɫ��״���ʿ���Ϊ������������ᣬ��ԭ��Һ�п��ܺ�SiO32��Ҳ���ܻ���AlO2-����B����
C. ��Cl2+H2O![]() HCl+HClO֪����ˮ��Ư������Ҫ��HClO�����ã����Լ���̼��Ʒ�ĩʹƽ�������ƶ�����ˮƯ������ǿ����C��ȷ��
HCl+HClO֪����ˮ��Ư������Ҫ��HClO�����ã����Լ���̼��Ʒ�ĩʹƽ�������ƶ�����ˮƯ������ǿ����C��ȷ��
D. SΪ�������������۽�����Ӧ���ɵͼ۽�����������ۺ�ͭ�۷ֱ����ۻ�ϼ��ȣ��ֱ�����FeS��Cu2S�����ܱȽ�Fe��Cu�Ļ�ԭ�ԣ���D����
��ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Bi��OH��3+3OH-+Cl2+Na+=NaBiO3+2C1-+3H2O����5NaBiO3+2Mn2++14H+=2MnO4-+5Bi3++5Na++7H2O�������ƶϲ���ȷ���ǣ� ��
A.��Ӧ���У�����10.45gBi3+����ʱת�Ƶ�����Ϊ0.5NA
B.�κ������£������������ԣ�C12��NaBiO3��MnO4-
C.NaBiO3�������ᷢ����Ӧ��NaBiO3+6H++2C1-=Bi3++Na++C12��+3H2O
D.��֪BiC13����Bi2O3����ˮ��Ũ�����Ũ����Ļ�����Ӧ��ȡ��˵��Bi3+���ܱ���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ϳɾ����������オ���Ե��л��߷��Ӳ������л���ѧ�о�����Ҫ����֮һ���۴�����ϩ����PVAc��ˮ�����ɵľ���ϩ����PVA���������������オ���ԣ�������������ȫ�����в����PVB���йغϳ�·����ͼ�����ַ�Ӧ�����Ͳ�����ȥ����
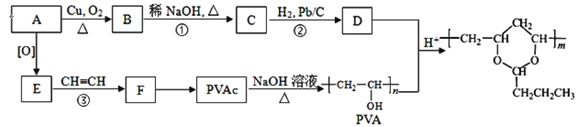
��֪����.RCHO+R��CH2CHO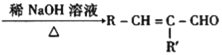 +H2O
+H2O
��.![]() ��R��R���ɱ�ʾ��������ԭ�ӣ�
��R��R���ɱ�ʾ��������ԭ�ӣ�
��.AΪ����һԪ������������������ԼΪ34.8%����ش�
��1��C�й����ŵ�����Ϊ_____���÷����������_____��ԭ�ӹ�ƽ�档
��2��D�뱽��ȩ��Ӧ�Ļ�ѧ����ʽΪ_____��
��3���۵ķ�Ӧ������____��
��4��PVAc�Ľṹ��ʽΪ____��
��5��д����F������ͬ�����ŵ�ͬ���칹��Ľṹ��ʽ____����дһ�֣���
��6������������Ϣ����ƺϳ�·����������Ϊԭ�ϣ��������Լ���ѡ���ϳ�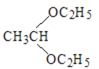 ��____��
��____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���̷���FeSO4��7H2O��������ԭ������ɫ������ҩ�ȣ��ڲ�ͬ�¶����ֽ�õ��������������������������֪SO3��һ����ɫ���壬�۵�16.8�棬�е�44.8�棬�����Լ���ˮ�Խ�Ũ����ǿ����Ư��ijЩ�л�Ⱦ�ϣ���Ʒ��ȡ��ش��������⣺
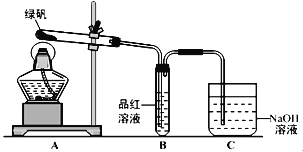
��1������ͬѧ������ͼ��ʾ��װ�ã�ͨ��ʵ������̷��ķֽ���װ��B�пɹ۲쵽��������_____________________________�������ɴ˵ó��̷��ķֽ�����к���SO2��װ��C��������_________________________��
��2������ͬѧ��Ϊ����ͬѧ��ʵ����۲��Ͻ�����Ϊ��Ҫ����ʵ�顣�Լ���ͬѧ����ʵ���Bװ�õ��Թܼ��ȣ�������ɫ��Ʒ����Һδ�ָ���ɫ�����֤���̷��ֽ�IJ�����__________������ĸ����
A������SO2 B�����ܺ�SO2 C��һ������SO3
��3������ͬѧ�������Ϸ����̷����ȷֽ������O2�ų���Ϊ�ˣ�����ͬѧѡ�ü���ͬѧ�IJ���װ�ú���ͼ����װ����Ƴ���һ�����̷��ֽ�������̬�����װ�ã�
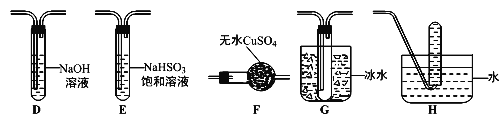
�ٱ���ͬѧ��ʵ��װ���У��������ӵĺ���˳��Ϊ_______________________��
����֤���̷��ֽ��������O2�ļ��鷽����________________________��
��4��Ϊ֤���̷��ֽ�����к����������IJ���������____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��S-�տ����Ƽ��ܱ����ʻ�ʢ����S-�տ��صķ��ӽṹ��ͼ�����й��ڸ�����˵����ȷ����

A.S-�տ����Ƽ�����������̼ԭ�Ӳ����ܴ���ͬһƽ����
B.1 mol S-�տ����Ƽ������ 4 mol Br2 �����ӳɷ�Ӧ
C.�� Cu �� Ag �������������������ܱ� O2 ����Ϊȩ
D.�û����ﲻ�ܷ����ۺϷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������������ȡ��κ͵��ʣ���һ����;�㷺�Ļ���ԭ�ϡ���������һ�ֹ㷺���ڵ��ӹ�ҵ ��ͨѶ�������Ҫ��������Ԫ��(31Ga)��Ԫ�����ڱ���λ�ڵ������� IIIA �壬��ѧ��������Ԫ�����ơ�
(1)��ͼ�ǵ���Ӧ���а� n(N2):n(H2)=1:3 Ͷ�Ϻ��� 200����400����600���£���Ӧ�ﵽƽ��ʱ��������� NH3�����ʵ���������ѹǿ�ı仯���ߡ�
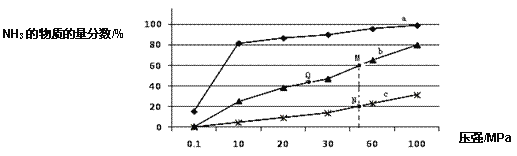
������ a ��Ӧ���¶���_____________��
�ڹ��ڹ�ҵ�ϳɰ��ķ�Ӧ������������ȷ����____________������ĸ����
A����ʱ����� NH3 ������� H2 ��ƽ��ת����
B��������������ԭ����һ����ø����·�����Ӧ
C����ͼ�� M��N��Q ��ƽ�ⳣ�� K �Ĵ�С��ϵ�� K(M) �� K(Q) >K(N)
��M ���Ӧ�� H2 ת������____________��
(2)��ҵ������ Ga �� NH3 �ϳɹ���뵼����ϵ�����(GaN)ͬʱ���������ɡ���Ӧ�У����� 3 mol H2 ʱ�ͻ�ų�30.8 kJ ���ȡ�
�ٸ÷�Ӧ���Ȼ�ѧ����ʽ��____________________��
�ڷ�Ӧ�Ļ�ѧƽ�ⳣ������ʽ��____________��
���ں��º��ݵ��ܱ���ϵ�ڽ����������淴Ӧ�������йر�����ȷ����____________��
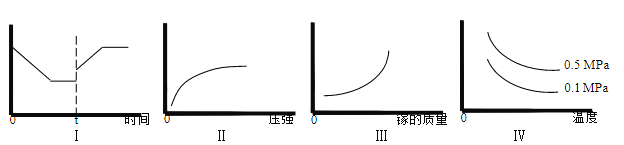
A��I ͼ�������������Ϊ����Ӧ���ʣ��� t ʱ�̸ı����������Ϊ����
B��II ͼ�������������Ϊ�ص�ת����
C��III ͼ�������������Ϊ��ѧ��Ӧ����
D����ͼ�������������Ϊ��ϵ�ڻ������ƽ����Է�������
�ܵ�����(GaN)�����ȶ������ܻ������ܽ����ȵ� NaOH ��Һ�У��÷�Ӧ�����ӷ���ʽ�ǣ�___________________��
(3)��һ�������Ͻ���ȫ�����ռ���Һ�еõ���Һ X����֪��
Al(OH)3 | Ga(OH)3 | |
��ʽ���볣�� Ka | 2��10�� 11 | 1��10�� 7 |
��ʽ���볣�� Kb | 1.3��10�� 33 | 1.4��10�� 34 |
�� X ��Һ�л���ͨ�� CO2����������������������____________��
(4)��ҵ���Ե�⾫���������ص�ԭ�����£��Դ��ᴿ�Ĵ��أ��ں� Zn��Fe��Cu ���ʣ�Ϊ�������Ըߴ���Ϊ�������� NaOH ˮ��ҺΪ�������Һ���ڵ���������ʹ�����������ܽ����������Һ����ͨ��ij������Ǩ�Ƽ� �������������������ŵ������ߴ��ء�
�ټ�֪����������˳��Ϊ��Zn2+<Ga3+< Fe2+<Cu2+����⾫����ʱ������ijɷ���____________��
��GaO2�� �������ŵ�ĵ缫����ʽ��___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ӦA(g)��B(g) ![]() 2C(g)��3D(g)�����ֲ�ͬ����µķ�Ӧ�������£����б�ʾ
2C(g)��3D(g)�����ֲ�ͬ����µķ�Ӧ�������£����б�ʾ
��Ӧ����������
A. v(A)��0.20mol��L��1��min��1 B. v(B)��0.30 mol��L��1��min��1
C. v(C)��0.40 mol��L��1��min��1 D. v(D)��0.50 mol��L��1��min��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ���������ֵ������˵���в���ȷ����
A.10g��������Ϊ46%���Ҵ�ˮ��Һ�к��е���ԭ������Ϊ1.2NA
B.NA��P4(![]() )��NA�����������Ĺ��ۼ���Ŀ֮��Ϊ1��1
)��NA�����������Ĺ��ۼ���Ŀ֮��Ϊ1��1
C.�����£�1 L pH��13��M(OH)2��Һ�к��е�OH����ĿΪ0.1NA
D.��0.4 mol HNO3��Ũ������������ͭ��Ӧ��ת�Ƶĵ���������0.2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ�������Ӧ�Ľ�����ȷ���ǣ� ��
ѡ�� | ʵ����� | ʵ������ | ���� |
A | ��Ũ��Ϊ0.1mol/LNaCl��KI���Һ����μ���AgNO3��Һ | ���ֻ�ɫ���� | �ܽ��ԣ�AgCl>AgI |
B | ��������NaOH���Ҵ���Һ���ȣ����������ͨ�����Ը��������Һ�� | ��Һ��ɫ��ȥ | ֤������ϩ���� |
C | ��X����Һ�е���ŨNaOH��Һ���������ɫʯ����ֽ���ڹܿ� | ���������� | X��Һ����NH4+ |
D | ��SO2����ͨ��Ba(NO3)2��Һ | ������ɫ���� | ����ΪBaSO3 |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com