
| A. | 原子半径呈周期性变化 | |
| B. | 元素的化合价呈周期性变化 | |
| C. | 元素原子的核外电子排布呈周期性变化 | |
| D. | 第一电离能呈周期性变化 |
分析 根据随原子序数的递增,原子的结构呈现周期性的变化而引起元素的性质的周期性变化来解答.
解答 解:A、因元素的原子半径是元素的性质,不能解释元素性质的周期性变化,故A错误;
B、因元素的化合价属于元素的性质,则不能解释元素性质的周期性变化,故B错误;
C、因原子的核外电子排布中电子层数和最外层电子数都随原子序数的递增而呈现周期性变化,则引起元素的性质的周期性变化,故C正确;
D、因第一电离能并不是完全呈周期性变化,则不能解释元素性质的周期性变化,故D错误;
故选:C.
点评 本题考查元素周期律的实质,明确原子的结构与性质的关系、元素的性质有哪些是解答的关键,并注意不能用元素本身的性质来解释元素性质的周期性变化.


科目:高中化学 来源: 题型:解答题
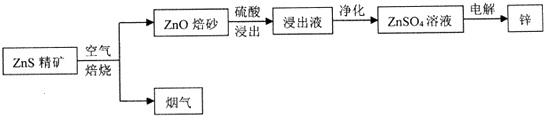
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
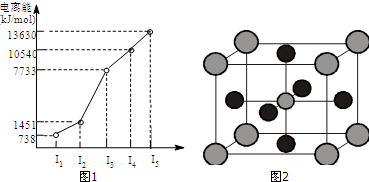
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加催化剂 | B. | 增大压强 | C. | 充入N2 | D. | 降低温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氮分子为非极性分子 | |
| B. | 在灯泡中充入氮气可防止钨丝被氧化 | |
| C. | 氮元素比磷元素非金属性强,所以硝酸比磷酸酸性强 | |
| D. | 氮分子中有2个σ键1个π键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数:a>b>c>d | |
| B. | 离子半径:A2+>B+>C2->D- | |
| C. | 单质还原性:B>A,单质氧化性:D>C | |
| D. | 离子还原性:C2->D-,离子氧化性:B+>A2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解结束后,在阳极底部会有阳极泥产生,主要成分是铁、金和银 | |
| B. | 电解结束后,溶液中Cu2+浓度变大 | |
| C. | 纯铜作阳极,粗铜作阴极,硫酸铜为电解质溶液 | |
| D. | 粗铜作阳极,纯铜作阴极,硫酸铜为电解质溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com