
| A. | C在O2充足时,发生的反应主要是放热反应 | |
| B. | 煤燃烧时吹入的氧气越多越好 | |
| C. | CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO这一反应属于吸热反应 | |
| D. | 煤燃烧时,反应物自身总能量高于生成物总能量,所以放出热量 |
分析 A.燃烧都是放热反应;
B.煤燃烧时吹入的氧气越多,气体流通带走的热量多;
C.碳与二氧化碳的反应是吸热反应;
D.煤燃烧为放热反应,反应物总能量和高于生成物总能量和.
解答 解:A.木炭在氧气中的燃烧,属于燃烧反应,是放热反应,故A正确;
B.煤燃烧时吹入的氧气越多,气体流通带走的热量越多,所以不是煤燃烧时吹入的氧气越多越好,故B错误;
C.碳与二氧化碳的反应是吸热反应,故C正确;
D.当反应物的能量高于生成物总能量时,反应是放热反应,煤燃烧时,反应物自身总能量高于生成物总能量,所以放出热量,故D正确;
故选ACD.
点评 本题考查化学反应能量的变化,题目难度不大,注意有关概念的理解,学习中注意基础知识的积累.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用A装置,若A为浓醋酸、B为碳酸钠(粉状)、C为苯酚钠溶液,一定能验证醋酸、碳酸、苯酚酸性的强弱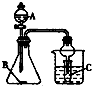 | |
| B. | 利用B装置可以完成乙酸乙酯制取实验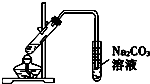 | |
| C. | 利用C装置可以完成石油蒸馏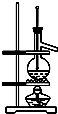 | |
| D. | 利用D装置可以完成实验室制乙烯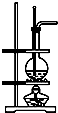 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 延展性 | B. | 导电性 | C. | 弹性 | D. | 导热性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子半径:Q>W>Z | |
| B. | Q的氢化物的水溶液一定具有强酸性 | |
| C. | X、Y、Q可同时存在同一离子化合物中 | |
| D. | 单质的沸点:W>Q>Z |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | ①⑤⑥ | B. | ②④⑦ | C. | ①⑥⑦ | D. | ⑤⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 硝基还原为氨基:
硝基还原为氨基: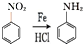
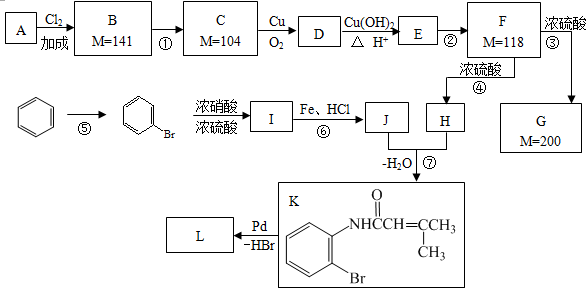
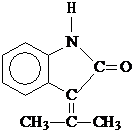 .
.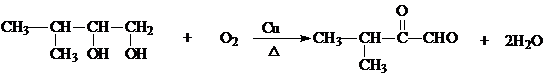 .
. .
.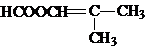 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
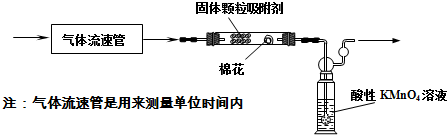
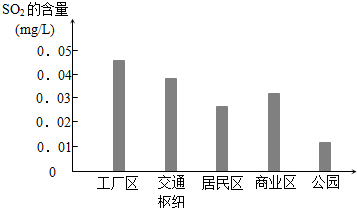
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com