

分析 利用微热法可检验气密性,a为分液漏斗,A中发生2NaNO2+(NH4)2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2N2↑+Na2SO4+4H2O,B中缓冲瓶可防止倒吸,因Mg与氮气、氧气均反应,可知C中硫酸亚铁除去氧气,D中浓硫酸干燥氮气,E中Mg与氮气反应生成氮化镁,F可防止G中液体倒吸进入E,G中硫酸亚铁可除去空气中的氧气,防止进入E中,且氮化镁与水反应、Mg与盐酸反应,以此来解答.
解答 解:(1)检查装置气密性的方法是微热b,这时G中有气泡冒出,停止加热冷却后,G中插在溶液里的玻璃管形成一段水柱,则气密性良好,由图可知,a为分液漏斗,
故答案为:微热b,这时G中有气泡冒出,停止加热冷却后,G中插在溶液里的玻璃管形成一段水柱,则气密性良好;分液漏斗;
(2)NaNO2和(NH4)2SO4反应制备氮气的化学方程式为2NaNO2+(NH4)2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2N2↑+Na2SO4+4H2O,
故答案为:2NaNO2+(NH4)2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2N2↑+Na2SO4+4H2O;
(3)C的作用是除去氧气(及氮氧化物),不能将C和D的位置对调,因对调后无法除去水蒸气,
故答案为:除去氧气(及氮氧化物); 不能,对调后无法除去水蒸气;
(4)E中发生反应的化学方程式为N2+3Mg$\frac{\underline{\;\;△\;\;}}{\;}$Mg3N2,故答案为:N2+3Mg$\frac{\underline{\;\;△\;\;}}{\;}$Mg3N2;
(5)用化学方法确定是否有氮化镁生成,并检验是否含有未反应的镁,实验操作及现象为取少量产物于试管中,加入少量蒸馏水,试管底部有沉淀生成,可闻到刺激性氨味(把湿润的红色石蕊试纸放在管口,试纸变蓝),证明产物中含有氮化镁;弃去上清液,加入盐酸,若观察到有气泡产生,则证明产物中含有未反应的镁,
故答案为:取少量产物于试管中,加入少量蒸馏水,试管底部有沉淀生成,可闻到刺激性氨味(把湿润的红色石蕊试纸放在管口,试纸变蓝),证明产物中含有氮化镁;弃去上清液,加入盐酸,若观察到有气泡产生,则证明产物中含有未反应的镁.
点评 本题考查物质的制备实验,为高频考点,把握实验装置的作用、物质的性质、发生的反应、混合物分离提纯为解答的关键,侧重分析与实验能力的考查,注意物质的制备及检验方法,题目难度不大.


 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径呈周期性变化 | |
| B. | 元素的化合价呈周期性变化 | |
| C. | 第一电离能呈周期性变化 | |
| D. | 元素原子的核外电子排布呈周期性变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
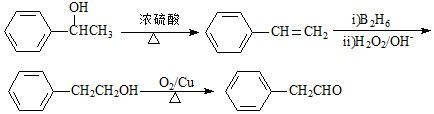
 . G的一种合成路线如下:
. G的一种合成路线如下:


 ;X生成Y的反应类型是消去反应.
;X生成Y的反应类型是消去反应.
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 用如图装置完成下列实验,不需要试管①的是(内盛有相应的除杂试剂)就能达到实验目的是
用如图装置完成下列实验,不需要试管①的是(内盛有相应的除杂试剂)就能达到实验目的是| 实验目的 | ②中的试剂 | |
| A | 检验碳与浓硫酸反应产生的气体中含有二氧化碳 | 澄清石灰水 |
| B | 用碳酸钙与盐酸反应产生的气体验证碳酸的酸性强于苯酚 | 苯酚钠溶液 |
| C | 验证乙醇在浓硫酸作用下发生消去反应产生的气体为不饱和烃 | 酸性高锰酸钾溶液 |
| D | 验证石蜡油在碎瓷片上受热分解产生的气体中含有不饱和烃 | 溴的四氯化碳溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 84消毒液、高温等方法均可有效杀死H7N9禽流感病毒 | |
| B. | 地沟油不可食用,但可以和乙醇反应制备生物柴油 | |
| C. | 化石燃料燃烧产生大量的CO2是造成酸雨的主要原因,酸雨、温室效应和臭氧空洞是世界三大环境问题 | |
| D. | 目前使用的化石能源实际上是地球在远古时代为我们储存的太阳能 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质硅是良好的半导体材料 | B. | 光导纤维的主要成分是硅酸盐 | ||
| C. | 硅是构成矿物与岩石的主要元素 | D. | 玻璃、水泥、陶瓷都属于硅酸盐产品 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com