
| A. | ①② | B. | ③ | C. | ③④ | D. | ④ |
分析 醋酸钠是弱酸强碱盐,醋酸根离子在水溶液中水解显碱性,配制CH3COO-与Na+离子物质的量浓度之比为1:1的溶液需要加入抑制醋酸根离子水解的试剂.
解答 解:①醋酸根离子在水溶液中水解显碱性,加入盐酸促进醋酸根离子的水解,配制CH3COO-与Na+离子物质的量浓度之比小于1:1,故错误;
②适量的NaCl固体,钠离子浓度增大,配制CH3COO-与Na+离子物质的量浓度之比小于1:1的溶液,故错误;
③醋酸钠中醋酸根离子水解生成醋酸,加入适量的醋酸,会抑制醋酸根离子水解,所以溶液中Na+的浓度与CH3COO-的浓度比接近1:1,故正确;
④加入适量的醋酸钠,会使得醋酸根离子浓度、钠离子浓度都增加,但是醋酸根离子的水解程度减小,所以醋酸根离子浓度增加的程度大,所以溶液中Na+的浓度与CH3COO-的浓度比小于1:1,故错误.
故选:B.
点评 本题考查了盐类水解平衡的影响因素分析判断,注意阴离子和阳离子的浓度变化,题目较简单.


科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ③④⑤ | C. | ②③⑤ | D. | ②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,44.8L乙醇中含有的分子数目为0.2NA | |
| B. | 常温常压下,6.4gSO2中含有的氧原子数目为0.2NA | |
| C. | 1L0.1mol•L-1K2CO3溶液中含有的钾离子数目为0.1NA | |
| D. | 100mL1.0mol•L-1FeCl3溶液与足量铜反应,转移的电子数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氢气是一种清洁能源,氢气的制取是氢能源利用领域的研究热点;氢气也是重要的化工原料.
氢气是一种清洁能源,氢气的制取是氢能源利用领域的研究热点;氢气也是重要的化工原料.| 时间/min | 20 | 40 | 60 | 80 |
| n(O2)/mol | 0.0010 | 0.0016 | 0.0020 | 0.0020 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
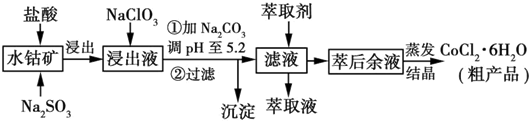
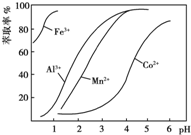
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com