
【题目】二氧化碳的捕集和转化是科学研究中的热点问题。我国科研人员提出了以Ni/Al2O3为催化剂,由 CO2(g)和H2(g)转化为CH4(g)和H2O(g)的反应历程,其示意图如下:
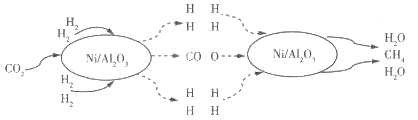
(1)该可逆反应的化学方程式为_________。使用催化剂Ni/Al2O3_________ (填“能”或“不能”)提髙CO2的平衡转化率。
(2)300℃下,在一恒容密闭容器中充入一定量的CO2与H2,发生上述反应,一段时间后反应达平衡,若其他条件不变,温度从300℃升至500℃,反应重新达到平衡时,H2的体积分数增加。下列说法错误的是_________(填标号)。
A.该反应的![]()
B.平衡常数大小:![]()
C.300℃下,减小![]() 的值,
的值,![]() 的平衡转化率升高
的平衡转化率升高
D.反应达到平衡时化![]()
(3)在一定条件下,反应体系中CO2的平衡转化率a( CO2)与L和X的关系如图所示,L和X表示温度或压强。
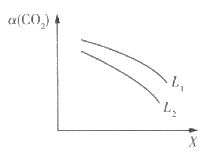
①X表示的物理量是___________。
②L1_____________L2(填“<”“>”),判断理由是______________________________________。
(4)向1 L恒容密闭容器中加入4.0 mol H2(g),1.0 mol CO2,控制条件(催化剂为 Ni/AI2O3、温度为T1)使之发生上述反应,测得容器内气体的压强随时间的变化如图所示。
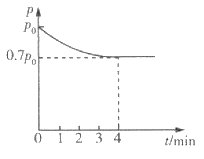
①4 min时CO2的转化率为___________。
②T1温度下该反应的化学平衡常数为___________。
【答案】CO2(g)+4H2(g)![]() CH4(g)+2H2O(g) 不能 BC 温度 > 该反应为气体分子数减小的反应,其他条件一定时,增大压强,平衡右移,CO2的平衡转化率升髙 75% 6.75
CH4(g)+2H2O(g) 不能 BC 温度 > 该反应为气体分子数减小的反应,其他条件一定时,增大压强,平衡右移,CO2的平衡转化率升髙 75% 6.75
【解析】
(1)根据图示书写该可逆反应的化学方程式;催化剂只能加快反应的速率,不能提高CO2的平衡转化率;
(2)A.温度从300℃升至500℃反应重新达到平衡时,H2的体积分数增加,根据温度对平衡移动的影响分析;
B.正反应为放热反应,升高温度平衡逆向移动,平衡常数减小;
C.减小![]() 的值,CO2的含量增大,据此分析;
的值,CO2的含量增大,据此分析;
D.反应达到平衡时,反应速率之比等于化学计量数之比;
(3)①根据方程式 CO2(g) +4H2(g)![]() CH4(g) +2H2O(g)及反应的
CH4(g) +2H2O(g)及反应的![]() H<0 可知结合图像转化率的变化分析判断影响因素;
H<0 可知结合图像转化率的变化分析判断影响因素;
②结合题图及①中的分析判断;
(4)由题图可知,4 min时反应体系处于平衡状态,此时压强为0. 7p0,结合气体压强之比等于物质的量之比,列出三段式计算CO2的转化率及反应平衡常数。
(1)由题意可知该可逆反应的化学方程式为CO2(g)+4H2(g)![]() CH4(g)+2H2O(g) +2H2O(g),催化剂只能加快反应的速率,不能提高CO2的平衡转化率;
CH4(g)+2H2O(g) +2H2O(g),催化剂只能加快反应的速率,不能提高CO2的平衡转化率;
(2)A.对于该可逆反应,若其他条件不变, 温度从300℃升至500℃反应重新达到平衡时,H2的体积分数增加,说明正反应为放热反应,故A正确;
B.正反应为放热反应,因此![]() ,故B错误;
,故B错误;
C.减小![]() 的值,CO2的平衡转化率降低,故C错误;
的值,CO2的平衡转化率降低,故C错误;
D.反应达到平衡时,![]() ,故D正确;
,故D正确;
答案选BC;
(3)①根据方程式 CO2(g) +4H2(g)![]() CH4(g) +2H2O(g)及反应的
CH4(g) +2H2O(g)及反应的![]() H<0 可知,其他条件一定时,升温,CO2的平衡转化率降低,其他条件一定时,加压,CO2的平衡转化率升高,则X表示的物理量是温度;
H<0 可知,其他条件一定时,升温,CO2的平衡转化率降低,其他条件一定时,加压,CO2的平衡转化率升高,则X表示的物理量是温度;
②L表示压强,结合题图及上述分析,可知L1>L2;
(4)①由题图可知,4 min时反 应体系处于平衡状态,此时压强为0. 7p0,设发生反应的CO2为x mol,列出三段式:
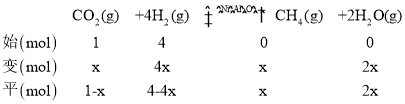
根据恒温恒容条件下,气体压强之比等于物质的量之比得出![]() ,解得 x=0.75,则CO2的转化率为
,解得 x=0.75,则CO2的转化率为![]() ;
;
②平衡常数![]() 。
。


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】我国科学家最近成功合成了世界上首个五氮阴离子盐(N5)6(H3O)3(NH4)4Cl(用R代表)。回答下列问题:
(1)氮原子价层电子的轨道表达式(电子排布图)为_____________。
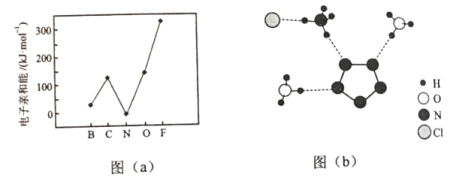
(2)元素的基态气态原子得到一个电子形成气态负一价离子时所放出的能量称作第一电子亲和能(E1)。第二周期部分元素的E1变化趋势如图(a)所示,其中除氮元素外,其他元素的E1自左而右依次增大的原因是___________;氮元素的E1呈现异常的原因是__________。
(3)经X射线衍射测得化合物R的晶体结构,其局部结构如图(b)所示。
①从结构角度分析,R中两种阳离子的相同之处为_________,不同之处为__________。(填标号)
A.中心原子的杂化轨道类型 B. 中心原子的价层电子对数
C.立体结构 D.共价键类型
②R中阴离子N5中的σ键总数为________个。分子中的大π键可用符号![]() 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为![]() ),则N5—中的大π键应表示为____________。
),则N5—中的大π键应表示为____________。
③图(b)中虚线代表氢键,其表示式为(NH4+)NH…Cl、____________、____________。
(4)R的晶体密度为d g·cm3,其立方晶胞参数为a nm,晶胞中含有y个单元,该单元的相对质量为M,则y的计算表达式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物F是从我国特产植物中提取的一种生物碱,其人工合成路线如图:
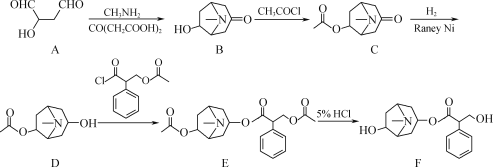
(1)A中含氧官能团的名称为___和___。
(2)C→D的反应类型为___。
(3)E→F的过程中,会有副产物X(分子式为C8H15NO2)生成,写出X的结构简式:___。
(4)C的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:__。
①分子中有醚键;
②能与FeCl3溶液发生显色反应,能与盐酸反应;
③有4种不同化学环境的氢且数目比为9∶2∶2∶2。
(5)已知:R—O—R′+2HBr![]() R—Br+R′—Br十H2O(R、R′表示烃基)。
R—Br+R′—Br十H2O(R、R′表示烃基)。
写出以![]() 、CH3NH2和CO(CH2COOH)2为原料制备
、CH3NH2和CO(CH2COOH)2为原料制备![]() 的合成路线流程图___(无机试剂任用,合成路线流程图示例见本题题干)。
的合成路线流程图___(无机试剂任用,合成路线流程图示例见本题题干)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(Ⅰ)、如图为一“铁链”图案,小明在图案上分别写了H2、CO2、Na2O、NaCl、FeCl3五种物质,图中相连的两种物质均可归属为一类,相交部分A、B、C、D为其相应的分类依据代号。请回答下列问题:
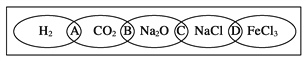
(1)请将分类依据代号填入相应的括号内:
(______)两种物质都不是电解质
(______)两种物质都是盐
(2)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入饱和的图中某种物质M的溶液加热至呈红褐色。
①物质M的化学式为________________。
②证明有红褐色胶体生成的实验操作是________________________________________。
(Ⅱ)反应:A.2F2+2H2O=4HF+O2↑; B.2Na+2H2O=2NaOH+H2↑;
C.CaO+H2O=Ca(OH)2; D.2H2O=2H2↑+O2↑。
其中水是氧化剂的是______,水是还原剂的是________。(填序号)
(Ⅲ)反应:3Cu + 8HNO3 = 3Cu(NO3)2+2NO↑+4H2O,还原剂与氧化剂的物质的量之比:_______,当有0.6mol电子转移时。生成的NO在标准状况的体积为________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是
A.由乙醇和乙酸生成乙酸乙酯的反应属于取代反应
B.煤中含有苯、甲苯和粗氨水,可通过干馏得到
C.甲苯和乙苯分子内共平面的碳原子数最多均为7
D.![]() 的同分异构体有7种(不考虑立体异构)
的同分异构体有7种(不考虑立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】太阳能的开发利用在新能源研究中占据重要地位,单晶硅太阳能电池片在加工时,一般掺杂微量的铜、钴、硼、镓、硒等。回答下列问题:
(1)基态二价铜离子的电子排布式为______,已知高温下Cu2O比CuO更稳定,试从核外电子排布角度解释______。
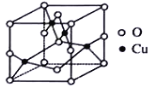
(2)铜的某种氧化物晶胞如图,该晶胞中阴离子的个数为_________。
(3)铜与(SCN)2反应生成Cu(SCN)2,中心体为___________,HSCN结构有两种,硫氰酸(H-S-C≡N)的沸点低于异硫氰酸(H-N=C=S)的原因是_________。
(4)BF3能与NH3反应生成BF3·NH3。B与N之间形成配位键,氮原子提供_____,第二周期元素中,电离能介于B和N之间的元素有_______个。
(5)如图EMIM+离子中,碳原子的杂化方式是___________。分子中的大π键可用符号πnm表示,其中n代表参与形成大π键的原子数,m代表参与形成大π键的电子数(如苯分子中的大π键可表示为π66),则EMM+离子中的大π键应表示为___________。
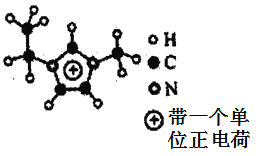
(6)如图六方氮化硼晶体结构与石墨晶体相似,则六方氮化硼晶体中层间的相互作用为___________。六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构、硬度与金刚石相似,其晶胞如图,晶胞边长为361.5pm,立方氮化硼的密度是___________g·cm-3(只列算式,![]() 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工业流程中,进入反应塔的混合气体中NO和O2的物质的量分数分別为0.10和0.06,发生化学反应2NO(g)+O2(g) ![]() 2NO2(g),在其他条件相同时,测得实验数据如下表:
2NO2(g),在其他条件相同时,测得实验数据如下表:
压强/(×105Pa) | 温度/℃ | NO达到所列转化率需要时间/s | ||
50% | 90% | 98% | ||
1.0 | 30 | 12 | 250 | 2830 |
90 | 25 | 510 | 5760 | |
8.0 | 30 | 0.2 | 3.9 | 36 |
90 | 0.6 | 7.9 | 74 | |
根据表中数据,下列说法正确的是
A.升高温度,反应速率加快
B.增大压强,反应速率变慢
C.在1.0×105 Pa、90℃条件下,当转化率为98%时反应已达平衡
D.若进入反应塔的混合气体为a mol,反应速率以![]() 表示,则在8.0×105Pa、30℃条件下,转化率从50%增至90%时段NO的反应速率为
表示,则在8.0×105Pa、30℃条件下,转化率从50%增至90%时段NO的反应速率为![]() mols-1
mols-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.澄清石灰水与稀盐酸反应:Ca(OH)2+2H+=Ca2++2H2O
B.氯气通入到FeCl2溶液中:Fe2++Cl2=Fe3++2Cl-
C.稀硫酸与氢氧化钡溶液反应:H++OH-+Ba2++![]() =H2O+BaSO4↓
=H2O+BaSO4↓
D.碳酸氢钠溶液与氢氧化钾反应:HCO3-+OH-=H2O+![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有八种短周期主族元素x、y、z、d、e、f、g、h,其中x、y、d、f随着原子序数的递增,其原子半径的相对大小、最高正价或最低负价的变化如图1所示。z、e、g、h的最高价氧化物对应的水化物溶液(浓度均为0.01mol/L)的pH与原子序数的关系如图2所示。
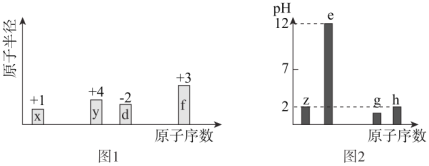
根据上述信息进行判断,并回答下列问题:
(1)g在元素周期表中的位置是______;
(2)比较d、e、f的简单离子半径大小为 < < (用离子符号表示)______;y、h的最高价氧化物对应水化物酸性较强的是______ (用化学式表示);
(3)下列可作为比较c和f金属性强弱的依据是______;
①测同温同压同浓度相应氯化物水溶液的pH
②测两种元素单质的硬度和熔、沸点
③比较单质作还原剂时失去的电子数目的多少
④比较两种元素在化合物中化合价的高低
⑤比较单质与同浓度盐酸反应的难易程度
(4)由上述元素中的y、z、e组成的某剧毒化合物eyz不慎泄露时,消防人员通常采用喷洒过氧化氢溶液的方式处理,以减少污染。反应生成一种酸式盐和一种气体,二者的水溶液均呈碱性,该反应的化学方程式为______。已知eyz含有Z2分子中类似的化学键,写出化合物eyz的电子式___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com