
在标准状况下15 g CO与CO2的混合气体,体积为11.2 L。则:
(1)混合气体的密度是____________________________________________________。
(2)混合气体的平均摩尔质量是____________________________________________。
(3)CO2和CO的体积之比是______________________________________________。
(4)CO的体积分数是____________________________________________________。
(5)CO2和CO的质量之比是______________________________________________。
(6)CO的质量分数是____________________________________________________。
(7)混合气体中所含氧原子的物质的量是___________________________________。
(8)混合气体中所含碳原子的物质的量是___________________________________。
答案 (1)1.339 g·L-1 (2)30 g·mol-1 (3)1∶7 (4)87.5% (5)11∶49 (6)81.7% (7)0.562 5 mol (8)0.5 mol
解析 (1)密度=质量/体积=15 g/11.2 L=1.339 g·L-1。
(2)解法一:n= =0.5 mol,M=m/n=15 g/0.5 mol=30 g·mol-1。
=0.5 mol,M=m/n=15 g/0.5 mol=30 g·mol-1。
解法二:M=ρ·Vm=1.339 g·L-1×22.4 L·mol-1=30 g·mol-1。
(3)根据阿伏加德罗定律:体积之比=物质的量之比,最简单的方法是用十字交叉法计算:

n(CO2)/n(CO)=1/7。
(4)CO的体积分数=CO的物质的量分数=7÷8×100%=87.5%。
(5) =
=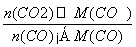 =
=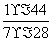 =11∶49。
=11∶49。
(6)CO的质量分数= ×100%=81.7%。
×100%=81.7%。
(7)n(O)=2n(CO2)+n(CO)=2×0.5 mol×1/8+0.5 mol×7/8=0.562 5 mol。
(8)n(C)=n(CO2)+n(CO)=0.5 mol。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
向x mL 2.0 mol/L的盐酸中投入a g镁铝合金,金属完全溶解,再加入y mL 1.0 mol/L的NaOH溶液,沉淀达到最大值,且质量为(a+1.7)g,则下列说法不正确的是( )
A.x=2y
B.镁铝合金与盐酸反应时转移电子的数目为0.1NA
C.镁铝合金与盐酸反应产生H2的体积在常温常压下大于1.12 L
D.a的取值范围为0.9 g<a<1.2 g
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值。下列说法正确的是 ( )
A.1 L 1 mol·L-1的NaClO溶液中含有ClO-的数目为NA
B.78 g苯含有C===C双键的数目为3NA
C.常温常压下,14 g由N2与CO组成的混合气体含有的原子数目为NA
D.标准状况下,6.72 L NO2与水充分反应转移的电子数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
将a g二氧化锰粉末加入c L b mol·L-1的浓盐酸中加热完全溶解,反应中转移电子d个,设NA为阿伏加德罗常数的值,下列叙述正确的是 ( )
A.可以收集到氯气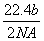 L
L
B.反应后溶液中的Cl-数目为
C.NA可表示为
D.反应后溶液中的H+数目为bc-2d
查看答案和解析>>
科目:高中化学 来源: 题型:
现有一瓶乙二醇和丙三醇的混和物,已知它们的性质如下表,据此,将乙二醇和丙三醇互相分离的最佳方法是
| 物质 | 分子式 | 熔点℃ | 沸点℃ | 密度(g/cm3) | 溶解性 |
| 乙二醇 | C2H6O2 | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
| 丙三醇 | C3H8O3 | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |
A.萃取法 B. 结晶法 C.分液法 D.蒸馏法
查看答案和解析>>
科目:高中化学 来源: 题型:
利用下列实验装置进行的相应实验,不能达到实验目的的是
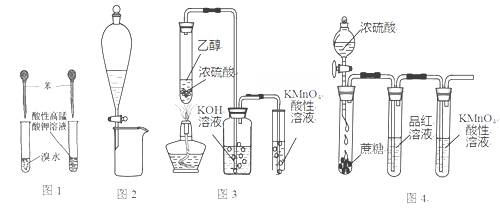
A.图1验证苯中是否有碳碳双键
B.图2所示装置可分离CH3CH2OH和CCl4混合液
C.图3所示装置可制取乙烯并验证其易被氧化
D.图4所示装置可说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期主族元素W、X、Y、Z位于同一周期,且原子序数依次增大。W、X是金属元素,Y、Z是非金属元素,W、X的最高价氧化物对应的水化物可以相互反应,Y的最外层电子数是核外电子层数的2倍。下列说法正确的是
A.W2Y溶液显中性
B.W与Z形成的化合物中不含有离子键
C.1mol元素Z的单质与足量的W的最高价氧化物对应的水化物的溶液反应,转移1mol电子
D.W、X的单质通常是电解其氧化物得到
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25℃时,下列物质的电离常数大小有如下顺序:
H2SO3(一级电离)>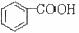 >HSO3->
>HSO3->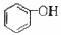 (苯酚,溶于水呈酸性)
(苯酚,溶于水呈酸性)
水杨酸(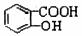 )与亚硫酸钠溶液反应,可能生成的物质是
)与亚硫酸钠溶液反应,可能生成的物质是
A.  B. SO2 C. NaHSO3 D.
B. SO2 C. NaHSO3 D. 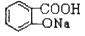
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com