
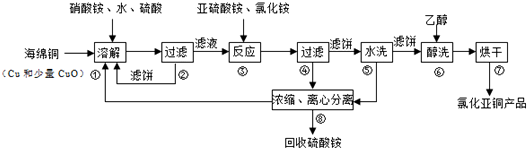
���� ������������������Ӿ��������ԣ�����������ͭ����Ҫ�ɷ���Cu������CuO����������ͭ�����˺�����Һ�м���������立���������ԭ��Ӧ����CuCl������2Cu2++SO32-+2Cl-+H2O=2CuCl+SO42-+2H+���õ���CuCl��������ϴ��ˮϴ�������Ҵ�ϴ�ӣ��ɿ��ٳ�ȥ��������ˮ�֣���ֹˮ�⡢����������ڡ��ܡ��ݡ��Ҫ���й�Һ���룬���ݻ�ϵ�ˮ���Խ��з��룬û�з�����ѧ�仯���������Ļ��Լ���ʽѹ�˻����Եõ��˱����Ȼ���ͭ���Ȼ�������Fe3++CuCl�TFe2++Cu2++Cl-������K2Cr2O7��Һ������6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O����Ϲ�ϵʽ�����⣮
��� �⣺������������������Ӿ��������ԣ�����������ͭ����Ҫ�ɷ���Cu������CuO����������ͭ�����˺�����Һ�м���������立���������ԭ��Ӧ����CuCl������2Cu2++SO32-+2Cl-+H2O=2CuCl+SO42-+2H+���õ���CuCl��������ϴ��ˮϴ�������Ҵ�ϴ�ӣ���ɵõ��Ȼ���ͭ��
��1������������������������Ӿ��������ԣ�������Cu����CuSO4��Cu2+���ܽ��¶�Ӧ������60-70�棬ԭ�����¶ȵ��ܽ��ٶ������¶ȹ�����ηֽ⣬
�ʴ�Ϊ��CuSO4��Cu2+���¶ȵ��ܽ��ٶ������¶ȹ�����ηֽ⣻
��2������ڡ��ܡ��ݡ��Ҫ���й�Һ���룬���ݻ�ϵ�ˮ���Խ��з��룬û�з�����ѧ�仯���������Ļ��Լ���ʽѹ�˻����Եõ��˱���
�ʴ�Ϊ��BD��
��3��ͭ������������立���������ԭ��Ӧ����CuCl������2Cu2++SO32-+2Cl-+H2O=2CuCl+SO42-+2H+���ʴ�Ϊ��2Cu2++SO32-+2Cl-+H2O=2CuCl+SO42-+2H+��
��4�������̿�֪������ϴ��ˮϴ��õ�����泥���Ӧ�������ᣬΪ��ֹCuCl�ܽ⣬���ܼ���������������ᣬҲ���ܼ������ᣬ��ֹ���������ʣ�
�ʴ�Ϊ�����
��5�������Ϊ��ϴ�����Ҵ��е�ͣ��ӷ��������Ҵ�ϴ�ӣ��ɿ��ٳ�ȥ��������ˮ�֣���ֹˮ�⡢������
�ʴ�Ϊ����ϴ�����ڼӿ�ȥ��CuCl����ˮ�ַ�ֹ��ˮ��������
��6���Ȼ���ͭ���Ȼ�������Fe3++CuCl�TFe2++Cu2++Cl-������K2Cr2O7��Һ������6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O��
��Ӧ�Ĺ�ϵʽΪ6CuCl��6Fe2+��Cr2O72-��
6 1
n ab��10-3mol
n=6ab��10-3mol��
m��CuCl��=99.5g/mol��6ab��10-3mol=0.597abg��
����Ʒ��CuCl����������Ϊ$\frac{0.597ab}{m}$��100%��
�ʴ�Ϊ��$\frac{0.597ab}{m}$��100%��
���� ���⿼���Ʊ�ʵ�鷽������ƣ�Ϊ��Ƶ���㣬��Ŀ����ѧ���Ķ���ȡ��Ϣ�����������û�ѧ���������ԭ�ζ���Ӧ�õȣ�������ѧ���ķ���������ʵ�������ͼ��������Ŀ��飬ע��������ʵ������Լ���Ӧ���̣��Ѷ��еȣ�ע�⣨6�������ù�ϵʽ�ļ��㣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | Pb2+ | Ca2+ | Fe3+ | Mn2+ |
| ����ǰŨ��/��mg•L-1�� | 0.100 | 29.8 | 0.12 | 0.087 |
| ������Ũ��/��mg•L-1�� | 0.004 | 22.6 | 0.04 | 0.053 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
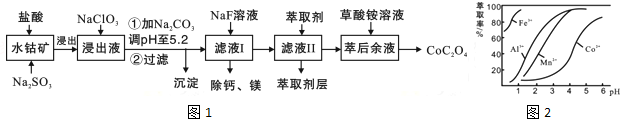
| ������ | Fe��OH��3 | Fe��OH��2 | Co��OH��2 | Al��OH��3 | Mn��OH��2 |
| ��ȫ������pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������ָ����Ԫ�صĻ����� | B�� | ������ᡢ��ζ�����Ԫ�� | ||
| C�� | ����������һ���ǽ��������� | D�� | ����������һ���Ƿǽ��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڢۢܢߢ� | B�� | �ڢۢܢޢ� | C�� | �ۢܢޢߢ� | D�� | �٢ڢۢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
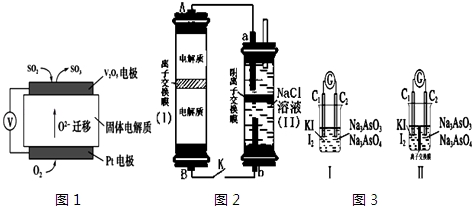
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Թ��е�ͭ��Ũ������ȣ������Թܵײ��а�ɫ���岢������������ɫ���ʣ��˰�ɫ����Ϊ����ͭ����ɫ����Ϊ����ͭ | |
| B�� | SO2ͨ��������Fe��NO3��3ϡ��Һ�У���Һ���ػ�ɫ��Ϊdz��ɫ���������ֱ���ػ�ɫ��˵�������ԣ�HNO3��ϡ���Fe3+ | |
| C�� | ����һ�����ʵ���Ũ����Һʱ����Ũ��ƫ�ͣ���������������Һ���õ�����ƿ����δ���� | |
| D�� | Ũ�����ڹ��������±�ƣ�˵��Ũ����ȶ������ɵ���ɫ����������Ũ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com