
【题目】若往20mL 0.01molL﹣l HNO2(弱酸)溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如图所示,下列有关说法不正确的是( ) 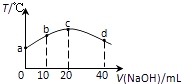
A.HNO2的电离平衡常数:c点>b点
B.b点混合溶液显酸性:c(Na+)>c(NO2﹣)>c(H+)>c(OH﹣)
C.c点混合溶液中:c(OH﹣)>c(HNO2)
D.d点混合溶液中:c(Na+)>c(OH﹣)>c(NO2﹣)>c(H+)
【答案】B
【解析】解:A、HNO2的电离是吸热过程,温度越高电离平衡常数越大,而c高于b,所以电离平衡常数:c点>b点,故A正确; B、b点得到HNO2 , 和NaNO2混合溶液显酸性,说明电离大于水解,所以离子浓度大小为:c(NO2﹣)>c(Na+)>c(H+)>c(OH﹣),故B错误;
C、a→c温度升高说明两者恰好完全中和,点两者恰好完全反应,而c→d温度降低,所水解为主,所以c点得到NaNO2溶液是强碱弱酸盐,水解溶液呈碱性,所以c(OH﹣)>c(HNO2),故C正确;
D、d点混合溶液中当c(NaOH)较大时,得到NaOH和NaNO2混合溶液,所以离子的浓度为:c(Na+)>c(OH﹣)>c(NO2﹣)>c(H+),故D正确;
故选B.
A、HNO2的电离是吸热过程,温度越高电离平衡常数越大;
B、b点得到HNO2 , 和NaNO2混合溶液显酸性,说明电离大于水解,由此分析解答,也可能结合电荷守恒分析;
C、a→c温度升高说明两者恰好完全中和,点两者恰好完全反应,而c→d温度降低,所水解为主;
D、d点混合溶液中当c(NaOH)较大时,得到NaOH和NaNO2混合溶液.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列图像分别表示有关反应的反应过程与能量变化的关系,据此判断下列说法中正确的是( )


A. 石墨转变为金刚石是放热反应
B. 白磷比红磷稳定
C. S(g)+O2(g)====SO2(g) ΔH1, S(s)+O2(g)====SO2(g) ΔH2 则ΔH1<ΔH2
D. CO(g)+H2O(g)====CO2(g)+H2(g) ΔH1>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开.在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅.已知:3I2+6OH﹣═IO3﹣+5I﹣+3H2O则下列说法不正确的是( ) 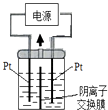
A.右侧发生的电极方程式:2H++2e﹣═H2↑
B.电解槽内发生反应的总化学方程式KI+3H2O═KIO3+3H2↑
C.如果用阳离子交换膜代替阴离子交换膜,电解槽内发生的总化学方程式不变
D.电解结束时,右侧溶液中含有IO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用无水Na2CO3配制250 mL 1.000 mol·L-1 Na2CO3溶液时,下列操作会使配制的溶液浓度偏大的是
A. 称量时碳酸钠固体含有结晶水
B. 移液时有液滴洒落瓶外
C. 定容时俯视容量瓶刻度线
D. 容量瓶没有干燥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是
A. 开启啤酒瓶后,瓶中立刻泛起大量泡沫
B. 由H2、I2蒸气、HI组成的平衡混合物加压后颜色变深
C. 向氯水中加适量NaHCO3后,溶液漂白能力增强
D. 在含有Fe(SCN)3的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是由4个圆所构成的元素概念的关系图,其中4为最大圆,3、2、1依次减小.试判断符合这种关系的是( )
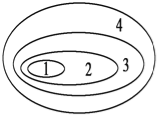
A. 1.大量元素、2.主要元素、3.基本元素、4.最基本元素
B. 1.基本元素、2.最基本元素、3.大量元素、4.主要元素
C. 1.最基本元素、2.基本元素、3.主要元素、4.大量元素
D. 1.主要元素、2.大量元素、3.最基本元素、4.基本元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com