
| A. | 不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛 | |
| B. | 不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液 | |
| C. | 如果浓H2SO4沾到皮肤上,可立即用大量水冲洗,然后涂上硼酸溶液 | |
| D. | 如果少量酒精失火燃烧,可用湿抹布盖灭火焰 |
分析 A.不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛,以最大程度减小对眼睛的危害.
B.根据浓碱溶液的腐蚀性分析;
C.浓硫酸具有较强较强的腐蚀性,不慎沾到皮肤上,应立即用布拭去;
D.从灭火的原理和方法分析,灭火的方法有:(1)与空气(或氧气)隔绝.(2)降温到可燃物的着火点以下.(3)撤走可燃物.
解答 解:A.不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛,以最大程度减小对眼睛的危害,故A正确.
B.浓碱具有腐蚀性,不慎洒在衣服上,用较多的水冲洗,再涂上硼酸溶液,故B正确;
C.浓硫酸具有较强的腐蚀性,不慎沾到皮肤上,应立即用布拭去,再用大量清水冲洗,然后涂上稀的碳酸氢钠溶液,故C错误;
D.酒精的密度小于水的密度,酒精燃烧时,用自来水灭火时不但不能灭火,而且能扩大燃烧面积,应该用湿抹布盖灭,故D正确.
故选C.
点评 本题考查了化学安全及事故处理,难度不大,注意配制稀硫酸时,是浓硫酸向蒸馏水中倒,不是蒸馏水向浓硫酸中倒.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
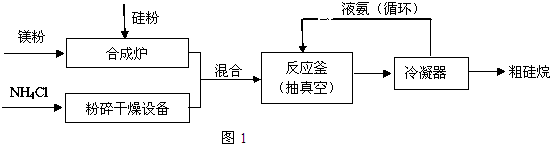
. (2)三硅酸镁(Mg2Si3O8?nH2O)难溶于水,在医药上可做抗酸剂.它除了可以中和胃液中多余酸之外,生成的H2SiO3还可覆盖在有溃疡的胃表面,保护其不再受刺激.三硅酸镁与盐酸反应的化学方程式为Mg2Si3O8?nH2O+4HCl═2MgCl2+3H2SiO3+(n-1)H2O.
(2)三硅酸镁(Mg2Si3O8?nH2O)难溶于水,在医药上可做抗酸剂.它除了可以中和胃液中多余酸之外,生成的H2SiO3还可覆盖在有溃疡的胃表面,保护其不再受刺激.三硅酸镁与盐酸反应的化学方程式为Mg2Si3O8?nH2O+4HCl═2MgCl2+3H2SiO3+(n-1)H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | 甲 | 乙 | 丙 |
| ① | CO2 | SO2 | 石灰水 |
| ② | HCI | CO2 | 石灰水 |
| ③ | NO2 | SO2 | BaCI2 |
| ④ | CO2 | NH3 | CaCI2 |
| A. | ②④ | B. | ① | C. | ①③ | D. | ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 醋酸溶于水:CH3COOH=CH3COO-+H+ | |
| B. | 熔融状态下的NaHSO4:NaHSO4=Na++H++SO42- | |
| C. | 碳酸氢钠溶于水:NaHCO3=HCO3-+Na+ | |
| D. | 硫化氢溶于水:H2S?2H++S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg在空气中燃烧 | |
| B. | 铁丝在Cl2中燃烧 | |
| C. | 足量铜与浓硝酸充分反应得到的气体 | |
| D. | 足量的锌粒与浓硫酸反应得到的气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com