
【题目】短周期主族元素![]() 原子序数依次增大,
原子序数依次增大,![]() 同主族且与
同主族且与![]() 处于不同周期,
处于不同周期,![]() 同主族且
同主族且![]() 的原子序数是
的原子序数是![]() 的两倍,以下说法正确的是
的两倍,以下说法正确的是
A.原子半径:![]()
B.由![]() 组成的化合物中可能含共价键
组成的化合物中可能含共价键
C.![]() 元素最高价氧化物对应的水化物的酸性比
元素最高价氧化物对应的水化物的酸性比![]() 强
强
D.![]() 的简单气态氢化物的热稳定性比
的简单气态氢化物的热稳定性比![]() 的弱
的弱
【答案】B
【解析】
短周期主族元素X、Y、Z、W、Q原子序数依次增大,Y、W同主族且W的原子序数是Y的两倍,则Y为O,W为S;X、Z同主族且与Y处于不同周期,则X为H,Z为Na元素;Q的原子序数大于S,则Q为Cl元素,据此结合元素周期律知识解答。
根据分析可知,X为H,Y为O,Z为Na,W为S元素,Q为Cl元素,
A.同一周期从左向右原子半径逐渐减小,同一主族从上到下原子半径逐渐增大,则原子半径r(Z)>r(W)>r(Y)>r(X),故A错误;
B.O、Na形成的过氧化钠中含有共价键,故B正确;
C.非金属性S<Cl,则W元素最高价氧化物对应的水化物的酸性比Q弱,故C错误;
D.非金属性O>S,则Y的简单气态氢化物的热稳定性比W的强,故D错误;
故答案为B。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】某化学兴趣小组设计了如图装置,该装置能制取Cl2,并进行相关性质实验,且可利用装置G储存多余的氯气。
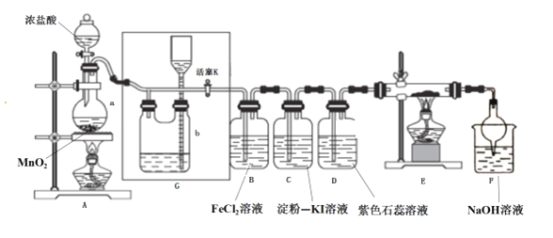
(1)A中发生反应的化学反应方程式为________________________________
(2)实验开始时,先打开分液漏斗旋塞和活塞K,点燃A处酒精灯,让氯气充满整个装置,再点燃E处酒精灯,回答下列问题:
①在装置D中能看到的实验现象分别是 ___________________ ;
②在装置E的硬质玻璃管内盛有碳粉,发生氧化还原反应,产物为CO2和HCl,则E中发生反应的化学方程式为______________________________;
③装置F中球形干燥管的作用是____________________________;
(3)储气瓶b内盛放的试剂是______________________________;
(4)B处发生反应的离子方程式为___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X(g)+3Y(g)![]() 2W(g) +M(s) △H=-a kJ·mol-1(a>0),一定温度下,在容积为1L密闭容器中,加入1 mol X(g)与1mol Y(g),2s后Y的物质的量浓度为0.4 mol·L-1,下列说法正确的是
2W(g) +M(s) △H=-a kJ·mol-1(a>0),一定温度下,在容积为1L密闭容器中,加入1 mol X(g)与1mol Y(g),2s后Y的物质的量浓度为0.4 mol·L-1,下列说法正确的是
A.X体积分数保持不变,说明反应已经达到平衡状态
B.若减小Y的浓度,则正反应速率减小,逆反应速率增大
C.0~2s, W的平均反应速率为0.2mol·L-1·s-1
D.反应达到平衡状态时,W与M的物质的量浓度比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过一硫酸氢钾复合盐(KHSO4·2KHSO5·K2SO4)常用作漂白剂和消毒剂,其制备流程如图:
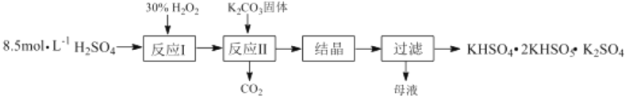
(1)反应Ⅰ的化学方程式为:H2O2+H2SO4H2SO5+H2O,△H<0;则反应Ⅱ中K2CO3与H2SO5反应生成KHSO5的化学方程式为___。
(2)生产原料的理论比值[n(H2O2):n(H2SO4)]为0.4:1,但实际生产最佳投料比为0.6:1,其原因是___。
(3)准确称取3.350g复合盐样品配制成250mL溶液,取25.00mL置于锥形瓶中,加入适量的稀硫酸和足量的KI溶液,摇匀后置于暗处,充分反应后,加入少量淀粉溶液,用0.1000mol·L-1Na2S2O3标准溶液滴定至终点,消粍标准溶液20.00mL。计算复合盐中有效成分KHSO5的质量分数。(写出计算过程)(已知:HSO5-+I-+H+→SO42-+I2+H2O,I2+S2O32-→I-+S4O62--未配平)___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下反应可表示获得乙醇并用作汽车燃料的过程,下列有关说法正确的是( )
①6CO2(g)+6H2O(l)=C6H12O6(s)+6O2(g) ΔH1
②C6H12O6(s)=2C2H5OH(l)+2CO2(g) ΔH2
③C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l) ΔH3
A.2ΔH3=ΔH1-ΔH2
B.ΔH3、ΔH1、ΔH2均为ΔH<0
C.在不同油耗汽车中发生反应③,ΔH3会不同
D.植物的光合作用通过反应①将热能转化为化学能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,在“H2A—HA-—A2-”的水溶液体系中,H2A、HA-和A2- 三者中各自所占的物质的量分数(α)随溶液pH变化的关系如图所示。下列说法正确的是
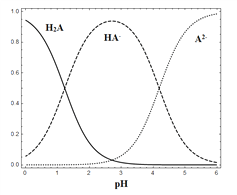
A. 在含H2A、HA-和A2- 的溶液中,加入少量NaOH固体,α(HA-)一定增大
B. 将等物质的量的NaHA和Na2A混合物溶于水,所得的溶液中α(HA-)=α(A2-)
C. NaHA溶液中,HA-的水解能力小于HA-的电离能力
D. 在含H2A、HA-和A2-的溶液中,若c(H2A)+2c(A2-)+c(OH-)=c(H+),则α(H2A)和α(HA-)一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.常温下,向0.1mol·L-1的醋酸溶液中加水稀释,溶液中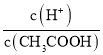 增大
增大
B.反应N2(g)+3H2(g) ![]() 2NH3(g) △H<0达平衡后,降低温度,正反应速率增大、逆反应速率减小,平衡向正反应方向移动
2NH3(g) △H<0达平衡后,降低温度,正反应速率增大、逆反应速率减小,平衡向正反应方向移动
C.铜锌原电池中,盐桥中的K+和NO3-分别移向正极和负极
D.电解精炼铜时,阳极泥中含有Zn、Fe、Ag、Au等金属
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施或事实不能用勒夏特列原理解释的是
A.新制的氯水在光照下颜色变浅
B.H2、I2、HI平衡混合气加压后颜色变深
C.在合成氨的反应中,加压有利于氨的合成
D.Fe(SCN)3溶液中加入NaOH后溶液颜色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某有机物A的红外光谱和核磁共振氢谱如下图所示,下列说法中错误的是
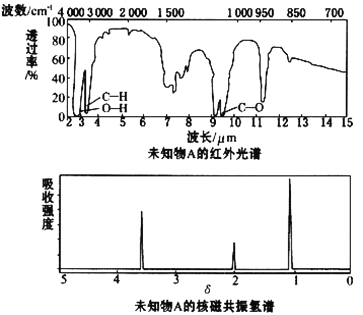
A. 由红外光谱可知,该有机物中至少含有三种不同的化学键
B. 由核磁共振氢谱可知,该有机物分子中有三种不同的氢原子且个数比为1:2:3
C. 仅由其核磁共振氢谱可知其分子中的氢原子总数
D. 若A的化学式为C2H6O,则其结构简式为CH3CH2OH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com