
下列事实不能说明Cl原子的得电子能力比S原子强的是( )
①HCl比H2S稳定
②HClO氧化性比H2SO4强
③HClO4酸性比H2SO4强
④Cl2能与H2S反应生成S
⑤Cl原子最外层有7个电子,S原子最外层有6个电子
⑥Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS
A.②⑤ B.①② C.①②④ D.①③⑤
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2014年高考化学一轮复习课后规范训练7-3练习卷(解析版) 题型:选择题
已知:2CH3OH(g)  CH3OCH3(g)+H2O(g) ΔH=-25 kJ/mol某温度下的平衡常数为400。此温度下,在1 L的密闭容器中加入CH3OH,反应到某时刻测得各组分的物质的量浓度如下:
CH3OCH3(g)+H2O(g) ΔH=-25 kJ/mol某温度下的平衡常数为400。此温度下,在1 L的密闭容器中加入CH3OH,反应到某时刻测得各组分的物质的量浓度如下:
物质 | CH3OH | CH3OCH3 | H2O |
c/(mol·L-1) | 0.8 | 1.24 | 1.24 |
下列说法正确的是( )
①平衡后升高温度,平衡常数>400
②平衡时,c(CH3OCH3)=1.6 mol/L
③平衡时,反应混合物的总能量减少20 kJ
④平衡时,再加入与起始等量的CH3OH,达新平衡后CH3OH转化率增大
⑤此时刻反应达到平衡状态
⑥平衡时CH3OH的浓度为0.08 mol·L-1
A.①②④⑤ B.②⑥ C.②③④⑥ D.②④⑥
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练6-1练习卷(解析版) 题型:选择题
已知C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g) ΔH1=-a kJ/mol
C2H5OH(g)=C2H5OH(l) ΔH2=-b kJ/mol
H2O(g)=H2O(l) ΔH3=-c kJ/mol
若使92 g酒精液体完全燃烧,最后恢复到室温,则放出的热量(单位kJ)为( )
A.4a+4b+4c B.2a-2b+6c
C.2a-2b+2c D.2a-6b+2c
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练5-3练习卷(解析版) 题型:选择题
下列有关化学用语的使用正确的是( )
A.CH4分子的比例模型:
B.NH3的电子式: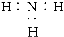
C.Cl-的结构示意图: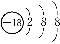
D.CO2的结构式:O=C=O
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练5-2练习卷(解析版) 题型:选择题
下表是部分短周期元素的原子半径及主要化合价,以下叙述正确的是( )
元素代号 | L | M | Q | R | T |
原子半径 | 0.160 nm | 0.143 nm | 0.112 nm | 0.104 nm | 0.066 nm |
主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
A.气态氢化物的稳定性为H2T<H2R
B.单质与稀盐酸反应的速率为L<Q
C.M与T形成的化合物具有两性
D.L2+与R2-的核外电子数相等
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练5-1练习卷(解析版) 题型:填空题
A、B、C、D、E、F、G七种短周期主族元素的原子序数依次增大。A和E最外层电子数相同,短周期主族元素的原子中,E原子的半径最大;B、C和F在周期表中相邻,B、C同周期,C、F同主族,F原子的质子数是C原子质子数的2倍;A和C可形成两种常见的液态化合物X和Y(相对分子质量X<Y);D形成的分子为双原子分子。回答问题:
(1)D元素的名称为 ,F形成的离子的结构示意图为 。
(2)写出液态化合物Y的一种用途 。
(3)用某种金属易拉罐与A、C、E组成的化合物的水溶液反应,产生的气体可充填气球,请写出该反应的离子方程式 ,使用这种气球存在的隐患是 。
(4)P和Q两种物质都是由A、C、E、F四种元素组成的盐,其水溶液都显酸性,等物质的量的P和Q恰好完全反应。写出该反应的离子方程式: 。
(5)A、B、G三种元素两两组合形成的化合物在空气中相遇形成白烟,反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练5-1练习卷(解析版) 题型:选择题
从宏观方面看物质是由元素组成的,从微观方面看物质是由粒子构成的,下列有关说法不正确的是( )
A.元素原子的多样性是由构成原子的质子和中子数目引起的
B.元素的化学性质主要取决于元素原子的最外层电子数
C.只由一种分子构成的物质一定是纯净物
D.质子数等于电子数的微粒,可能是一种分子和一种离子
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练4-4练习卷(解析版) 题型:选择题
下列工业生产中,各物质的物质的量间的关系式不正确的是( )
A.制漂白粉:2Cl2~Ca(ClO)2
B.制H2SO4:FeS2~2H2SO4
C.合成氨:C~H2~2/3NH3
D.制HNO3:NH3~HNO3
查看答案和解析>>
科目:高中化学 来源:2014年高考化学一轮复习课后规范训练4-1练习卷(解析版) 题型:选择题
向存在大量K+、Cl-的溶液中通入足量CO2后,该溶液中还可能大量存在的离子组是( )
A.Na+、Br-、CO32- B.AlO2-、Na+、MnO4-
C.NH4+、Na+、SO42- D.Na+、Ag+、NO3-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com