
【题目】某离子反应中涉及H2O、ClO-、NH4+、H+、N2、Cl-六种微粒。常温条件下反应时,溶液pH 随时间变化的曲线如图所示。下列判断错误的是
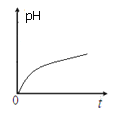
A.该反应的氧化剂是ClO-
B.该反应中有两种离子生成
C.该反应生成1mol氧化产物时,转移的电子为6 mol
D.参加反应的氧化剂与还原剂的物质的量之比为2 : 3
【答案】D
【解析】
试题分析:由图象分析可知,pH值随反应进行逐渐增大,ClO-应是反应物,氯元素化合价降低,是氧化剂,具有还原性的NH4+为反应物,由氮元素守恒可知N2是生成物,结合电子守恒、电荷守恒及原子守恒可得此反应的离子方程式应为3ClO-+2NH4+=N2↑+3H2O+3Cl-+2H+。A.根据上述分析,该反应的氧化剂是ClO-,A项正确;B.该反应中有Cl-和H+两种离子生成,B项正确;C.由离子方程式可知,N元素化合价由-3价升高到0价,则该反应生成1mol氧化产物时,转移的电子为6 mol,C项正确;D.由方程式可知氧化剂和还原剂的物质的量之比为3:2,D项错误;答案选D。


 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:
【题目】下列关于物质分类的正确组合是( )
A.碱:Na2CO3 酸: H2SO4 盐: NaHCO3 碱性氧化物: SiO2 酸性氧化物: CO2
B.碱:NaOH 酸: HCl 盐: NaCl 碱性氧化物: Na2O 酸性氧化物: CO
C.碱:NaOH 酸: CH3COOH 盐: CaF2 碱性氧化物: SO3 酸性氧化物: SO2
D.碱:KOH 酸: HNO3 盐: CaCO3 碱性氧化物: CaO 酸性氧化物: SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学—选修5:有机化学基础]A的产量可以用来衡量—个国家的石油化工发展水平。用A为原料可以合成一种醚类香料和一种缩醛类香料。具体合成路线如下图所示(部分反应条件略去):

回答下列问题:
(1)A的名称是_______,图中缩醛的分子式是_______________。
(2)B的结构简式为__________,C中含有的官能团名称是________________。
(3)D为单取代芳香族化合物且能与金属钠反应。反应⑤的化学方程式为_______________。
(4)反应⑥的反应类型是__________________。
(5)写出满足下列条件的苯乙醛的所有同分异构体的结构简式:______________。
A.含有苯环和![]() 结构;B.核磁共振氢谱有4组峰,且峰面积之比为3:2:2:1
结构;B.核磁共振氢谱有4组峰,且峰面积之比为3:2:2:1
(6)参照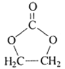 的合成路线,设计一条由2-氯丙烷制备
的合成路线,设计一条由2-氯丙烷制备 的合成路线(注明必要的反应条件)________________。
的合成路线(注明必要的反应条件)________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分离方法不合理的是( )
A. 用分馏的方法,可从石油中得到汽油
B. 提取溴水中的溴,可用加入乙醇萃取的方法
C. 只含有泥沙的粗盐,可通过溶解、过滤、结晶的方法提纯
D. 除FeCl2溶液中的少量FeCl3,可用加入足量铁屑过滤的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】捕碳技术(主要指捕获CO2)在降低温室气体排放中具有重要的作用。
在海洋碳循环中,通过右图所示的途径固碳。

①写出钙化作用的离子方程式:______ ______________。
②同位素示踪法证实光合作用释放出的O2只来自于H2O。 用18O标记光合作用的化学方程式如下,将其补充完整。
__________+__________![]() (CH2O)x+x18O2+ xH2O)
(CH2O)x+x18O2+ xH2O)
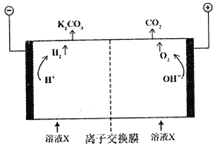
(2)工业上常用高浓度K2CO3溶液吸收CO2得到溶液X,再利用电解法使K2CO3溶液再生,并将CO2富集,其装置如下图。在阳极区发生的反应包括_________和H++HCO3-=H2O+CO2↑。简述CO32-在阴极区再生的原理:______________。
(3)将上述富集的CO2和甲烷重整制合成气(CO和H2)是CO2资源化利用的有效途径。合成气用干制备甲醇的反应为:2H2(g) +CO (g) ![]() CH3OH(g) △H=-90.l kJ/mol
CH3OH(g) △H=-90.l kJ/mol
在T℃时,容积相同的甲、乙、丙三个恒容密闭容器中,按不同方式投入反应物,测得反应达到平衡时的有关数据如下表。

根据上表信息填空(填写“>”“< ”或“=”):
2c1_________c3;②|x|+|y|___________90.1;
③2p2_________p3;④α1+α2_________1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是元素周期表的一部分,用表中①~⑨的元素符号或物质化学式回答问题:
族 周 期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
一 | ||||||||
二 | ① | ② | ③ | ④ | ||||
三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(1)元素⑥的原子的核外电子数为_______,原子的L层电子数是K层2倍的元素为
_______(填元素符号);
(2)化学性质最不活泼的元素原子的原子结构示意图为____________;
(3)①~⑧中,元素原子半径最大的是________(填元素符号),这些元素的最高价氧化物对应的水化物中,酸性最强的酸是________(填化学式);
(4)请写出元素⑤的过氧化物的电子式______________;
(5)用电子式表示元素②的氢化物的形成过程________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.工业上有一种用CO2来生产甲醇燃料的方法:
CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) △H=-49.0kJ·mol-1
CH3OH(g)+H2O(g) △H=-49.0kJ·mol-1
将6 mol CO2和8 mol H2充入2 L的密闭容器中,测得H2的物质的量随时间变化如下图所示(实线)。图中数据a(1,6)表示:在1 min时H2的物质的量是6 mol。
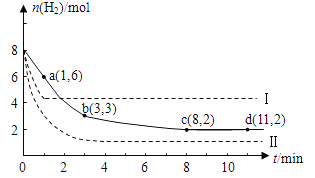
(1)a点正反应速率 (填“大于”“等于”或“小于”)逆反应速率。计算其化学平衡常数K=
(2)下列时间段平均反应速率最大的是
A.O~1 min B.1~3 min C.3~8 min D.8~11 min
(3)仅改变某一实验条件再进行两次实验测得H2的物质的量随时间变化如图中虚线所示。曲线I对应的实验条件改变是 ,曲线Ⅱ对应的实验条件改变是 。
(4)锰酸锂、钛酸锂都是绿色环保新型能源材料,可以用MnO2为原料制取锰酸锂。
①以石墨为电极,电解酸化的MnSO4溶液可制备MnO2,则阳极的电极反应式为 。
②MnO2是碱性锌锰电池的正极材料.碱性锌锰电池放电时,正极的电极反应式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com