
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是
A. ![]()
B. ![]()
C. ![]()
D. ![]()
【答案】A
【解析】分析:A项,NaHCO3受热分解成Na2CO3、CO2和H2O,Na2CO3与饱和石灰水反应生成CaCO3和NaOH;B项,Al与NaOH溶液反应生成NaAlO2和H2,NaAlO2与过量盐酸反应生成NaCl、AlCl3和H2O;C项,AgNO3中加入氨水可获得银氨溶液,蔗糖中不含醛基,蔗糖不能发生银镜反应;D项,Al与Fe2O3高温发生铝热反应生成Al2O3和Fe,Fe与HCl反应生成FeCl2和H2。
详解:A项,NaHCO3受热分解成Na2CO3、CO2和H2O,Na2CO3与饱和石灰水反应生成CaCO3和NaOH,两步反应均能实现;B项,Al与NaOH溶液反应生成NaAlO2和H2,NaAlO2与过量盐酸反应生成NaCl、AlCl3和H2O,第二步反应不能实现;C项,AgNO3中加入氨水可获得银氨溶液,蔗糖中不含醛基,蔗糖不能发生银镜反应,第二步反应不能实现;D项,Al与Fe2O3高温发生铝热反应生成Al2O3和Fe,Fe与HCl反应生成FeCl2和H2,第二步反应不能实现;物质间转化均能实现的是A项,答案选A。


科目:高中化学 来源: 题型:
【题目】下列解释事实的方程式不正确的是
A. 测得0. Imol/L氨水的pH为11: ![]()
B. 用NaCl溶液做铁的吸氧腐蚀实验,O2减少:![]()
C. 用H2、O2进行氢氧燃料电池实验,产生电流:![]()
D. 用NH4Cl溶液溶解Mg(OH)2,沉淀溶解![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某消毒液的主要成分为NaClO,还含有一定量的NaOH,下列用来解释事实的方程式中不合理的是(已知:饱和NaClO溶液的pH约为11)
A. 该消毒液可用NaOH溶液吸收Cl2制备:Cl2+2OH-="==" Cl-+ ClO-+ H2O
B. 该消毒液的pH约为12:ClO-+ H2O![]() HClO+ OH-
HClO+ OH-
C. 该消毒液与洁厕灵(主要成分为HCl)混用,产生Cl2:2H++ Cl-+ ClO-= Cl2↑+H2O
D. 该消毒液加白醋生成HClO,可增强漂白作用:CH3COOH+ ClO-= HClO+CH3COO—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质的叙述一定不正确的是
A. 向FeCl2溶液中滴加NH4SCN溶液,溶液显红色
B. KAl(SO4) 2·12H2O溶于水可形成 Al(OH)3胶体
C. NH4Cl与Ca(OH)2混合加热可生成NH3
D. Cu与FeCl3溶液反应可生成CuCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A. 饱和Na2CO3溶液与CaSO4固体反应:CO32+CaSO4![]() CaCO3+SO42
CaCO3+SO42
B. 酸化NaIO3和NaI的混合溶液:I +IO3+6H+![]() I2+3H2O
I2+3H2O
C. KClO碱性溶液与Fe(OH)3反应:3ClO+2Fe(OH)3![]() 2FeO42+3Cl+4H++H2O
2FeO42+3Cl+4H++H2O
D. 电解饱和食盐水:2Cl+2H+![]() Cl2↑+ H2↑
Cl2↑+ H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 氢氧燃料电池放电时化学能全部转化为电能
B. 反应4Fe(s)+3O2(g)![]() 2Fe2O3(s)常温下可自发进行,该反应为吸热反应
2Fe2O3(s)常温下可自发进行,该反应为吸热反应
C. 3 mol H2与1 mol N2混合反应生成NH3,转移电子的数目小于6×6.02×1023
D. 在酶催化淀粉水解反应中,温度越高淀粉水解速率越快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,等质量的 SO2 气体和 SO3 气体相比较,下列叙述中正确的是
A. 物质的量之比为 4:5 B. 密度比为 4:5
C. 体积比为 1:1 D. 原子数之比为 3:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法正确的是( )
A. MgCl2的摩尔质量为95g
B. 18g H2O含有的原子总数为3NA
C. 0.5mol H2所占体积约为11.2L
D. 0.1 mol·L-1 BaCl2溶液中,Cl-的物质的量浓度为0.1 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯氧磷(POCl3)是一种工业化工原料。无色透明的带刺激性臭味的液体,在潮湿空气中剧烈发烟。某化学小组采用PCl3氧化法制备POCl3。已知:POCl3的熔点为-112℃,沸点为75.5℃。在潮湿空气中二者均极易水解面剧烈“发烟”。回答下列问题:
I.制备PCl3
(1)实验室用高锰酸钾和浓盐酸反应制取氯气。发生装置可以选择图中的_____(填字母代号)。
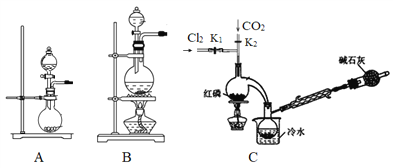
(2)检查装置气密性并装入药品后,先关闭K1,打开K2通入干燥的CO2,一段时间后,关闭K2,加热曲颈瓶同时打开K1通入干燥氯气,反应立即进行。通干燥CO2的作用是_______。
II.制备POCl3(如图)
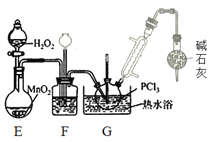
(3)盛放碱石灰的仪器的作用是________,装置G中发生反应的化学方程式为________ 。
(4)装置F的作用除观察O2的流速之外,还有________。
III.测定POCl3含量
实验制得的POCl3中常含有PCl3杂质,通过下面方法可测定产品的纯度:
①快速称取5.000g产品,加水反应后配成250mL溶液;
②取以上溶液25.00mL,向其中加入10.00mL0.1000mol/L碘水(足量),充分反应;
③向②所得溶液中加入几滴淀粉溶液,用0.1000mol/L的Na2S2O3溶液滴定;
④重复②、③操作,平均消耗0.1000mol/LNa2S2O3溶液8.00mL.
已知:H3PO3+I2+H2O==H3PO4+2HI,I2+2Na2S2O3==2NaI+Na2S4O6.
(5)滴定终点的现象为__________。该产品的纯度为________。
(6)若滴定管在滴定前无气泡,滴定后有气泡,则测定结果______(填“偏高”“偏低”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com