
����Ŀ���ѻӷ��Զ�������TaS2 ���ɲ�������װ���ᴿ����������TaS2 ��ĩװ��ʯӢ��һ�ˣ�����պ����������Ⲣ��ܣ����ڼ���¯�С���Ӧ���£�
TaS2��g��+2I2��g��![]() TaI4��g��+S2��g��
TaI4��g��+S2��g��
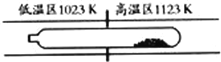
����˵����ȷ���� �� ��
A���ڲ�ͬ�¶�����TaI4 �������ֲ���
B�����ᴿ�����У�I2 �������ϼ���
C�����ᴿ�����У�I2�������ǽ�TaS2 �Ӹ�����ת�Ƶ�������
D��������Ӧ��ƽ�ⳣ����TaI4 ��S2 ��Ũ�ȳ˻��ɷ���

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ͪ��һ��ҽҩ�м��壬��ṹ��ʽ��ͼ��ʾ������˵����ȷ����( )
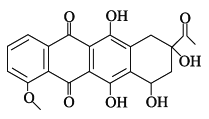
A. ÿ�����ͪ�����к��� 1 ������̼ԭ�ӣ������ĸ���ͬ���ŵ�̼ԭ�ӣ�
B. ���ͪ���������е�̼ԭ�Ӷ���ͬһ��ƽ����
C. һ�����������ͪ�ɷ����������ӳɡ���ȥ��Ӧ
D. 1 mol ���ͪ������ 4 mol �����ᷢ��ȡ����Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ӵ���Һ�зֱ����SO3�������Һ���������Ӹ���������ǣ�������
A.Mg2+B.CO32��C.Ba2+D.SO32��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£�ij�ݻ��̶����ܱ������У��������л�ѧƽ�⣺C(s)��H2O(g)![]() CO(g)
CO(g)
��H2(g)�����������в���˵���������淴Ӧ�Ѵﵽ��ѧƽ��״̬���ǣ� ��
A. ��ϵ��ѹǿ���ٷ����仯
B. v��(CO)��v��(H2O)
C. ����n mol CO��ͬʱ����n mol H2
D. 1 mol H��H�����ѵ�ͬʱ����2 mol H��O��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I.A~D�����������ӵ����ģ��(��ͼ)
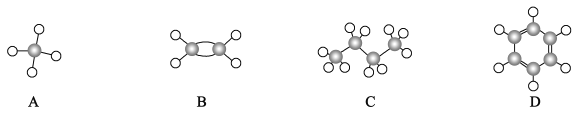
(1)����ԭ��һ����ƽ�����______(�����)
(2)��ʹ���Ը��������Һ��ɫ��������_____ (�����)
(3)D��Ũ�����Ũ���Ṳ�ȵĻ�ѧ����ʽ______��
II.ijЩ�л����ת������ͼ��ʾ����֪:A��Ӫ������֮һ��������ͷ�и���A��������������ˮ������ղ�����B��C�ǰƵ���Ҫ�ɷ֣�D��ˮ��Һ��ʹ��ɫʯ����Һ��졣
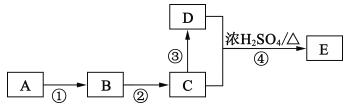
(4)C�й����ŵ�����Ϊ______����Ӧ�۵ķ�Ӧ����Ϊ______����Ӧ�ܵĻ�ѧ����ʽΪ______��
(5)��Ӧ���У�D���ѵĻ�ѧ����_______ (�CһH������OһH����CһO��)
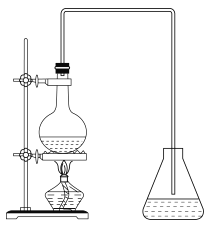
(6)ʵ�����ɷ�Ӧ���Ʊ�E��װ����ͼ��ʾ����ƿ�����μ���C��Ũ���ᡢD�����Ƭ����ƿ�м�����DZ���̼������Һ��ʵ�����������ƿ��Һ�壬���������ݲ������������ݵ�ԭ����__________(�����ӷ���ʽ��ʾ)������ƿ�е�Һ�����ķ�����_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ĿǰΪֹ���ɻ�ѧ��ת������ܻ������Ȼ������ʹ������Ҫ����Դ��
��1����ѧ��Ӧ�зų������ܣ��ʱ䣬��H���뷴Ӧ���������ļ��ܣ�E���йأ���֪��H2��g��+Cl2��g��=2HCl��g����H=��a kJmol��1��E��H��H��=b kJmol��1 �� E��Cl��Cl��=c kJmol��1 �� ��E��H��Cl��=��
��2����ԭ�Ӷ�O3�ķֽ��д����ã�O3��g��+Cl��g��=ClO��g��+O2��g����H1 �� ClO��g��+O��g��=Cl��g��+O2��g����H2 �� ����������ķֽⷴӦ��O3+O=2O2��H���÷�Ӧ�������仯ʾ��ͼ��ͼ1��ʾ����ӦO3��g��+O��g��=2O2��g��������Ӧ�Ļ��ΪkJmol��1 �� 
��3��ʵ���в���ֱ�Ӳ����ʯī��������Ӧ���ɼ��鷴Ӧ�ķ�Ӧ�ȣ����ɲ��CH4��ʯī��H2ȼ�շ�Ӧ�ķ�Ӧ�ȣ�����ʯī���ɼ���ķ�Ӧ�ȣ���֪��
��CH4��g��+2O2��g���TCO2��g��+2H2O��l����H=��a kJmol��1
��C��ʯī��+O2��g���TCO2��g����H=��b kJmol��1
��H2��g��+ ![]() O2��g���TH2O��l����H=��c kJmol��1
O2��g���TH2O��l����H=��c kJmol��1
��ӦC��ʯī��+2H2��g����CH4��g���ķ�Ӧ�ȣ�
��H=kJmol��1 ��
����֪���÷�ӦΪ���ȷ�Ӧ����H��T��S����Ϊ��Ӧ������оݣ�����H��T��S��0ʱ���Է����У���÷�Ӧ��ʲô�����¿��Է����� �� ������¡��������¡���
��4����ͼ2��ʾ��װ�ã���װ����Cu��Ϊ������ͭƬ�������仯Ϊ12.8gʱ��a�������ĵ�O2�ڱ�״���µ����ΪL��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݿ�ͼ����������˵������ȷ����
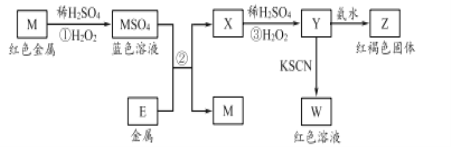
A. �ҹ�������������ʹ�÷�Ӧ��ұ������M�Ĺ���
B. M2+�������Ա�E2+��������ǿ
C. �ڷ�Ӧ����������ϡ���ᣬ���ܹ۲쵽���ɫ����
D. �ڷ�Ӧ����ϡ����ȱ��ֳ��������ֱ��ֳ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������CO����ϳɼ״�(CH3OH)����ȩ(CH3CHO)���Ҵ���̼�ĺ����������ǽ�������ѧ��Ƚϻ�Ծ���о�����֮һ��
��1����֪��������CO(g)+2H2(g)![]() CH3OH(g) ��H1=-90.1kJ/mol
CH3OH(g) ��H1=-90.1kJ/mol
������2CH3OH(g)![]() CH3OCH3(g)+H2O(g) ��H2=-24.5kJ/mol
CH3OCH3(g)+H2O(g) ��H2=-24.5kJ/mol
������C2H5OH(g)![]() CH3OCH3(g) ��H3=+50.7kJ/mol
CH3OCH3(g) ��H3=+50.7kJ/mol
����CO�������Ʊ��Ҵ�����(��һ����Ϊˮ����)���Ȼ�ѧ��Ӧ����ʽΪ________��
��2��ֱ�Ӽ״�ȼ�ϵ��(DMFC)�ɱ��͡�Ч�ʸߣ�ij�о���������DMFC���������Ʒ�ˮ�����ڷ�ˮpHl0~12.5���������У�CN���ȱ�������CNO��(���������е�Ԫ�ؾ�Ϊ-3��)���ٽ�һ������Ϊ̼���κ�N2��
����д��CNO���������ĵ缫��Ӧʽ________��
��������1m3CN������Ϊ390mg/L�ĵ�Ʒ�ˮ����������________kg�״���
��3����2.0L�ܱ������з���1 molCO��2molH2���ڷ�Ӧ�¶�T1ʱ�������·�Ӧ��
CO(g)+2H2(g)=CH3OH(g)����Ӧʱ��(t)�����������������ʵ���(n)�����ݼ��±���
ʱ��t/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
�����ʵ���n/mol | 3.0 | 2.7 | 2.5 | 2.3 | 2.1 | 2.0 | 2.0 |
����0~5minʱ�Σ���Ӧ����v(CH3OH)Ϊ________�����������������Ӧƽ��ת���ʵ�������________��
A.���¸�ѹ B.���µ�ѹ C.���µ�ѹ D.���¸�ѹ
�ڼ����¶�T1ʱ��Ӧ��ƽ�ⳣ��K1________��T1ʱ��ƽ��ı䷴Ӧ�¶�ΪT2��ƽ�ⳣ��������T2________T1(������������С����)���ж�������________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com