
| A. | 质谱法是测定有机物所含官能团的常用方法 | |
| B. | 红外光谱常用来测定有机物所含几种类型的氢原子 | |
| C. | 核磁共振氢谱可以区别乙醇与甲醚 | |
| D. | 红外光谱不能分别乙醇和甲醚 |
分析 A.质谱法用于测定有机物的相对分子质量;
B.红外光谱仪能测定出有机物的官能团和化学键;
C.核磁共振氢谱中吸收峰的数目等于于有机物分子中H原子种类,H原子数目之比等于对应峰的面积之比;
D.红外光谱仪能测定出有机物的官能团和化学键.
解答 解:A.质谱法用于测定有机物的相对分子质量,红外光谱仪能测定出有机物的官能团,故A错误;
B.红外光谱仪能测定出有机物的官能团,核磁共振氢谱中吸收峰的数目等于于有机物分子中H原子种类,故B错误;
C.乙醇含有3种H原子,而甲醚含有1种H原子,可以用核磁共振氢谱区别,故C正确;
D.乙醇含有羟基,甲醚含有醚键,可以用红外光谱仪区别,故D错误,
故选C.
点评 本题考查了有机物测定常用谱图,比较基础,旨在考查学生对基础知识的理解掌握.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 实验步骤 | 预期现象和结论 |
| 步骤1: | |
| 步骤2: | |
| 步骤3: |
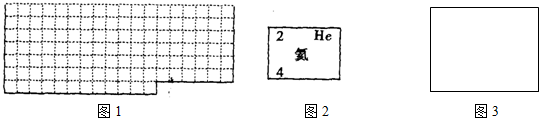
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
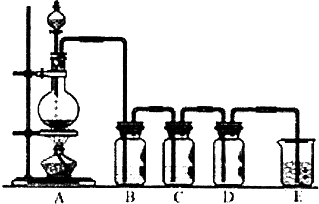 (1)若利用如图装置制备纯净、干燥的氯气,装置A中反应的化学方程式为MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.则装置B中的液体是饱和NaCl溶液;装置C中试剂的作用是干燥氯气
(1)若利用如图装置制备纯净、干燥的氯气,装置A中反应的化学方程式为MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.则装置B中的液体是饱和NaCl溶液;装置C中试剂的作用是干燥氯气查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 4 | ⑨ | ⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10mL 0.4mol/L硝酸 | B. | 10mL 0.2mol/L硫酸 | ||
| C. | 10mL 0.2mol/L盐酸 | D. | 50mL 0.1mol/L盐酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com